向NaOH和Na2CO3混合溶液中滴加1mol/L的稀盐酸,CO2的生成量与加入盐酸的量的关系如图所示。下列判断正确的是
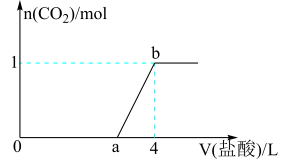

| A.a=0.3 |
B.ab段发生反应的离子方程式为CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| C.在0~a范围内,发生中和反应和复分解反应 |
| D.原混合溶液中NaOH与Na2CO3的物质的量之比为1∶1 |
更新时间:2023-01-01 23:01:36
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】2.0g铜镁合金完全溶解于50mL密度为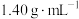 ,质量分数为63%的浓硝酸中,无固体剩余,得到
,质量分数为63%的浓硝酸中,无固体剩余,得到 和NO的混合气体1344mL(标准状况),向反应后的溶液中加入
和NO的混合气体1344mL(标准状况),向反应后的溶液中加入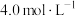 NaOH溶液,当金属离子全部沉淀时,得到3.7g沉淀,下列说法不正确的是
NaOH溶液,当金属离子全部沉淀时,得到3.7g沉淀,下列说法不正确的是
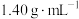 ,质量分数为63%的浓硝酸中,无固体剩余,得到
,质量分数为63%的浓硝酸中,无固体剩余,得到 和NO的混合气体1344mL(标准状况),向反应后的溶液中加入
和NO的混合气体1344mL(标准状况),向反应后的溶液中加入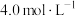 NaOH溶液,当金属离子全部沉淀时,得到3.7g沉淀,下列说法不正确的是
NaOH溶液,当金属离子全部沉淀时,得到3.7g沉淀,下列说法不正确的是| A.溶解铜镁合金的反应中,起酸性作用的硝酸的物质的量为0.1mol |
| B.将所得气体通入水中,还需标准状况下560mL的氧气可使气体恰好被完全吸收 |
C. 和NO的混合气体中, 和NO的混合气体中, 的体积分数是40% 的体积分数是40% |
| D.得到3.7g沉淀时,加入NaOH溶液的至少体积是160mL |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】把27g含镁、铝、铜的合金粉末分为两等份,一份放入过量氢氧化钠溶液中,得到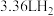 (标准状况),另一份放入过量盐酸中,得到
(标准状况),另一份放入过量盐酸中,得到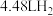 (标准状况)。该合金中镁、铝、铜的物质的量之比为
(标准状况)。该合金中镁、铝、铜的物质的量之比为
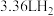 (标准状况),另一份放入过量盐酸中,得到
(标准状况),另一份放入过量盐酸中,得到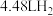 (标准状况)。该合金中镁、铝、铜的物质的量之比为
(标准状况)。该合金中镁、铝、铜的物质的量之比为| A.2:1:3 | B.2:4:1 | C.1:2:3 | D.3:2:4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】草酸晶体(H2C2O4⋅2H2O)用途广泛,易溶于水,其制备及纯度测定实验如下。
I.制备
步骤1:将mg淀粉溶于水与少量硫酸加入反应器中,保持85~90℃约30min,然后逐渐降温至60℃左右。
步骤2:控制反应温度在55~60℃条件下,边搅拌边缓慢滴加含有适量催化剂的混酸(65%硝酸与98%硫酸),主要反应为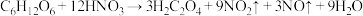 。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体
。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体 。
。
Ⅱ.纯度测定
称取制得的草酸晶体 ,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。对于上述实验,下列说法正确的是
,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。对于上述实验,下列说法正确的是
I.制备
步骤1:将mg淀粉溶于水与少量硫酸加入反应器中,保持85~90℃约30min,然后逐渐降温至60℃左右。
步骤2:控制反应温度在55~60℃条件下,边搅拌边缓慢滴加含有适量催化剂的混酸(65%硝酸与98%硫酸),主要反应为
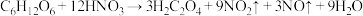 。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体
。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体 。
。Ⅱ.纯度测定
称取制得的草酸晶体
 ,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。对于上述实验,下列说法正确的是
,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。对于上述实验,下列说法正确的是A.65%浓硝酸( )的物质的量浓度约为13.6mol·L-1 )的物质的量浓度约为13.6mol·L-1 |
B.草酸晶体的产率为 |
| C.配制的草酸溶液物质的量浓度为0.025cVmol·L-1 |
D.草酸晶体的纯度为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)、(3)、(4)图中分别有OA<AB,OA=AB,OA>AB,则下列分析与判断一定正确的是(不计CO2的溶解)
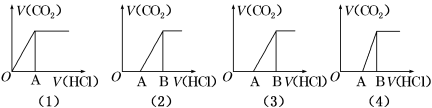
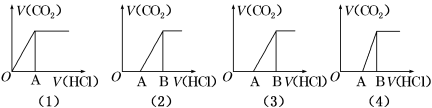
| A.(1)图显示M中只有一种溶质且为Na2CO3 |
| B.(3)图显示M中有两种溶质且为Na2CO3、NaOH |
| C.(2)图显示M中有两种溶质且为Na2CO3、NaHCO3 |
| D.(4)图显示M中c(NaHCO3)=c(Na2CO3) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某Na2CO3、NaAlO2的混合溶液中逐滴加入1 mol∙L−1的盐酸,测得溶液中的HCO 、CO
、CO 、AlO
、AlO 、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是
、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是
 、CO
、CO 、AlO
、AlO 、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是
、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是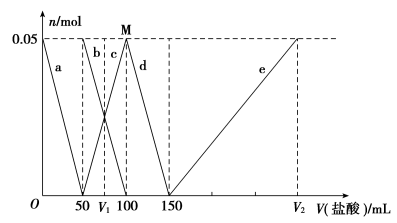
A.原混合溶液中的CO 与AlO 与AlO 的物质的量之比为1:2 的物质的量之比为1:2 |
| B.V1:V2=1:5 |
| C.M点时生成的CO2为0.05mol |
| D.e曲线表示的离子方程式为:Al(OH)3+3H+=Al3++3H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L1的盐酸,测得溶液中的CO32、HCO3、AlO2、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法正确的是( )(已知:H2CO3的电离平衡常数K1 = 4.3×107,K2 = 5.6×1011;Al(OH)3的酸式电离平衡常数K=6.3×1013)
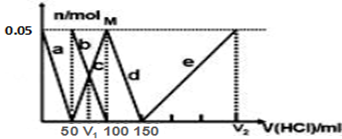

| A.a曲线表示的离子方程式为:AlO2+4H+ = Al3+ + 2H2O |
| B.M点时生成的CO2为0.05 mol |
| C.原混合溶液中的CO32与AlO2的物质的量之比为1:2 |
| D.V1:V2=1:4 |
您最近一年使用:0次



