按要求完成以下方程式:
(1)磁性氧化铁溶于盐酸的化学方程式:______ 。
(2)氯化铁溶液中通入SO2气体的离子方程式:______ 。
(3)偏铝酸钠溶液中通入过量CO2的离子方程式:______ 。
(4)碳单质和浓硝酸反应的化学方程式:______ 。
(1)磁性氧化铁溶于盐酸的化学方程式:
(2)氯化铁溶液中通入SO2气体的离子方程式:
(3)偏铝酸钠溶液中通入过量CO2的离子方程式:
(4)碳单质和浓硝酸反应的化学方程式:
12-13高一下·广东汕头·期末 查看更多[2]
更新时间:2016-12-08 20:51:22
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】有一无色透明溶液,欲确定其是否含有下列离子: 、
、 、
、 、
、 、
、 、
、 、
、 ,实验如下:
,实验如下:
①用玻璃棒蘸取少量该溶液,点在pH试纸中部,试纸变为红色;
②取少量该溶液,加入过量 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
③取②中反应后的上层清液,加入 溶液,有白色沉淀生成,且不溶于稀硝酸;
溶液,有白色沉淀生成,且不溶于稀硝酸;
④取少量原溶液,加入过量的NaOH溶液,有白色沉淀生成。
回答下列问题:
(1)溶液中一定存在的离子是______ ;溶液中肯定不存在的离子是______ 。
(2)分别写出实验②、③中发生反应的离子方程式:______ 。
(3)写出实验④中生成的沉淀的化学式:______ 。
(4)不能确定是否含有的离子是______ ,为了进一步确定其是否存在,应该补充的实验是______ (写出实验操作、现象和结论)。
 、
、 、
、 、
、 、
、 、
、 、
、 ,实验如下:
,实验如下:①用玻璃棒蘸取少量该溶液,点在pH试纸中部,试纸变为红色;
②取少量该溶液,加入过量
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;③取②中反应后的上层清液,加入
 溶液,有白色沉淀生成,且不溶于稀硝酸;
溶液,有白色沉淀生成,且不溶于稀硝酸;④取少量原溶液,加入过量的NaOH溶液,有白色沉淀生成。
回答下列问题:
(1)溶液中一定存在的离子是
(2)分别写出实验②、③中发生反应的离子方程式:
(3)写出实验④中生成的沉淀的化学式:
(4)不能确定是否含有的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】 Ⅰ.现有下列物质:①酒精、② 溶液、③硫酸、④
溶液、③硫酸、④ 、⑤
、⑤ 固体、⑥铁、⑦小苏打(
固体、⑥铁、⑦小苏打( )、⑧淀粉溶液
)、⑧淀粉溶液
(1)属于电解质的是:___________ ,(填序号,下同)属于非电解质的是:___________ 。
(2)其中在上述状态下能导电的有:___________ 。
(3)②⑧的微观本质区别是___________ 。
(4)写出②的电离方程式:___________ 。
Ⅱ.写出下列的离子方程式
(5)胃液中含有盐酸,用⑦能治疗胃酸过多的离子方程式___________ 。
(6)③和⑥溶液反应的离子方程式是___________ 。
(7)澄清石灰水检验 气体的离子方程式:
气体的离子方程式:___________ 。
(8)将⑤逐滴加入②的溶液中至恰好沉淀完全反应,离子方程式为:___________ 。
 溶液、③硫酸、④
溶液、③硫酸、④ 、⑤
、⑤ 固体、⑥铁、⑦小苏打(
固体、⑥铁、⑦小苏打( )、⑧淀粉溶液
)、⑧淀粉溶液(1)属于电解质的是:
(2)其中在上述状态下能导电的有:
(3)②⑧的微观本质区别是
(4)写出②的电离方程式:
Ⅱ.写出下列的离子方程式
(5)胃液中含有盐酸,用⑦能治疗胃酸过多的离子方程式
(6)③和⑥溶液反应的离子方程式是
(7)澄清石灰水检验
 气体的离子方程式:
气体的离子方程式:(8)将⑤逐滴加入②的溶液中至恰好沉淀完全反应,离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I、下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:
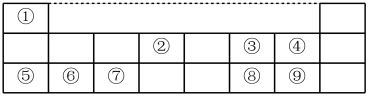
(1)元素⑧在周期表中的位置___________ ;
(2)在①~⑨元素中,某种元素的氧化物可用于呼吸面具中氧气来源,请写出该氧化物与二氧化碳反应的化学方程式___________ 。
(3)等质量的单质⑦分别与足量的稀硫酸和氢氧化钠溶液反应,相同条件下产生的气体体积之比为___________ 。
(4)元素⑨的单质可使湿润的淀粉-KI试纸变蓝,请写出离子方程式___________ 。
II、如图是某学校实验室从化学试剂商店采购的浓硫酸试剂标签上的部分内容。

(5)若实验室用该浓硫酸配制240mL0.5mol/L的稀硫酸,请计算需要该浓硫___________ mL(精确到小数点后1位)。
(6)配制过程中的正确操作顺序是:b、d___________ 、e(填“字母”)。
a、用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶。
b、用量筒量取所需体积浓硫酸注入盛有约50mL蒸馏水的烧杯。
c、用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。
d、用玻璃棒慢慢搅动,混合均匀。
e、盖好容量瓶瓶塞,反复上下颠倒,摇匀。
f、将稀释后的H2SO4溶液沿玻璃棒注入250mL容量瓶。
g、往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处。
(7)下列操作将导致所配制的H2SO4溶液浓度偏大的是___________ 。
a、移液过程有H2SO4溶液溅出瓶外
b、移液后未洗涤烧杯和玻璃棒
c、定容时俯视容量瓶刻度线
d、加水超过刻度线,用胶头滴管吸出多余液体
e、洗涤时将量筒洗涤液也加入容量瓶

(1)元素⑧在周期表中的位置
(2)在①~⑨元素中,某种元素的氧化物可用于呼吸面具中氧气来源,请写出该氧化物与二氧化碳反应的化学方程式
(3)等质量的单质⑦分别与足量的稀硫酸和氢氧化钠溶液反应,相同条件下产生的气体体积之比为
(4)元素⑨的单质可使湿润的淀粉-KI试纸变蓝,请写出离子方程式
II、如图是某学校实验室从化学试剂商店采购的浓硫酸试剂标签上的部分内容。

(5)若实验室用该浓硫酸配制240mL0.5mol/L的稀硫酸,请计算需要该浓硫
(6)配制过程中的正确操作顺序是:b、d
a、用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶。
b、用量筒量取所需体积浓硫酸注入盛有约50mL蒸馏水的烧杯。
c、用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。
d、用玻璃棒慢慢搅动,混合均匀。
e、盖好容量瓶瓶塞,反复上下颠倒,摇匀。
f、将稀释后的H2SO4溶液沿玻璃棒注入250mL容量瓶。
g、往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处。
(7)下列操作将导致所配制的H2SO4溶液浓度偏大的是
a、移液过程有H2SO4溶液溅出瓶外
b、移液后未洗涤烧杯和玻璃棒
c、定容时俯视容量瓶刻度线
d、加水超过刻度线,用胶头滴管吸出多余液体
e、洗涤时将量筒洗涤液也加入容量瓶
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据要求回答下列问题:
(1)写出下列物质在水溶液中的电离方程式:
① :
:__________ ;
②
___________ ;
③写出①②水溶液混合后恰好沉淀完全的离子方程式______________ ;
(2)标准状况下,相同质量的 和
和 物质的量比为
物质的量比为_____ ,所含氧原子数比为______ ,密度比为______ 。
(3)某建筑材料主要成分为铝硅酸盐,化学式是 ;改写成氧化物形式为
;改写成氧化物形式为______ 。
(1)写出下列物质在水溶液中的电离方程式:
①
 :
:②

③写出①②水溶液混合后恰好沉淀完全的离子方程式
(2)标准状况下,相同质量的
 和
和 物质的量比为
物质的量比为(3)某建筑材料主要成分为铝硅酸盐,化学式是
 ;改写成氧化物形式为
;改写成氧化物形式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】①SO3+H2O===H2SO4②Cl2+H2O===HCl+HClO ③2F2+2H2O===4HF+O2④2K+2H2O===2KOH+H2↑⑤CO2+2NaOH===Na2CO3+H2O
(1)上述反应中不属于氧化还原反应的有____ (填序号,下同);
(2)H2O只做氧化剂的是____ ,H2O只做还原剂的是____ ,
(3)属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是____ 。
(4)④的离子方程式_________________________ 。 ⑤的离子方程式_______________ 。
(1)上述反应中不属于氧化还原反应的有
(2)H2O只做氧化剂的是
(3)属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是
(4)④的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3、KOH五种物质,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号:

①相连的两种物质都是电解质的是___ (填分类标准代号,下同),都是氧化物的是___ 。
②图中相连的两种物质能够相互反应的是___ ,所属基本反应类型的是___ 反应。
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的离子方程式为___ 。
(2)分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼。如:
①CO2、SiO2、SO2、SO3都属于酸性氧化物,由CO2+Ca(OH)2=CaCO3↓+H2O,可完成SO3与NaOH反应的化学方程式为___ 。
②NaHCO3、NaHSO3、NaHS都属于弱酸形成的酸式盐,由NaHCO3+HCl=NaCl+H2O+CO2↑及NaHCO3+NaOH=Na2CO3+H2O,可完成NaHS分别与HCl、NaOH反应的化学方程式为___ 、___ 。
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3、KOH五种物质,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号:

①相连的两种物质都是电解质的是
②图中相连的两种物质能够相互反应的是
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的离子方程式为
(2)分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼。如:
①CO2、SiO2、SO2、SO3都属于酸性氧化物,由CO2+Ca(OH)2=CaCO3↓+H2O,可完成SO3与NaOH反应的化学方程式为
②NaHCO3、NaHSO3、NaHS都属于弱酸形成的酸式盐,由NaHCO3+HCl=NaCl+H2O+CO2↑及NaHCO3+NaOH=Na2CO3+H2O,可完成NaHS分别与HCl、NaOH反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硫铁化合物(FeS、FeS2等)应用广泛。在弱碱性溶液中,FeS与 反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为
反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为___________ 。
 反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为
反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Mg(OH)2和稀盐酸的反应:OH-+H+=H2O。( )
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下列反应的离子方程式不正确 的是_______ 。
A.(2020·北京市等级考)湿润的淀粉碘化钾试纸遇氯气变蓝:3Cl2+I-+3H2O=6Cl-+IO +6H+
+6H+
B. (2020·全国Ⅲ卷)向CaCl2溶液中通入CO2:Ca2++H2O+CO2=CaCO3↓+2H+
C. (2022·全国甲卷)硅酸钠溶液中通入二氧化碳:SiO +CO2+H2O=HSiO
+CO2+H2O=HSiO +HCO
+HCO
D. (2022·浙江6月选考)溴与冷的NaOH溶液反应:Br2+OH-=Br-+BrO-+H+
E. (2019年4月·浙江学考真题)硫酸铜溶液中加少量的铁粉:3Cu2++2Fe=2Fe3++3Cu
F. (2019·江苏高考)室温下用稀HNO3溶解铜:Cu+2NO +2H+=Cu2++2NO2↑+H2O
+2H+=Cu2++2NO2↑+H2O
G. (2018·浙江11月学考真题)Na与CuSO4水溶液反应:2Na+Cu2+=Cu+2Na+
H. (2017·海南高考)向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3CO =Al2(CO3)3↓
=Al2(CO3)3↓
J. (2016·天津高考)用碳酸氢钠溶液检验水杨酸中的羧基: +2HCO
+2HCO →
→ +2H2O+2CO2↑
+2H2O+2CO2↑
A.(2020·北京市等级考)湿润的淀粉碘化钾试纸遇氯气变蓝:3Cl2+I-+3H2O=6Cl-+IO
 +6H+
+6H+B. (2020·全国Ⅲ卷)向CaCl2溶液中通入CO2:Ca2++H2O+CO2=CaCO3↓+2H+
C. (2022·全国甲卷)硅酸钠溶液中通入二氧化碳:SiO
 +CO2+H2O=HSiO
+CO2+H2O=HSiO +HCO
+HCO
D. (2022·浙江6月选考)溴与冷的NaOH溶液反应:Br2+OH-=Br-+BrO-+H+
E. (2019年4月·浙江学考真题)硫酸铜溶液中加少量的铁粉:3Cu2++2Fe=2Fe3++3Cu
F. (2019·江苏高考)室温下用稀HNO3溶解铜:Cu+2NO
 +2H+=Cu2++2NO2↑+H2O
+2H+=Cu2++2NO2↑+H2OG. (2018·浙江11月学考真题)Na与CuSO4水溶液反应:2Na+Cu2+=Cu+2Na+
H. (2017·海南高考)向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3CO
 =Al2(CO3)3↓
=Al2(CO3)3↓J. (2016·天津高考)用碳酸氢钠溶液检验水杨酸中的羧基:
 +2HCO
+2HCO →
→ +2H2O+2CO2↑
+2H2O+2CO2↑
您最近一年使用:0次



