人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于胃酸 。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:

(1)试剂1可选择_______ 。
(2)加入试剂2为了验证 是否被氧化,试剂2选择
是否被氧化,试剂2选择_______ 。
(3)一般在服用“速力菲”时,同时服用维生素C,将不易吸收的 转化为
转化为 ,说明维生素C具有
,说明维生素C具有_______ 性。
(4)加入新制氯水,溶液中发生反应的离子方程式是_______ 。
(5)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色絮状沉淀
,溶液中白色絮状沉淀 更易被氧化,请写出
更易被氧化,请写出 在空气中被
在空气中被 氧化的化学方程式是
氧化的化学方程式是_______ ,沉淀转化过程的现象是_______ 。
 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:
(1)试剂1可选择
(2)加入试剂2为了验证
 是否被氧化,试剂2选择
是否被氧化,试剂2选择(3)一般在服用“速力菲”时,同时服用维生素C,将不易吸收的
 转化为
转化为 ,说明维生素C具有
,说明维生素C具有(4)加入新制氯水,溶液中发生反应的离子方程式是
(5)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色絮状沉淀
,溶液中白色絮状沉淀 更易被氧化,请写出
更易被氧化,请写出 在空气中被
在空气中被 氧化的化学方程式是
氧化的化学方程式是
更新时间:2023-01-07 19:30:56
|
相似题推荐
【推荐1】五氧化二钒广泛用于冶金、化工等行业,用作合金添加剂、生产硫酸或石油精炼用的催化剂等。从废钒催化剂中(含有K2SO4、V2O4、SiO2、Al2O3等)回收钒,既能避免对环境的污染,又能节约宝贵的资源。回收工艺流程如图所示:

已知:①“酸浸”时V2O4与稀硫酸反应生成VO2+;
②VO2+在有机溶剂中的溶解度大于水;
③溶液中VO 与VO
与VO 可相互转化:VO
可相互转化:VO +H2O
+H2O VO
VO +2H+,NH4VO3为沉淀。
+2H+,NH4VO3为沉淀。
(1)“滤渣1”的主要成分是____ (填名称)。
(2)已知K2SO4溶解度随温度的变化不明显,则“操作1”的名称是____ 。
(3)“氧化”过程中发生反应的离子方程式为____ 。
(4)“沉钒”时,通入氨气的作用是____ ,以沉钒率(NH4VO3沉淀中V的质量和废催化剂V的质量之比)表示该步反应钒的回收率(如图所示)。温度为80℃时沉钒率最高的原因是____ 。

(5)“煅烧”工艺中发生的化学反应方程式为____ 。
(6)已知将5.85 g NH4VO3固体进行热重分析,测得135℃时剩余固体质量为5.0 g,则该温度下剩余固体的化学式为____ 。

已知:①“酸浸”时V2O4与稀硫酸反应生成VO2+;
②VO2+在有机溶剂中的溶解度大于水;
③溶液中VO
 与VO
与VO 可相互转化:VO
可相互转化:VO +H2O
+H2O VO
VO +2H+,NH4VO3为沉淀。
+2H+,NH4VO3为沉淀。(1)“滤渣1”的主要成分是
(2)已知K2SO4溶解度随温度的变化不明显,则“操作1”的名称是
(3)“氧化”过程中发生反应的离子方程式为
(4)“沉钒”时,通入氨气的作用是

(5)“煅烧”工艺中发生的化学反应方程式为
(6)已知将5.85 g NH4VO3固体进行热重分析,测得135℃时剩余固体质量为5.0 g,则该温度下剩余固体的化学式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氮氧化合物和二氧化硫是引起雾霾重要物质,工业用多种方法来治理。某种综合处理含 废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
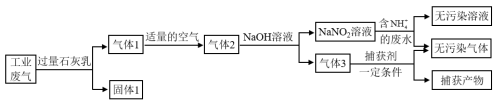
已知:NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)NO是___________ 色的气体,___________ (填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应,写出NO2与水反应的化学方程式为___________ 。
(2)SO2造成的一种常见的环境污染为___________ 。
(3)固体1的主要成分有Ca(OH)2、___________ 、___________ (填化学式)。
(4)验证废水中NH 已基本除净的方法是
已基本除净的方法是___________ (写出操作现象与结论)。
(5)捕获剂捕获的气体主要是___________ (填化学式)。
(6)流程中生成的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O,I2可以使淀粉溶液变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl固体。需选用的物质是___________ (填序号)。
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
 废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
已知:NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)NO是
(2)SO2造成的一种常见的环境污染为
(3)固体1的主要成分有Ca(OH)2、
(4)验证废水中NH
 已基本除净的方法是
已基本除净的方法是(5)捕获剂捕获的气体主要是
(6)流程中生成的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O,I2可以使淀粉溶液变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl固体。需选用的物质是
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】聚合硫酸铁铝(PFAS)是一种新型高效水处理剂。利用硫铁矿烧渣(主要成分为Fe3O4、FeO、SiO2等)为铁源,粉煤灰(主要成分为Al2O3、Fe2O3、FeO等)为铝源,制备PFAS的工艺流程如下: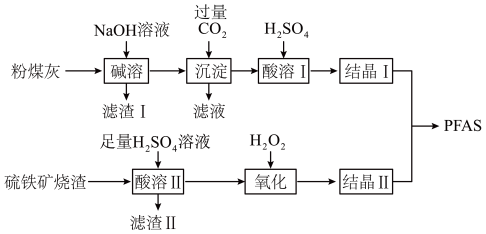
(1)“碱溶”时,粉煤灰发生反应的化学方程式为_____________________________
(2)“酸溶Ⅱ”时,Fe3O4发生反应的离子方程式为______________________________
(3)“滤渣Ⅰ”、“滤渣Ⅱ”在本流程中能加以利用的是__________________________
(4)“氧化”时应控制温度不超过57 ,其原因是
,其原因是_____________________________
(5)“氧化”时若用MnO2代替H2O2,发生反应的离子方程式是____________________

(1)“碱溶”时,粉煤灰发生反应的化学方程式为
(2)“酸溶Ⅱ”时,Fe3O4发生反应的离子方程式为
(3)“滤渣Ⅰ”、“滤渣Ⅱ”在本流程中能加以利用的是
(4)“氧化”时应控制温度不超过57
 ,其原因是
,其原因是(5)“氧化”时若用MnO2代替H2O2,发生反应的离子方程式是
您最近半年使用:0次
【推荐1】铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物,“速力菲”(主要成分为的琥珀酸亚铁,即丁二酸亚铁)是市场上一种常用的补铁药物,它难溶于水,但在人体胃酸的作用下可以释放出Fe2+,从而被人体吸收。
(1)某同学为了检验其中的Fe2+,将药物研磨、水溶后过滤。
①如图是某学生的过滤操作示意图,其操作不规范的是___ (填标号)
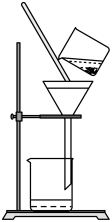
a.玻璃棒用作引流
b.漏斗末端颈尖未紧靠烧杯壁
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中搅动以加快过滤速度
②取少量所得滤液,分别加入 K3Fe(CN)6溶液(一种检验Fe2+的试剂)和KSCN溶液(一种检验Fe3+的试剂),均未出现明显现象。其主要原因是___ 。
(2)取酸性环境下“速力菲”溶解过滤后的滤液敞口放置在空气中一段时间,然后滴入KSCN溶液,溶液立即呈现血红色说明有Fe3+生成,说明Fe2+___ 。
(3)医生通常会建议:与维生素C同时服用,能增强“速力菲”的补铁效果。此举是利用了维生素C的___ 。(填“氧化性”、“还原性”或“碱性”)
(1)某同学为了检验其中的Fe2+,将药物研磨、水溶后过滤。
①如图是某学生的过滤操作示意图,其操作不规范的是

a.玻璃棒用作引流
b.漏斗末端颈尖未紧靠烧杯壁
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中搅动以加快过滤速度
②取少量所得滤液,分别加入 K3Fe(CN)6溶液(一种检验Fe2+的试剂)和KSCN溶液(一种检验Fe3+的试剂),均未出现明显现象。其主要原因是
(2)取酸性环境下“速力菲”溶解过滤后的滤液敞口放置在空气中一段时间,然后滴入KSCN溶液,溶液立即呈现血红色说明有Fe3+生成,说明Fe2+
(3)医生通常会建议:与维生素C同时服用,能增强“速力菲”的补铁效果。此举是利用了维生素C的
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下列框图中的物质均为中学化学中常见物质,其中甲、乙为单质,其余均为化合物,B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色。

请问答下列问题:
(1)A是____________ ,G是______________ 。(填化学式)
(2)反应①-⑤中,属于氧化还原反应的是________________ (填序号)。
(3)反应⑤的化学方程式为_________________________ 。
甲与B反应的离子方程式___________________________ 。
(4)在实验室将C溶液滴入F溶液中,观察到的现象是___________________ 。
(5)在F溶液中加入等物质的量的A,发生反应的总的离子方程式:____________________ 。
(6)已知:酚酞在c(OH-) 为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色。向3.9g A和 100g B混合后的溶液中滴入2滴酚酞试液,溶液变红色,片刻红色褪去。(假设过程中液体体积不变)①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的。
上述观点是否正确_____________ ,请通过计算对比数据加以说明_____________________ 。
②乙同学认为“红色迅速褪去”是由于A + B = 碱 + H2O2 ,H2O2具有氧化性和漂白性导致的。试设计简单实验证明烧瓶内溶液中含H2O2,简述实验原理_____________________________ 。

请问答下列问题:
(1)A是
(2)反应①-⑤中,属于氧化还原反应的是
(3)反应⑤的化学方程式为
甲与B反应的离子方程式
(4)在实验室将C溶液滴入F溶液中,观察到的现象是
(5)在F溶液中加入等物质的量的A,发生反应的总的离子方程式:
(6)已知:酚酞在c(OH-) 为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色。向3.9g A和 100g B混合后的溶液中滴入2滴酚酞试液,溶液变红色,片刻红色褪去。(假设过程中液体体积不变)①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的。
上述观点是否正确
②乙同学认为“红色迅速褪去”是由于A + B = 碱 + H2O2 ,H2O2具有氧化性和漂白性导致的。试设计简单实验证明烧瓶内溶液中含H2O2,简述实验原理
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】铜和三氧化二铁在工农业生产中用途广泛。用黄铜矿(主要成分为 ,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
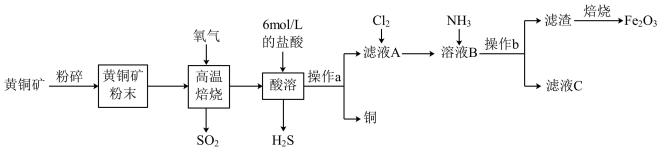
回答下列问题:
(1)将黄铜矿粉碎的目的是_______ 。
(2)高温焙烧时发生的反应是 ,焙烧过程
,焙烧过程_______ 元素被氧化,1mol  参加反应时,反应中转移电子
参加反应时,反应中转移电子_______ mol。
(3)向滤液A中通入 的目的是
的目的是_______ 。
(4) 的电子式为
的电子式为_______ ,向溶液B中通入 后发生反应的离子方程式为
后发生反应的离子方程式为_______ 。
(5)工业上用生物法处理 的原理为:(硫杆菌作催化剂)
的原理为:(硫杆菌作催化剂)

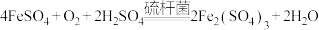
由图甲和图乙判断使用硫杆菌的最佳条件为_______ 。若反应温度过高,反应速率下降,其原因是_______ 。

 ,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
回答下列问题:
(1)将黄铜矿粉碎的目的是
(2)高温焙烧时发生的反应是
 ,焙烧过程
,焙烧过程 参加反应时,反应中转移电子
参加反应时,反应中转移电子(3)向滤液A中通入
 的目的是
的目的是(4)
 的电子式为
的电子式为 后发生反应的离子方程式为
后发生反应的离子方程式为(5)工业上用生物法处理
 的原理为:(硫杆菌作催化剂)
的原理为:(硫杆菌作催化剂)
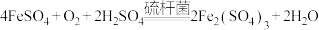
由图甲和图乙判断使用硫杆菌的最佳条件为

您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加_________ ,该过程的现象为:_____________ 。
(2)步骤②加入过量H2O2的目的:____________ 。
(3)步骤③中反应的离子方程式:____________ 。
(4)步骤④中一系列处理的操作步骤:过滤、_________ 、灼烧、_________ 、称量。
(5)若实验无损耗,则每片补血剂含铁元素的质量_________ g。
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+=5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需___________ 。
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是_________ 。
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
③滴定到终点时的溶液颜色为_________ 色。

请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加
(2)步骤②加入过量H2O2的目的:
(3)步骤③中反应的离子方程式:
(4)步骤④中一系列处理的操作步骤:过滤、
(5)若实验无损耗,则每片补血剂含铁元素的质量
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+=5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
③滴定到终点时的溶液颜色为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾[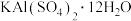 ]有如下两条途径。
]有如下两条途径。
途径I
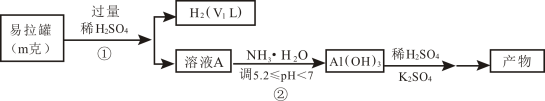
途径II
回答下列问题:
(1)Al元素在周期表中的位置为_______ 。
(2)溶液A中的金属离子有_______ 、_______ 、 。
。
(3)过程②生成 的离子方程式为
的离子方程式为_______ 。
(4)过程③发生反应的离子方程式为_______ 。
(5)下列关于产物的说法中,错误的是_______ (填标号)。
A.用KSCN溶液可以检验产物中是否含有
B.向明矾中加入 ,发生反应的离子方程式为
,发生反应的离子方程式为
C.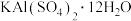 属于混合物
属于混合物
(6)途径II与途径I比较,优点有_______ (写出一点即可)。
(7)若V1与V2之差为2.24L(已折算成标准状况),则m克易拉罐样品中含Fe_______ g。
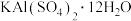 ]有如下两条途径。
]有如下两条途径。途径I

途径II

回答下列问题:
(1)Al元素在周期表中的位置为
(2)溶液A中的金属离子有
 。
。(3)过程②生成
 的离子方程式为
的离子方程式为(4)过程③发生反应的离子方程式为
(5)下列关于产物的说法中,错误的是
A.用KSCN溶液可以检验产物中是否含有

B.向明矾中加入
 ,发生反应的离子方程式为
,发生反应的离子方程式为
C.
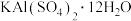 属于混合物
属于混合物(6)途径II与途径I比较,优点有
(7)若V1与V2之差为2.24L(已折算成标准状况),则m克易拉罐样品中含Fe
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】I.无水 可用作有机合成的催化剂、食品膨松剂等。工业上可由铝土矿(主要成分是
可用作有机合成的催化剂、食品膨松剂等。工业上可由铝土矿(主要成分是 和
和 )和焦炭制备,流程如下:
)和焦炭制备,流程如下:

已知: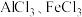 分别在
分别在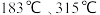 时升华,完成下列填空:
时升华,完成下列填空:
(1)氯化炉中 和焦炭在高温下发生反应的化学方程式为
和焦炭在高温下发生反应的化学方程式为___________ 。
(2)升华器中主要含有 和
和 ,需加入少量
,需加入少量 ,其作用是
,其作用是___________ 。
(3) 时,升华器中物质经充分反应后需降温实现
时,升华器中物质经充分反应后需降温实现 和
和 的分离。请选择合适的温度范围
的分离。请选择合适的温度范围___________ 。
a.低于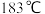 b.介于
b.介于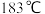 和
和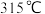 之间 c.高于
之间 c.高于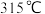
(4)欲证明 样品含有
样品含有 ,可采用的方法是
,可采用的方法是___________ 。
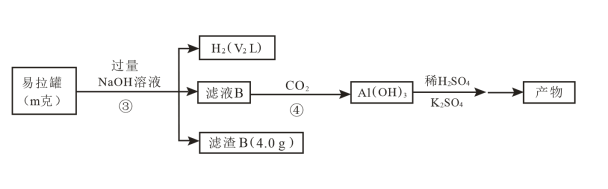
II.样品(含少量 )中
)中 含量可通过下列操作测得(部分物质略去)
含量可通过下列操作测得(部分物质略去)

(5)加入过量氢氧化钠涉及的离子方程式为___________ 。
(6)计算该样品中 的质量分数
的质量分数___________ (结果用m、n表示,不必化简)。
(7)取纯化后 配成溶液,向
配成溶液,向 的
的 溶液中滴加
溶液中滴加 的
的 溶液
溶液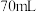 时,生成沉淀
时,生成沉淀___________ g。
 可用作有机合成的催化剂、食品膨松剂等。工业上可由铝土矿(主要成分是
可用作有机合成的催化剂、食品膨松剂等。工业上可由铝土矿(主要成分是 和
和 )和焦炭制备,流程如下:
)和焦炭制备,流程如下:
已知:
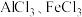 分别在
分别在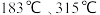 时升华,完成下列填空:
时升华,完成下列填空:(1)氯化炉中
 和焦炭在高温下发生反应的化学方程式为
和焦炭在高温下发生反应的化学方程式为(2)升华器中主要含有
 和
和 ,需加入少量
,需加入少量 ,其作用是
,其作用是(3)
 时,升华器中物质经充分反应后需降温实现
时,升华器中物质经充分反应后需降温实现 和
和 的分离。请选择合适的温度范围
的分离。请选择合适的温度范围a.低于
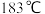 b.介于
b.介于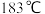 和
和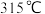 之间 c.高于
之间 c.高于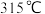
(4)欲证明
 样品含有
样品含有 ,可采用的方法是
,可采用的方法是II.样品(含少量
 )中
)中 含量可通过下列操作测得(部分物质略去)
含量可通过下列操作测得(部分物质略去)
(5)加入过量氢氧化钠涉及的离子方程式为
(6)计算该样品中
 的质量分数
的质量分数(7)取纯化后
 配成溶液,向
配成溶液,向 的
的 溶液中滴加
溶液中滴加 的
的 溶液
溶液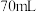 时,生成沉淀
时,生成沉淀
您最近半年使用:0次



