元素周期表揭示了化学元素间的内在联系,部分元素在周期表中的位置如图:
(1)属于第二周期且无正价的元素是_____ (填元素符号,下同),属于第ⅤA族的是_____ ,化学性质最稳定的元素是_____ 。
(2)H的最高价氧化物与L的最高价氧化物对应水化物反应的离子方程式为:_____ 。
(3)B与J形成原子个数比为1∶1的化合物,该化合物的电子式为:______ ,含有共价键的类型为:_____ ;用电子式表示N与K形成离子化合物的过程_____ 。
(4)A、G、F气态氢化物稳定性由强至弱的顺序:_____ (用对应的化学式表示);B、I、F、K、N对应的简单离子的半径由大到小的顺序:_____ (用对应的离子符号表示)。
| 周期 | ||||||||||||||||||
| 1 | ||||||||||||||||||
| 2 | D | B | A | |||||||||||||||
| 3 | J | I | H | C | G | F | E | |||||||||||
| 4 | L | K | N | |||||||||||||||
| 5 | M | |||||||||||||||||
| 6 | ||||||||||||||||||
(2)H的最高价氧化物与L的最高价氧化物对应水化物反应的离子方程式为:
(3)B与J形成原子个数比为1∶1的化合物,该化合物的电子式为:
(4)A、G、F气态氢化物稳定性由强至弱的顺序:
更新时间:2023-01-10 22:29:07
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表列出了①~⑦共7种元素在元素周期表中的位置。
回答下列问题:
(1)①可以形成原子空间排列方式不同的多种单质,这些不同的单质之间互称为_______ 。
(2)②形成的单质的电子式为_______ 。
(3)⑤的单质在工业上常用于冶炼熔点较高的金属,如用MnO2冶炼Mn,该反应的化学方程式为______ 。
(4)③⑤⑦三种元素的简单离子半径由大到小的顺序是_______ (填离子符号)。
(5)④的单质在③的单质中燃烧形成的化学键有_______ 、_______ 。
族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ |
(1)①可以形成原子空间排列方式不同的多种单质,这些不同的单质之间互称为
(2)②形成的单质的电子式为
(3)⑤的单质在工业上常用于冶炼熔点较高的金属,如用MnO2冶炼Mn,该反应的化学方程式为
(4)③⑤⑦三种元素的简单离子半径由大到小的顺序是
(5)④的单质在③的单质中燃烧形成的化学键有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表为元素周期表的粗表,①~⑧分别表示元素周期表中对应位置的元素
(1)用电子式表示①与②形成化合物A 的过程:________
(2)已知⑥原子的最外层有2个电子,请画出⑥原子的结构示意图:______________
(3)含有④元素的某种18 电子的离子与H+及OH-均可发生反应,请写出该离子的电子式______
(4)元素③④⑤的简单气态氢化物的稳定性由强到弱的顺序是_________ (用化学式表示),其沸点由高到低的顺序是_______ (用化学式表示)
(5)已知⑦的稳定化合态为+2 价,且⑦与③可按3:4 形成某化合物,该化合物具有较强氧化性, 可以与浓盐酸反应并释放出一种黄绿色的气体, 请写出该化学方程式:_________________
(6)①与③,①与④能形成18个电子的化合物,此两种化合物在溶液中发生反应的化学方程式为_________ 。
(7)⑧的一种氧化物为无色气体,在空气中能迅速变成红棕色。在一定条件下,2L的该无色气体与0.5 L 的氧气混合,该混合气体被足量的NaOH溶液完全吸收后没有气体残留,则所生成的一种含氧酸盐的化学式是_________ 。
(8)两种均含①与②③④四种元素的化合物相互反应放出气体的离子方程式为_________ 。
| ① | |||||||||||||||||
| ⑧ | ③ | ⑤ | |||||||||||||||
| ② | ④ | ||||||||||||||||
| ⑥ | |||||||||||||||||
| ⑦ | |||||||||||||||||
(1)用电子式表示①与②形成化合物A 的过程:
(2)已知⑥原子的最外层有2个电子,请画出⑥原子的结构示意图:
(3)含有④元素的某种18 电子的离子与H+及OH-均可发生反应,请写出该离子的电子式
(4)元素③④⑤的简单气态氢化物的稳定性由强到弱的顺序是
(5)已知⑦的稳定化合态为+2 价,且⑦与③可按3:4 形成某化合物,该化合物具有较强氧化性, 可以与浓盐酸反应并释放出一种黄绿色的气体, 请写出该化学方程式:
(6)①与③,①与④能形成18个电子的化合物,此两种化合物在溶液中发生反应的化学方程式为
(7)⑧的一种氧化物为无色气体,在空气中能迅速变成红棕色。在一定条件下,2L的该无色气体与0.5 L 的氧气混合,该混合气体被足量的NaOH溶液完全吸收后没有气体残留,则所生成的一种含氧酸盐的化学式是
(8)两种均含①与②③④四种元素的化合物相互反应放出气体的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分,根据表中给出的①—⑥六种元素,回答下列问题:
(1)画出元素④的原子结构示意图__________ ;
(2)元素①形成的最简单有机物的化学式是__________ ;
(3)表中所列元素中非金属性最强的元素是__________ (填元素符号)
(4)元素⑤形成的最高价氧化物对应的水化物的化学式是__________ ;
(5)元素③和元素⑥形成的化合物的电子式是__________ 。
族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ |
(2)元素①形成的最简单有机物的化学式是
(3)表中所列元素中非金属性最强的元素是
(4)元素⑤形成的最高价氧化物对应的水化物的化学式是
(5)元素③和元素⑥形成的化合物的电子式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素A、B、C、D、E原子序数依次增大;A与B可形成4核10电子的分子;C、E同主族,D、E同周期;C和D可形成离子化合物D2C,D2C中阴阳离子的电子层结构相同,且电子总数为30。
请回答下列问题 用元素符号表示
用元素符号表示 :
:
(1)元素A的一种同位素质子数与中子数相等,这种同位素的符号是______ 。
(2)元素B在周期表中的位置是______ 。
(3)元素A与B形成10电子的分子,其水溶液呈碱性,用电离方程式表示______ 。
(4)元素A、B、C形成的原子个数比为4:2:3的盐,属于______  填“离子“或“共价“
填“离子“或“共价“ 化合物,含有的化学键类型为
化合物,含有的化学键类型为______ 。
(5)元素C、D形成化合物D2C2的电子式为______ ,其与水反应的离子方程式为______ 。
(6)元素C、D、E、F形成简单离子的半径由小到大的顺序为______ 。
(7)元素E与F相比,元素原子得电子能力较强的是______ ,用离子方程式证明______ 。
请回答下列问题
 用元素符号表示
用元素符号表示 :
:(1)元素A的一种同位素质子数与中子数相等,这种同位素的符号是
(2)元素B在周期表中的位置是
(3)元素A与B形成10电子的分子,其水溶液呈碱性,用电离方程式表示
(4)元素A、B、C形成的原子个数比为4:2:3的盐,属于
 填“离子“或“共价“
填“离子“或“共价“ 化合物,含有的化学键类型为
化合物,含有的化学键类型为(5)元素C、D形成化合物D2C2的电子式为
(6)元素C、D、E、F形成简单离子的半径由小到大的顺序为
(7)元素E与F相比,元素原子得电子能力较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
(1)在⑤~⑧元素中,原子半径最大的是______ (填元素符号,下同),非金属性最强的元素是______
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有______ 。
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:______ 。
(4)③、⑤、⑧所形成的离子,其半径由小到大的顺序是______ (填离子符号)。
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是______ (填物质化学式);呈两性的氢氧化物是______ (填物质化学式),该化合物与NaOH溶液反应的离子方程式为______ 。
(6)表中元素⑦和氢元素可形成一种相对分子质量为32的化合物Y,⑧与氢元素按原子个数比1:1形成的化合物X,X与Y发生氧化还原反应,生成⑦单质和⑧的另一种氢化物,写出该反应的化学方程式______ 。
(7)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
①由镓的性质推知,镓与铝同主族,且位于铝的下一周期。试从原子结构的角度解释镓与铝性质相似的原因______ 。冶炼金属镓通常采用的方法是______ 。
②为判断Ga(OH)3是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、______ 和______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:
(4)③、⑤、⑧所形成的离子,其半径由小到大的顺序是
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(6)表中元素⑦和氢元素可形成一种相对分子质量为32的化合物Y,⑧与氢元素按原子个数比1:1形成的化合物X,X与Y发生氧化还原反应,生成⑦单质和⑧的另一种氢化物,写出该反应的化学方程式
(7)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
①由镓的性质推知,镓与铝同主族,且位于铝的下一周期。试从原子结构的角度解释镓与铝性质相似的原因
②为判断Ga(OH)3是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大,其中B与C同周期,D与E、F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,E为地壳中含量最高的金属元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。回答下列问题:
(1)元素E在元素周期表中的位置是___________ 。
(2)B.C、D三种元素的简单离子半径由大到小的顺序是___________ (填离子符号)。
(3)化合物DCA的俗称为___________ ,单质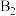 在工业上的用途为
在工业上的用途为___________ 。
(4)化合物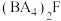 的摩尔质量为
的摩尔质量为___________ ,非金属性:C___________ F(填“>”、“<”)。
(5)少量的 与D的最高价氧化物对应的水化物可发生反应,生成物仅为
与D的最高价氧化物对应的水化物可发生反应,生成物仅为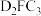 和
和 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(1)元素E在元素周期表中的位置是
(2)B.C、D三种元素的简单离子半径由大到小的顺序是
(3)化合物DCA的俗称为
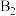 在工业上的用途为
在工业上的用途为(4)化合物
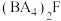 的摩尔质量为
的摩尔质量为(5)少量的
 与D的最高价氧化物对应的水化物可发生反应,生成物仅为
与D的最高价氧化物对应的水化物可发生反应,生成物仅为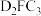 和
和 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
【推荐1】有位于前四周期的A、B、C、D、E、F、G七种元素(无稀有气体),它们的核电荷数依次增大。其中C、F、G是金属元素:A和F属同族,它们原子的最外层电子排布式为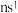 。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。G元素原子共有3个价电子,其中一个价电子位于第三能层d轨道。请回答下列问题:
。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。G元素原子共有3个价电子,其中一个价电子位于第三能层d轨道。请回答下列问题:
(1)G是___________ (用元素符号回答,下同),其最高化合价为___________ 。
(2)元素E的电子所占据的最高能级的原子轨道呈___________ 形。D、E可分别与A形成的最简分子,前者的稳定性弱于后者,从化学键的角度解释的原因是___________ ;
(3)B、C、D、F的简单离子半径由大到小的顺序为:___________ 。
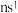 。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。G元素原子共有3个价电子,其中一个价电子位于第三能层d轨道。请回答下列问题:
。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。G元素原子共有3个价电子,其中一个价电子位于第三能层d轨道。请回答下列问题:(1)G是
(2)元素E的电子所占据的最高能级的原子轨道呈
(3)B、C、D、F的简单离子半径由大到小的顺序为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】随原子序数递增,八种短周期元素(用字母 x 等表示),原子半径的相对大小、最高正价或最低负价的变化如下图所示:
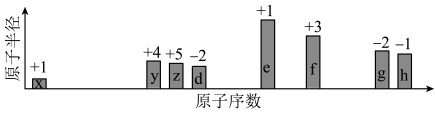
根据判断出的元素回答问题:
(1)g 在周期表中的位置是__________ .
(2)d、e、h 的简单离子半径由大到小顺序:_____________ (用离子符号表示).
(3)有关 y、z、d 三种元素的说法正确的是__________ (填序号).
①最高正价:d>z>y ②简单气态氢化物的稳定性:d>z>y
③非金属性:d>z>y ④单质活泼性:y>z>d
(4)根据g 和h 两种元素填空:
①最高正价氧化物对应水化物的酸性由强到弱的顺序是____________ .(用化学式表示)
②g2h2 分子中原子都满足 8 电子结构,试写出其电子式____________ .
(5)①试写出x、d、e 形成化合物的水溶液与单质f 反应的化学方程式________________ .
②已知化合物A、B 均由 x、d、e、g 四种元素组成,试写出A 和B 反应的离子方程式________________ 。

根据判断出的元素回答问题:
(1)g 在周期表中的位置是
(2)d、e、h 的简单离子半径由大到小顺序:
(3)有关 y、z、d 三种元素的说法正确的是
①最高正价:d>z>y ②简单气态氢化物的稳定性:d>z>y
③非金属性:d>z>y ④单质活泼性:y>z>d
(4)根据g 和h 两种元素填空:
①最高正价氧化物对应水化物的酸性由强到弱的顺序是
②g2h2 分子中原子都满足 8 电子结构,试写出其电子式
(5)①试写出x、d、e 形成化合物的水溶液与单质f 反应的化学方程式
②已知化合物A、B 均由 x、d、e、g 四种元素组成,试写出A 和B 反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,表中所列的每个字母分别代表某一元素。

回答下列问题:
(1)元素d的原子结构示意图为_______ ,a、b、e、g简单离子半径的大小顺序_______ (用离子符号表示)。
(2)化合物cd2的电子式为_______ ,化合物a2d2中含有的化学键为_______ 。
(3)由元素h、i组成的化合物砷化镓(GaAs)是一种重要的半导体材料,其中元素h、i中失电子能力更强的是_______ (填元素符号)。元素i与f的最高价氧化物水化物的酸性更强的是_______ (填化合物化学式,下同),元素i与f的简单气态氢化物还原性更强的是_______ 。
(4)设计实验证明g的得电子能力大于j,简述操作步骤和现象(可选用试剂:固体KMnO4、稀盐酸、浓盐酸、溴水、NaBr溶液、CCl4溶液):_______ 。

回答下列问题:
(1)元素d的原子结构示意图为
(2)化合物cd2的电子式为
(3)由元素h、i组成的化合物砷化镓(GaAs)是一种重要的半导体材料,其中元素h、i中失电子能力更强的是
(4)设计实验证明g的得电子能力大于j,简述操作步骤和现象(可选用试剂:固体KMnO4、稀盐酸、浓盐酸、溴水、NaBr溶液、CCl4溶液):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】元素在周期表中的位置,反映了元素的原子结构和性质。下图是元素周期表的一部分。请按要求回答下列问题。
(1)④⑥两种元素形成的化合物可用作防腐剂,常用于腌制食物,该化合物的电子式是_______ ,高温灼烧该化合物时,火焰呈_______ 色;
(2)①②③三种元素中,原子半径最小的是_______ (填元素符号);
(3)④⑦两种元素最高价氧化物对应的水化物碱性较强的是_______ (填化学式);
(4)①⑥两种元素的简单氢化物相遇会迅速反应,产生大量白烟,写出该反应的化学方程式是_______ 。
| He | |||||||||||||||||
| ① | ② | ③ | Ne | ||||||||||||||
| ④ | ⑤ | ⑥ | Ar | ||||||||||||||
| ⑦ | Kr |
(2)①②③三种元素中,原子半径最小的是
(3)④⑦两种元素最高价氧化物对应的水化物碱性较强的是
(4)①⑥两种元素的简单氢化物相遇会迅速反应,产生大量白烟,写出该反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有5种短周期元素的原子序数按E、D、B、A、C 的顺序依次增大; A、C 同周期,B、C同主族;A 与B 可形成离子化合物A2B,A2B 中阴阳离子的电子层结构完全相同,且电子总数为30;D 和E可形成4 核10 电子的分子。试回答下列问题:
(1)写出这5种元素的名称: A______ B______ C______ D______ E______
(2)写出下列物质的电子式:
①D 元素形成的单质___________ ②B 与E 形成的四原子化合物________
③A.B、E 形成的化合物__________ ④D、E 形成的简单化合物__________
(3)B、D、E形成的原子个数3:2:4的盐的化学式为_______ ,类别属于______ 化合物(填离子或共价),含有的化学键类型__________ 。
(1)写出这5种元素的名称: A
(2)写出下列物质的电子式:
①D 元素形成的单质
③A.B、E 形成的化合物
(3)B、D、E形成的原子个数3:2:4的盐的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】1962年首个稀有气体化合物XePtF6问世,目前已知的稀有气体化合物中,含氙(54Xe)的最多,氪(36Kr)次之,氩(18Ar)化合物极少。[BrOF2][AsF6]•xKrF2是[BrOF2]+、[AsF6]-与KrF2分子形成的加合物,回答下列问题:
(1)As元素原子序数为33,在周期表中的位置是_______ 。As原子的价电子排布式为_______ 。与磷酸相比,最高价氧化物的水化物酸性强弱的顺序是:_______ 。
(2)Ar、Kr、Xe原子半径大小顺序为_______ 。Ar、Kr、Xe原子的活泼性依序增强,原因是________ 。
(3)晶体熔点:KrF2_______ XeF2(填“>”“<”或“=”),判断依据是______________ 。
(4)试猜想:[BrOF2][AsF6]•xKrF2晶体中的化学键类型有_______ 。
(1)As元素原子序数为33,在周期表中的位置是
(2)Ar、Kr、Xe原子半径大小顺序为
(3)晶体熔点:KrF2
(4)试猜想:[BrOF2][AsF6]•xKrF2晶体中的化学键类型有
您最近一年使用:0次



