下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
(1)在⑤~⑧元素中,原子半径最大的是______ (填元素符号,下同),非金属性最强的元素是______
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有______ 。
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:______ 。
(4)③、⑤、⑧所形成的离子,其半径由小到大的顺序是______ (填离子符号)。
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是______ (填物质化学式);呈两性的氢氧化物是______ (填物质化学式),该化合物与NaOH溶液反应的离子方程式为______ 。
(6)表中元素⑦和氢元素可形成一种相对分子质量为32的化合物Y,⑧与氢元素按原子个数比1:1形成的化合物X,X与Y发生氧化还原反应,生成⑦单质和⑧的另一种氢化物,写出该反应的化学方程式______ 。
(7)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
①由镓的性质推知,镓与铝同主族,且位于铝的下一周期。试从原子结构的角度解释镓与铝性质相似的原因______ 。冶炼金属镓通常采用的方法是______ 。
②为判断Ga(OH)3是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、______ 和______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:
(4)③、⑤、⑧所形成的离子,其半径由小到大的顺序是
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(6)表中元素⑦和氢元素可形成一种相对分子质量为32的化合物Y,⑧与氢元素按原子个数比1:1形成的化合物X,X与Y发生氧化还原反应,生成⑦单质和⑧的另一种氢化物,写出该反应的化学方程式
(7)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
①由镓的性质推知,镓与铝同主族,且位于铝的下一周期。试从原子结构的角度解释镓与铝性质相似的原因
②为判断Ga(OH)3是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、
更新时间:2021-03-10 19:47:17
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】周期表中ⅡA族镁、铍及其及其化合物应用广泛。
I.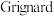 试剂(
试剂(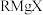 )是有机合成中的重要试剂之一,一种合成应用机理为:
)是有机合成中的重要试剂之一,一种合成应用机理为: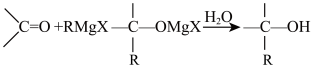 ,回答以下问题:
,回答以下问题:
(1) 中镁元素的化合价为
中镁元素的化合价为___________ ,丙酮(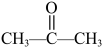 )与
)与 发生上述反应所得醇的结构简式为
发生上述反应所得醇的结构简式为___________ 。
(2) 易发生水解反应,生成甲烷、一种碱和一种镁盐。试写出该反应的化学方程式:
易发生水解反应,生成甲烷、一种碱和一种镁盐。试写出该反应的化学方程式:___________ 。
Ⅱ.铍是比热容最高的结构材料,常用来制作航天航空部件。以绿柱石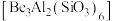 为原料制备金属铍的工艺如下:
为原料制备金属铍的工艺如下:
已知: 与
与 性质相似,强碱溶液中会转化为
性质相似,强碱溶液中会转化为 。
。
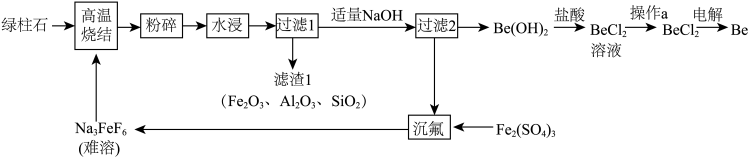
回答下列问题:
(3)烧结冷却后,粉碎的目的是___________ 。
(4)流程中沉铍加 不能过量,用化学方程式表示原因
不能过量,用化学方程式表示原因___________ 。往滤渣1中加强碱,分离回收铝元素的离子方程式为___________ 。
(5)操作 是
是___________ 。
(6)“水浸”后铍元素以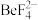 形式存在。“过滤2”得滤液“沉氟”的离子方程式为
形式存在。“过滤2”得滤液“沉氟”的离子方程式为___________ 。
I.
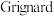 试剂(
试剂(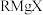 )是有机合成中的重要试剂之一,一种合成应用机理为:
)是有机合成中的重要试剂之一,一种合成应用机理为: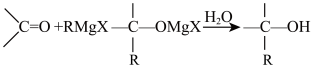 ,回答以下问题:
,回答以下问题:(1)
 中镁元素的化合价为
中镁元素的化合价为 )与
)与 发生上述反应所得醇的结构简式为
发生上述反应所得醇的结构简式为(2)
 易发生水解反应,生成甲烷、一种碱和一种镁盐。试写出该反应的化学方程式:
易发生水解反应,生成甲烷、一种碱和一种镁盐。试写出该反应的化学方程式:Ⅱ.铍是比热容最高的结构材料,常用来制作航天航空部件。以绿柱石
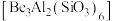 为原料制备金属铍的工艺如下:
为原料制备金属铍的工艺如下:已知:
 与
与 性质相似,强碱溶液中会转化为
性质相似,强碱溶液中会转化为 。
。
回答下列问题:
(3)烧结冷却后,粉碎的目的是
(4)流程中沉铍加
 不能过量,用化学方程式表示原因
不能过量,用化学方程式表示原因(5)操作
 是
是(6)“水浸”后铍元素以
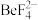 形式存在。“过滤2”得滤液“沉氟”的离子方程式为
形式存在。“过滤2”得滤液“沉氟”的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】硼镁泥是硼镁矿(2MgO·B2O3)生产硼砂(Na2B4O7·10H2O)时的废渣,其主要成分是MgCO3,还含有其它杂质(MgO、SiO2、Fe2O3、FeO、B2O3、Al2O3、MnO等)。硼镁泥制取七水硫酸镁的工艺流程如下:
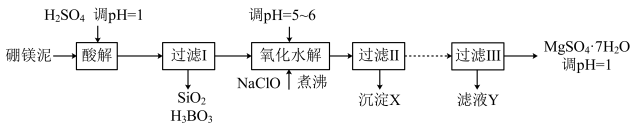
部分阳离子以氢氧化物形式完全沉淀时溶液的pH
(1)将硼镁矿粉碎后加水和纯碱,在加热加压下通入CO2可得硼砂。试写出反应方程式_________ 。
(2)已知硼酸(H3BO3)结构和性质与Al(OH)3相似,则硼酸与NaOH溶液反应的化学方程式为________ 。
(3)沉淀X中除了有Al(OH)3、Fe(OH)3外,还含有二氧化锰,用离子方程式解释原因为_________ 。
(4)过滤Ⅱ和过滤Ⅲ之间省略的操作步骤为__________ 。滤液Y中阴离子除了SO 外主要还含有
外主要还含有_______ ,其检验试剂为__________ 。

部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
(2)已知硼酸(H3BO3)结构和性质与Al(OH)3相似,则硼酸与NaOH溶液反应的化学方程式为
(3)沉淀X中除了有Al(OH)3、Fe(OH)3外,还含有二氧化锰,用离子方程式解释原因为
(4)过滤Ⅱ和过滤Ⅲ之间省略的操作步骤为
 外主要还含有
外主要还含有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下列物质A-F是我们熟悉的单质或化合物,其中A、B均是常见的金属,且B的合金用量最大;E在常温下是黄绿色气体;适当的条件下,它们之间可以发生如图所示的转化。
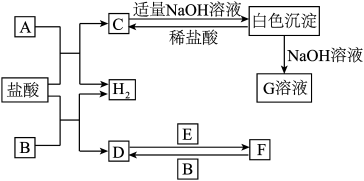
(1)A的原子结构示意图___ ;G溶液中溶质的化学式为___ 。
(2)请写出反应D→F的化学方程式:___ 。
(3)检验F中金属阳离子的常用试剂是___ (填物质的化学式);现象是___ 。
(4)E物质可与石灰乳反应制取漂白粉,写出漂白粉的有效成分___ 。
(5)写出C与足量氢氧化钠溶液反应的离子方程式___ 。
(6)FeCl3溶液和氢氧化铁胶体的本质区别是___ 。

(1)A的原子结构示意图
(2)请写出反应D→F的化学方程式:
(3)检验F中金属阳离子的常用试剂是
(4)E物质可与石灰乳反应制取漂白粉,写出漂白粉的有效成分
(5)写出C与足量氢氧化钠溶液反应的离子方程式
(6)FeCl3溶液和氢氧化铁胶体的本质区别是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。

请写下列空白:
(1)A与B形成 的电子式为
的电子式为_______ ;C的原子结构示意图为_______ 。
(2)B的最高价氧化物对应的水化物的化学式为_______ ;D、E的最高价氧化物对应的水化物中碱性较弱的是_______ (用化学式表示);元素C、D、E的原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)E位于周期表的第三周期第_______ 族;和F相邻的最外层电子数等于周期数的元素的氧化物与氢氧化钠溶液反应的离子方程式为_______ 。

请写下列空白:
(1)A与B形成
 的电子式为
的电子式为(2)B的最高价氧化物对应的水化物的化学式为
(3)E位于周期表的第三周期第
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图是元素周期表的一部分,根据①~⑨在周期表中的位置按题目要求回答:
(1)在元素①~⑨中,金属性最强的元素是______ (填元素符号)。
(2)画出元素④的原子结构示意图______ 。
(3)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,写出甲物质的电子式______ ,其化学键类型为______ 共价键(填“极性”或“非极性”)。
(4)元素③⑤对应的最高价氧化物的水化物,写出它们相互之间能发生反应的离子方程式______ 。
(5)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程______ 。
(6)②与⑥形成两种气态氢化物中,稳定性较高的是______ (填化学式),请从原子结构的角度解释其原因:______ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 4 | ⑧ | ⑨ | ||||||
(2)画出元素④的原子结构示意图
(3)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,写出甲物质的电子式
(4)元素③⑤对应的最高价氧化物的水化物,写出它们相互之间能发生反应的离子方程式
(5)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程
(6)②与⑥形成两种气态氢化物中,稳定性较高的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】表为元素周期表的一部分,请回答有关问题:
(1)⑤和⑨的元素符号是___ 和___ 。
(2)表中非金属性最强的元素是___ (填写元素名称)。
(3)④、⑤、⑥三种元素的氧化物对应的水化物中碱性最强的是___ (填化学式)。
(4)⑥、⑦、②三种元素原子半径由大到小的顺序是___>___>___(用元素符号填写)。__
(5)①与②形成能产生温室效应的气体的电子式:___ 。
(6)请设计一个实验方案,比较⑧、⑩单质氧化性的强弱:__ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 四 | ⑨ | ⑩ |
(2)表中非金属性最强的元素是
(3)④、⑤、⑥三种元素的氧化物对应的水化物中碱性最强的是
(4)⑥、⑦、②三种元素原子半径由大到小的顺序是___>___>___(用元素符号填写)。
(5)①与②形成能产生温室效应的气体的电子式:
(6)请设计一个实验方案,比较⑧、⑩单质氧化性的强弱:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表是元素周期表的一部分。
请回答下列问题。
(1)非金属性最强的元素名称为___________ ,它位于元素周期表中的位置___________ 。
(2)硅元素的原子结构示意图是____________ ,其最高价氧化物是____________ (填“酸性”或“碱性”)氧化物。
(3)硼酸(H3BO3)的酸性_________ (填“>” 或“<”)碳酸(H2CO3)的酸性,说明你判断的理由:__________________________ 。
(4)NH3的电子式为________________ ,它属于____________ (填“离子”或“共价”)化合物。NH3的还原性_________ (填“>” 或“<”)PH3的还原性。
(5)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的化学方程式______________ 。
| H | He | ||||||
| Li | Be | B | C | N | O | F | Ne |
| Na | Mg | Al | Si | P | S | Cl | Ar |
(1)非金属性最强的元素名称为
(2)硅元素的原子结构示意图是
(3)硼酸(H3BO3)的酸性
(4)NH3的电子式为
(5)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E为五种短周期元素,它们的原子序数依次增大。A与C同主族,A元素的周期数等于族序数,C在短周期元素中原子半径最大,D元素形成的简单离子在同周期中半径最小,B与E同主族,E2-与Ar原子具有相同的电子层结构。回答下列问题:
(1)D在元素周期表中的位置是_______ ;
(2)E2-的离子结构示意图为_______ ;
(3)A、B、C形成的化合物电子式为_______ ,其与单质D反应的离子方程式为_______ ;
(4)A分别与B、E形成的最简单化合物中,热稳定性较好的是_______ (填化学式),能证明B、E元素非金属性强弱的化学方程式是_______ 。
(1)D在元素周期表中的位置是
(2)E2-的离子结构示意图为
(3)A、B、C形成的化合物电子式为
(4)A分别与B、E形成的最简单化合物中,热稳定性较好的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、M、Q、R皆为周期表中前20号元素,其原子半径与主要化合价的关系如图所。 电子式为
电子式为_________ 。
(2)比较Y和Z的简单氢化物,更稳定的是_________ (填化学式)。
(3)已知Q位于第三周期,则R在元素周期表中的位置是_________ 。
(4)下列推断正确的是_________ (填“序号”)。
a.简单离子半径: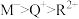
b.由X、Y、Z三种元素组成的化合物可能是盐或碱
c.Z与M的最高价氧化物对应水化物均为强酸
(5)M的单质通入淀粉-KI溶液,溶液变蓝,写出该反应的离子方程式_________ ;比较 和M的阴离子,还原性更强的是
和M的阴离子,还原性更强的是_________ (填离子符号),从原子结构的角度解释原因_________ 。
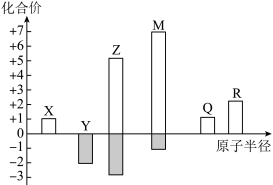
 电子式为
电子式为(2)比较Y和Z的简单氢化物,更稳定的是
(3)已知Q位于第三周期,则R在元素周期表中的位置是
(4)下列推断正确的是
a.简单离子半径:
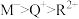
b.由X、Y、Z三种元素组成的化合物可能是盐或碱
c.Z与M的最高价氧化物对应水化物均为强酸
(5)M的单质通入淀粉-KI溶液,溶液变蓝,写出该反应的离子方程式
 和M的阴离子,还原性更强的是
和M的阴离子,还原性更强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知A、B、C、D、E、F是分属三个短周期六种主族元素,且原子序数依次增大。①B是植物生长三要素之一,它能形成多种氧化物,某些氧化物会造成光化学污染。②C和D能形成电子总数为30和38的两种化合物。③E的某种氧化物M可用做漂白剂。请回答下列问题:
(1)元素F在元素周期表中的位置是______________________________ 。
(2) C、D、E 三种元素原子半径由小到大的顺序是__________________ (用元素符号回答); C、D、E 三种元素形成的简单离子的离子半径由小到大的顺序是__________________ (用离子符号回答)。
(3) C和D形成电子总数为38的化合物中化学键类型有__________________________ (填“离子键”、“极性共价键”、“非极性共价键”)。
(4)写出D的最高价氧化物水化物的电子式______________________ 。
(5) E、F两种元素形成氢化物中还原性较强的是_________________ (填化学式); 用电子式表示该化合物的形成过程________________________________________ 。
(6)C、D、F形成的某种化合物N也可用做漂白剂,M、N以物质的量1∶1混合,混合物没有漂白性。用离子方程式解释其原因_____________________________________________ 。
(1)元素F在元素周期表中的位置是
(2) C、D、E 三种元素原子半径由小到大的顺序是
(3) C和D形成电子总数为38的化合物中化学键类型有
(4)写出D的最高价氧化物水化物的电子式
(5) E、F两种元素形成氢化物中还原性较强的是
(6)C、D、F形成的某种化合物N也可用做漂白剂,M、N以物质的量1∶1混合,混合物没有漂白性。用离子方程式解释其原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】1869年,门捷列夫制得世界上第一张元素周期表,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。如图为现代元素周期表的一部分,请回答下列问题:

(1)在这10种元素中,非金属性最强的元素在周期表中的位置是___________ 。
(2)由a、d、f三种元素形成的化合物属于___________ (填“离子”或“共价”)化合物。
(3)元素b、c形成的简单气态氢化物中较稳定的是___________ (填化学式)。
(4)d、h、i、j的简单离子半径由大到小 的顺序排列为___________ (填离子符号)。
(5)b和d可以形成一种酸性氧化物 ,其电子式为___________ 。
(6)c的最高价氧化物对应水化物的浓溶液与金属Cu反应的离子方程式 为___________ 。

(1)在这10种元素中,非金属性最强的元素在周期表中的位置是
(2)由a、d、f三种元素形成的化合物属于
(3)元素b、c形成的简单气态氢化物中较稳定的是
(4)d、h、i、j的简单离子半径
(5)b和d可以形成一种
(6)c的最高价氧化物对应水化物的浓溶液与金属Cu反应的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为___________ 。
(2)A、B、F三种元素的原子半径由大到小的顺序是___________ (填元素符号)。
(3)D元素最高价氧化物的水化物与E元素的最高价氧化物反应的离子方程式是___________ 。
(4)元素A与C形成的电子总数为22的分子的电子式为___________ ,B元素的单质的结构式为___________ 。
(5)用电子式表示元素D与G组成的化合物的形成过程___________ ,D元素最高价氧化物的水化物所含的化学键有___________ (填化学键类型)。
(6)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是___________ (填序号)。
a、与水反应比钠更剧烈
b、Rb2O在空气中易吸收水和二氧化碳
c、Rb2O2与水能剧烈反应并释放出O2
d、单质具有很强的氧化性
e、RbOH的碱性比同浓度的NaOH弱

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(2)A、B、F三种元素的原子半径由大到小的顺序是
(3)D元素最高价氧化物的水化物与E元素的最高价氧化物反应的离子方程式是
(4)元素A与C形成的电子总数为22的分子的电子式为
(5)用电子式表示元素D与G组成的化合物的形成过程
(6)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是
a、与水反应比钠更剧烈
b、Rb2O在空气中易吸收水和二氧化碳
c、Rb2O2与水能剧烈反应并释放出O2
d、单质具有很强的氧化性
e、RbOH的碱性比同浓度的NaOH弱
您最近一年使用:0次



