各类电池广泛用在交通工具(如电动汽车、电动自行车等)上,实现了节能减排,也为生活带来了极大的便利。
(1)传统汽车中使用的电池主要是铅蓄电池,其构造如图。

①放电时,铅蓄电池总反应式为:______ ;
②充电时,电源正极与______ (填“Pb”或“ ”)连接,溶液的pH会
”)连接,溶液的pH会______ (填“增大”、“减小”或“不变”)。
(2)重庆在新能源汽车的制造和开发上走在时代的前列。新能源汽车使用的主要是锂离子电池,某锂离子电池工作原理如图所示。
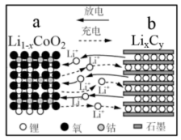
总反应式为:
①放电时,电极b是______ 极,a电极反应式为______ ;
②充电时,当导线中通过2mol 时,阴极的固体质量增加
时,阴极的固体质量增加______ g。
③与传统的铅蓄电池相比,锂电池具有的优点有:______ (一点即可)。
(3)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:
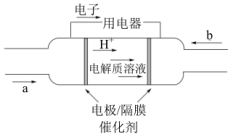
①a处通入的气体是______ ;
②电池每消耗5.6L(标准状况下)氢气,电路中通过的电子数目为______ 。
(1)传统汽车中使用的电池主要是铅蓄电池,其构造如图。

①放电时,铅蓄电池总反应式为:
②充电时,电源正极与
 ”)连接,溶液的pH会
”)连接,溶液的pH会(2)重庆在新能源汽车的制造和开发上走在时代的前列。新能源汽车使用的主要是锂离子电池,某锂离子电池工作原理如图所示。

总反应式为:

①放电时,电极b是
②充电时,当导线中通过2mol
 时,阴极的固体质量增加
时,阴极的固体质量增加③与传统的铅蓄电池相比,锂电池具有的优点有:
(3)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:

①a处通入的气体是
②电池每消耗5.6L(标准状况下)氢气,电路中通过的电子数目为
更新时间:2023-01-13 10:05:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据上表中记录的实验现象,回答下列问题。
(1)由电流表指针偏向可知,电流表指针偏向___________ 极(填“正”或“负”)。
(2)实验3中铝为___________ 极,电极反应式为___________ ;石墨为___________ 极,电极反应式为___________ 。
(3)写出实验4中铝电极的电极反应式___________ 。
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨烯 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
(1)由电流表指针偏向可知,电流表指针偏向
(2)实验3中铝为
(3)写出实验4中铝电极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)有一种新型的高能电池—钠硫电池(熔融的钠、硫为两极,以Na+导电的βAl2O3陶瓷作固体电解质),反应式为2Na+xS Na2Sx。
Na2Sx。

①充电时,钠极与外电源___ (填“正”或“负”)极相连。其阳极反应式:__ 。
②放电时,发生还原反应的是___ (填“钠”或“硫”)极。
③用该电池作电源电解(如图)NaCl溶液(足量),写出电解NaCl溶液的离子方程式:__ ,若钠硫电池工作一段时间后消耗23gNa(电能的损耗忽略不计),若要使溶液完全恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入(或通入)__ (填物质名称)。
④若用该钠硫电池作电源在一铁片上镀铜,此铁片与__ (填“钠”或“硫”)极相连。
(2)某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。

①放电时,交换膜左侧溶液中实验现象___ 。
②当电路中转移0.01mole-时,交换膜左侧溶液中约减少__ mol离子。
③该电池的能量转化的主要形式为__ 。
 Na2Sx。
Na2Sx。
①充电时,钠极与外电源
②放电时,发生还原反应的是
③用该电池作电源电解(如图)NaCl溶液(足量),写出电解NaCl溶液的离子方程式:
④若用该钠硫电池作电源在一铁片上镀铜,此铁片与
(2)某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。

①放电时,交换膜左侧溶液中实验现象
②当电路中转移0.01mole-时,交换膜左侧溶液中约减少
③该电池的能量转化的主要形式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】CO2、CO可与H2在一定条件下反应合成二甲醚(CH3OCH3)、甲醇(CH3OH)、草酸(H2C2O4)等化工原料。
(1)二甲醚可作为绿色环保型能源。二甲醚空气燃料电池的工作原理如图所示。该电池工作时,c通入的物质为______________ ,该电极的电极反应式为_______________ 。

(2)某同学用甲醇和其它试剂组装了如下图所示装置,来研究有关电化学问题(甲、乙、丙三池中电解质足量)。当闭合该装置的电键K时,观察到电流计的指针发生了偏转。

①丙池中F电极为____________ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为_______________ ;
②若丙池溶液的体积为500 mL,当乙池中C极质量减轻5.4g时,丙池溶液的pH为_______ (忽略溶液体积的变化);
③一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是______ (填序号)。
A. Cu B. CuO C. Cu(OH)2 D. Cu2(OH)2CO3
(3)已知:常温下,H2C2O4的电离常数分别是Ka1≈5.0×10-2,Ka2≈6.0×l0-5。草酸的钾盐有K2C2O4、KHC2O4。常温下,KHC2O4的水解常数Kh2=___________ ,KHC2O4溶液的pH______ 7(填“﹥”、“﹤”或“=”)。
(1)二甲醚可作为绿色环保型能源。二甲醚空气燃料电池的工作原理如图所示。该电池工作时,c通入的物质为

(2)某同学用甲醇和其它试剂组装了如下图所示装置,来研究有关电化学问题(甲、乙、丙三池中电解质足量)。当闭合该装置的电键K时,观察到电流计的指针发生了偏转。

①丙池中F电极为
②若丙池溶液的体积为500 mL,当乙池中C极质量减轻5.4g时,丙池溶液的pH为
③一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是
A. Cu B. CuO C. Cu(OH)2 D. Cu2(OH)2CO3
(3)已知:常温下,H2C2O4的电离常数分别是Ka1≈5.0×10-2,Ka2≈6.0×l0-5。草酸的钾盐有K2C2O4、KHC2O4。常温下,KHC2O4的水解常数Kh2=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
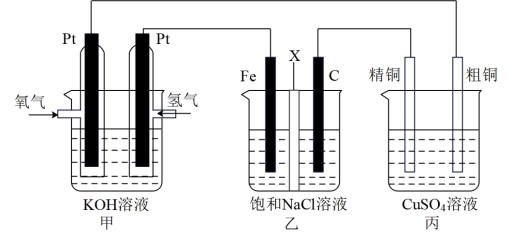
根据要求回答相关问题:
(1)通入氧气的电极为_______ (填“正极”或“负极”),
(2)铁电极为_______ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为_______ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_______ (填“增大”“减小”或“不变”)。
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为_______ ;丙装置中阴极析出铜的质量为_______ 。
(5)利用图制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的_______ 极;该发生器中反应的总离子方程式为_______
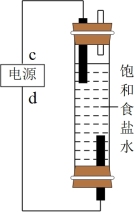
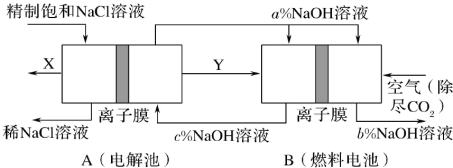
(6)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为_______ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
(5)利用图制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的

(6)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氢能源是21世纪极具开发前景的新能源之一,它既是绿色能源,又可循环使用。如图是氢能源循环体系图(X是H2O;Y是H2、O2)。回答下列问题:
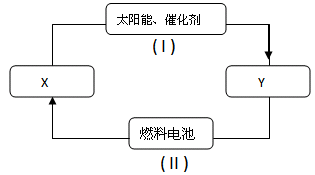
(1)从能量转换的角度看,过程II主要是将___ 能转化为____ 能。
(2)在该燃料电池中,H2所在的一极为_____ 极;若电解质溶液为碱性的KOH溶液,试写出两极的电极方程式:正极_______ 负极______________

(1)从能量转换的角度看,过程II主要是将
(2)在该燃料电池中,H2所在的一极为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.700℃时,若向2L恒容的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g) C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。

(1)0~10min 内的 CO2平均反应速率v( CO2)=___________
(2)图中A点v正___________ v逆(填“>”“<”或“=”)。
(3)下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO2与N2的物质的量之比为1∶1
B.混合气体的总物质的量不随时间的变化而变化
C.单位时间内每消耗a mol N2,同时消耗2a mol NO
D.N2的质量分数在混合气体中保持不变
E.混合气体的密度不随时间的变化而变化
Ⅱ.氢氧燃料电池的电解质溶液为KOH溶液,电池总反应为2H2+O2=2H2O。回答下列问题:
(4)该电池的负极反应式为___________ 。
(5)电池工作一段时间后电解质溶液的
___________ (填“增大”“减小”或“不变”)。
 C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。
(1)0~10min 内的 CO2平均反应速率v( CO2)=
(2)图中A点v正
(3)下列叙述中能说明上述反应达到平衡状态的是
A.反应中CO2与N2的物质的量之比为1∶1
B.混合气体的总物质的量不随时间的变化而变化
C.单位时间内每消耗a mol N2,同时消耗2a mol NO
D.N2的质量分数在混合气体中保持不变
E.混合气体的密度不随时间的变化而变化
Ⅱ.氢氧燃料电池的电解质溶液为KOH溶液,电池总反应为2H2+O2=2H2O。回答下列问题:
(4)该电池的负极反应式为
(5)电池工作一段时间后电解质溶液的

您最近一年使用:0次
【推荐1】利用电化学原理,将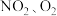 和熔融
和熔融 制成燃料电池,模拟工业电解法来处理含
制成燃料电池,模拟工业电解法来处理含 的废水,如图所示;电解过程中溶液发生反应:
的废水,如图所示;电解过程中溶液发生反应: 。
。
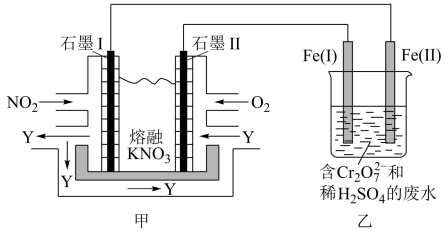
(1)甲池工作时, 转变成绿色硝化剂Y,Y是
转变成绿色硝化剂Y,Y是 ,可循环使用。则石墨II是电池的
,可循环使用。则石墨II是电池的_______ (填“正”或“负”)极;石墨I附近发生的电极反应式为_______ 。
(2)工作时,甲池内的 向
向_______ (填“石墨I”或“石墨II”)极移动;在相同条件下,消耗的 和
和 的体积比为
的体积比为_______ 。
(3)乙池中 (I)棒上发生的电极反应为
(I)棒上发生的电极反应为_______ 。
(4)若溶液中减少了 ,则电路中至少转移了
,则电路中至少转移了_______  电子。
电子。
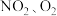 和熔融
和熔融 制成燃料电池,模拟工业电解法来处理含
制成燃料电池,模拟工业电解法来处理含 的废水,如图所示;电解过程中溶液发生反应:
的废水,如图所示;电解过程中溶液发生反应: 。
。
(1)甲池工作时,
 转变成绿色硝化剂Y,Y是
转变成绿色硝化剂Y,Y是 ,可循环使用。则石墨II是电池的
,可循环使用。则石墨II是电池的(2)工作时,甲池内的
 向
向 和
和 的体积比为
的体积比为(3)乙池中
 (I)棒上发生的电极反应为
(I)棒上发生的电极反应为(4)若溶液中减少了
 ,则电路中至少转移了
,则电路中至少转移了 电子。
电子。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】CH4﹣O2燃料电池具有放电稳定,无污染等优点,如图用甲烷氧气燃料电池电解饱和氯化钠溶液的模型图,其中氯化钠溶液滴有酚酞试液。已知甲烷氧气燃料电池的总反应式为:CH4+2O2+2KOH K2CO3+3H2O请认真读图,回答以下问题:

(1)请写出通入甲烷气体的一极所发生的电极反应式:____________________ ,其附近的pH值________ (填“不变”或“变大”或“变小”) 通入O2气体的一极所发生的电极反应式:_______________ ,其附近的pH值________ (填“不变”或“变大”或“变小”)。
(2)a为_______ 极,电极反应式为______________ ;b为_______ 极,电极反应式为_________________ ,现象是_______________ ;总方程式为 ____________________________ 。
(3)如果通入1mol的甲烷完全参与电极反应,则电路中转移___________ mol的电子,a电极产生的气体在标准状况下的体积为______________ L。

(1)请写出通入甲烷气体的一极所发生的电极反应式:
(2)a为
(3)如果通入1mol的甲烷完全参与电极反应,则电路中转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某课外活动小组用下图装置进行实验,试回答:

(1)若开始时K接M,则该装置为________ (填“原电池”或“电解池”)铁极上的电极反应式为________ 。
(2)若开始时K接N,则石墨极为______ 极(填“正”、“负”、“阳” 或“阴”),装置中的总化学方程式为________ ,铁极上的现象为________ ,石墨电极的反应现象为________ ,若反应过程中有0.1mol的电子发生转移,则铁电极上产生物质的质量为____ g,石墨极上产生的物质在标准状况下的体积为________ L。

(1)若开始时K接M,则该装置为
(2)若开始时K接N,则石墨极为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】CuSO4溶液是中学化学及农业生产中常见的一种试剂。
(1)某同学配制CuSO4溶液时,需加入一定量的硫酸溶液,用离子方程式说明其原因是____________ 。
(2)该同学利用制得的CuSO4溶液,进行以下实验探究。
①图一是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。电解质溶液乙是_______ (填“ZnSO4”或“CuSO4”) 溶液; Cu极的电板反应式是_______ 。

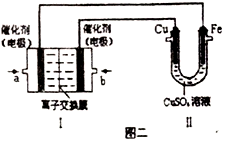
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则a 处通入的是_______ (填“CH4”或“O2” ),a处电极上发生的电极反应式是_____________ 。若只把Ⅱ中电极均换为惰性电极,电解时的化学反应方程式为_____________________ 。若把Ⅱ中电极均换为惰性电极,电解液换为含有0.04molCuSO4和0.04molNaCl的混合溶液400mL,当阳极产生的气体为672mL (标准状况下) 时,溶液的pH=_______ (假设电解后溶液体积不变)。
(1)某同学配制CuSO4溶液时,需加入一定量的硫酸溶液,用离子方程式说明其原因是
(2)该同学利用制得的CuSO4溶液,进行以下实验探究。
①图一是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。电解质溶液乙是


②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则a 处通入的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究电化学原理与应用有非常重要的意义。
(1)与普通(酸性)锌锰电池相比较,碱性锌锰电池的优点是_______ (回答一条即可)。
(2)铅蓄电池是最常见的二次电池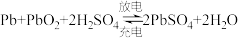 。
。
①充电时阴极反应为_______ 。
②用铅蓄电池为电源进行电解饱和食盐水实验(石墨棒为阳极,铁为阴极,食盐水500mL,温度为常温),当电路中有0.05mol电子转移时,食盐水的pH为_______ (假设溶液体积不变,产物无损耗)。
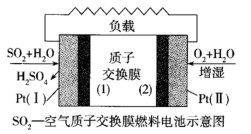
(3)二氧化硫—空气质子交换膜燃料电池实现了制硫酸发电、环保三位一体的结合,原理如图所示。Pt(II)上的电极反应式_______ 。
(4)高铁酸钠( )易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为
)易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为 ,工作原理如图所示。
,工作原理如图所示。
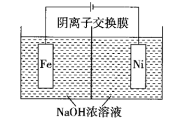
装置通电后,铁电极附近生成紫红色的 ,镍电极有气泡产生。电解一段时间后,
,镍电极有气泡产生。电解一段时间后, 降低的区域在
降低的区域在_______ (填“阴极室”或“阳极室”);铁电极发生的反应为_______ 。
(1)与普通(酸性)锌锰电池相比较,碱性锌锰电池的优点是
(2)铅蓄电池是最常见的二次电池
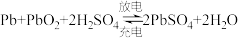 。
。①充电时阴极反应为
②用铅蓄电池为电源进行电解饱和食盐水实验(石墨棒为阳极,铁为阴极,食盐水500mL,温度为常温),当电路中有0.05mol电子转移时,食盐水的pH为
(3)二氧化硫—空气质子交换膜燃料电池实现了制硫酸发电、环保三位一体的结合,原理如图所示。Pt(II)上的电极反应式

(4)高铁酸钠(
 )易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为
)易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为 ,工作原理如图所示。
,工作原理如图所示。
装置通电后,铁电极附近生成紫红色的
 ,镍电极有气泡产生。电解一段时间后,
,镍电极有气泡产生。电解一段时间后, 降低的区域在
降低的区域在
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图所示,甲、乙两U形管各盛有100mL溶液,请回答下列问题:
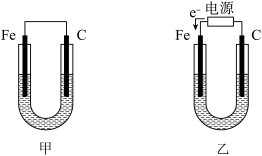
(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生_____________ 腐蚀(填“析氢”或“吸氧”),碳棒上电极反应式__________________________ ;
②甲池铁棒腐蚀的速率比乙池铁棒_____ (填“快”、“慢”或“相等”)。
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式___________________________________ ;
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为___________ mol·L-1。

(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生
②甲池铁棒腐蚀的速率比乙池铁棒
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为
您最近一年使用:0次



