常温下,下列事实能说明HClO是弱电解质的是
| A.0.01 mol⋅L−1的HClO溶液的导电能力弱于同浓度的盐酸 |
| B.NaClO、HClO都易溶于水 |
| C.NaClO的电离方程式:NaClO=Na++ClO− |
| D.HClO与Na2SO3溶液反应,可以得到Na2SO4 |
更新时间:2023-01-14 15:07:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述正确的是
| A.95℃时纯水的pH<7,说明加热可导致水呈酸性 |
| B.pH=3的醋酸溶液,稀释至10倍时溶液的pH<4 |
| C.等浓度的醋酸溶液与氢氧化钠溶液等体积混合后pH=7 |
| D.等体积pH均为3的醋酸和盐酸分别与足量Zn反应,盐酸产生的H2多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,在体积均为20mL、浓度均为0.1 的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)表示为
的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)表示为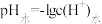 。
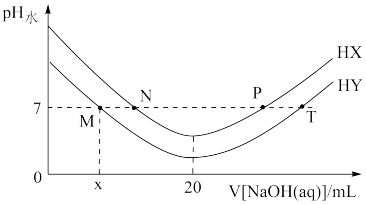
。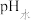 与滴加氢氧化钠溶液体积的关系如图所示。下列推断错误的是
与滴加氢氧化钠溶液体积的关系如图所示。下列推断错误的是
 的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)表示为
的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)表示为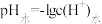 。
。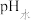 与滴加氢氧化钠溶液体积的关系如图所示。下列推断错误的是
与滴加氢氧化钠溶液体积的关系如图所示。下列推断错误的是
A.HX的电离方程式为 |
B.T点时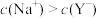 , ,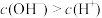 |
| C.常温下,用蒸馏水分别稀释N、P点溶液,pH都降低 |
D.常温下,HY的电离常数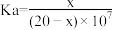 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气。下列说法不正确 的是
| A.甲烧杯中放入锌的质量比乙烧杯中放入锌的质量大 | B.乙烧杯中的酸过量 |
| C.两烧杯中参加反应的锌等量 | D.反应所需的时间:乙烧杯比甲烧杯长 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,下列有关两种溶液的说法不正确的是( )
| 序号 | ① | ② |
| pH | 12 | 12 |
| 溶液 | 氨水 | 氢氧化钠溶液 |
A.①②两溶液中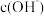 相等 相等 |
| B.②溶液的物质的量浓度为0.01mol·L-1 |
| C.①②两溶液分别加水稀释10倍,稀释后溶液的pH:①<② |
| D.等体积的①②两溶液分别与0.01mol·L-1的稀盐酸完全中和,消耗稀盐酸的体积:①>② |
您最近一年使用:0次

 的值增大
的值增大 的值增大
的值增大

