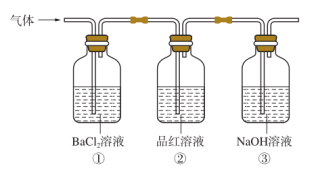
采用如图装置制取一定量的饱和氯水,并进行氯水的性质实验。
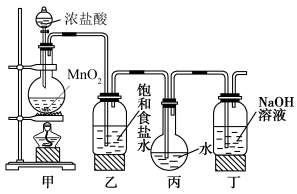
(1)在装入药品前应进行的操作______________ 。
(2)写出丁装置中发生反应的离子方程式:________ 。
(3)用制得的饱和氯水分别进行下列实验:
①滴入碳酸钠溶液中,有气体生成,说明氯水中发生反应的离子是___________ ;
②滴到蓝色石蕊试纸上的现象:_______________ 。
(4)久置的氯水漂白效果明显不足或消失,原因用化学方程式表示:_________________ 。
(5)将制得的饱和氯水慢慢滴入含有酚酞的 稀溶液中,当滴到一定量时,红色突然褪去。产生上述现象的原因可能有两种
稀溶液中,当滴到一定量时,红色突然褪去。产生上述现象的原因可能有两种 简要文字说明
简要文字说明 :
:

______________________ ;

______________________ 。

(1)在装入药品前应进行的操作
(2)写出丁装置中发生反应的离子方程式:
(3)用制得的饱和氯水分别进行下列实验:
①滴入碳酸钠溶液中,有气体生成,说明氯水中发生反应的离子是
②滴到蓝色石蕊试纸上的现象:
(4)久置的氯水漂白效果明显不足或消失,原因用化学方程式表示:
(5)将制得的饱和氯水慢慢滴入含有酚酞的
 稀溶液中,当滴到一定量时,红色突然褪去。产生上述现象的原因可能有两种
稀溶液中,当滴到一定量时,红色突然褪去。产生上述现象的原因可能有两种 简要文字说明
简要文字说明 :
:

更新时间:2023-01-17 09:33:00
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】为了探究HClO的漂白性,某同学设计了如下的实验。
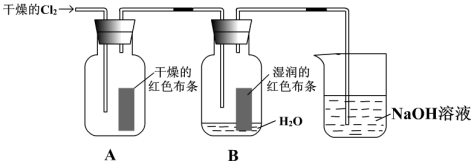
(1)写出Cl2与水反应的化学方程式_______ 。
(2)通入Cl2后,集气瓶A中的现象是_______ ,集气瓶B中的现象是_______ 。
(3)烧杯中发生反应的化学方程式是_______ 。

(1)写出Cl2与水反应的化学方程式
(2)通入Cl2后,集气瓶A中的现象是
(3)烧杯中发生反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某校化学兴趣小组为研究氯气的性质,设计用如图所示的装置进行实验,其中a为干燥的红色试纸,b为湿润的红色试纸。

回答下列问题:
(1)装置I中仪器c的名称是______ ,实验室用二氧化锰和浓盐酸制备氯气的化学方程式为_______ 。
(2)装置V的作用是_______ 。
(3)若产生的 足量,实验过程中装置IV中的实验现象是
足量,实验过程中装置IV中的实验现象是________ 。
(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“装置II中a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置I与II之间添加下图中的装置________ (填序号)。

(5)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应II的化学方程式为_________ 。

回答下列问题:
(1)装置I中仪器c的名称是
(2)装置V的作用是
(3)若产生的
 足量,实验过程中装置IV中的实验现象是
足量,实验过程中装置IV中的实验现象是(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“装置II中a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置I与II之间添加下图中的装置

(5)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应II的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】84消毒液是一种常见的含氯消毒剂。如图为某品牌84消毒液的说明书中的部分内容。
(1)常温,将氯气通入NaOH溶液中可制得84消毒液的主要成分。写出离子方程式:_______ 。
(2)某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。
;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。
I.向2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
II.向2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
III.测得84消毒液在不同温度时ORP随时间的变化曲线如下。
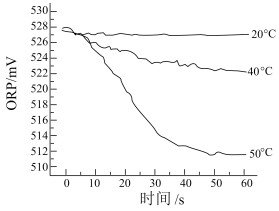
①已知白醋显酸性,不具有漂白性。实验I、II现象不同的原因是_______ 。
②由实验III可得出的结论是_______ 。ORP值不同的原因可能是_______ 。
(3)针对不同物品的消毒,84消毒液需要稀释到不同的浓度来使用。取含次氯酸钠14.9g/L的84消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为_______  。
。
(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是 将
将 氧化产生的
氧化产生的 促进藻类快速生长。写出该反应的化学方程式:
促进藻类快速生长。写出该反应的化学方程式:_______ 。
| 产品特点 本品是以次氯酸钠为主要成分的液体消毒剂。可杀灭肠道致病菌、化脓性球菌、致病性酵母菌,并能灭活病毒。 注意事项 1.本品易使有色衣脱色,禁止用于丝、毛、麻织物的消毒。 2.不得将本品与酸性产品(如洁厕类清洁产品)同时使用。 3.置于避光、阴凉处保存。 4.需稀释后使用,勿口服。 |
(1)常温,将氯气通入NaOH溶液中可制得84消毒液的主要成分。写出离子方程式:
(2)某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有
 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。
;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。I.向2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
II.向2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
III.测得84消毒液在不同温度时ORP随时间的变化曲线如下。

①已知白醋显酸性,不具有漂白性。实验I、II现象不同的原因是
②由实验III可得出的结论是
(3)针对不同物品的消毒,84消毒液需要稀释到不同的浓度来使用。取含次氯酸钠14.9g/L的84消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为
 。
。(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是
 将
将 氧化产生的
氧化产生的 促进藻类快速生长。写出该反应的化学方程式:
促进藻类快速生长。写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某研究小组利用下图所示装置制备氯气并进行卤素性质的探究。
Ⅰ.制备 并进行性质实验(夹持装置和加热仪器略)
并进行性质实验(夹持装置和加热仪器略) 与浓盐酸反应制取
与浓盐酸反应制取 ,反应的化学方程式为
,反应的化学方程式为________ 。
(2)B中发生反应的离子方程式为________ 。
(3)反应一段时间后,取一支试管,加入2mLC中的橙黄色溶液,再滴入几滴淀粉KI溶液,观察到溶液变为蓝色。通过以上实验,能否得出结论: 的氧化性强于
的氧化性强于 。理由
。理由________ 。
Ⅱ.研究小组为了进一步验证 和
和 能否将
能否将 氧化为
氧化为 ,设计如下实验:
,设计如下实验:
(4)同学甲认为实验i的现象说明溴水能将 氧化:同学乙认为仅从“溶液为黄色”得出“溴水能将
氧化:同学乙认为仅从“溶液为黄色”得出“溴水能将 氧化”的结论不严谨,原因为
氧化”的结论不严谨,原因为________ ,同学乙补充了实验方案,证明了“溴水能将 氧化”。同学乙补充的实验方案是
氧化”。同学乙补充的实验方案是________ 。
(5)分析实验ii及上述实验,判断 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为________ 。
(6)从“位置—结构—性质”的角度解释 、
、 、
、 氧化性逐渐减弱的原因
氧化性逐渐减弱的原因________ 。
Ⅰ.制备
 并进行性质实验(夹持装置和加热仪器略)
并进行性质实验(夹持装置和加热仪器略)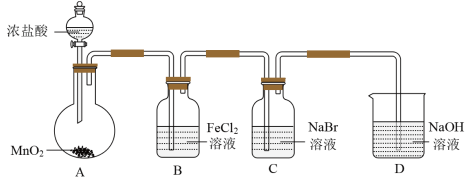
 与浓盐酸反应制取
与浓盐酸反应制取 ,反应的化学方程式为
,反应的化学方程式为(2)B中发生反应的离子方程式为
(3)反应一段时间后,取一支试管,加入2mLC中的橙黄色溶液,再滴入几滴淀粉KI溶液,观察到溶液变为蓝色。通过以上实验,能否得出结论:
 的氧化性强于
的氧化性强于 。理由
。理由Ⅱ.研究小组为了进一步验证
 和
和 能否将
能否将 氧化为
氧化为 ,设计如下实验:
,设计如下实验:实验 | 操作 | 现象 |
i | 先向试管中加入2mL新制 溶液,滴加少量溴水,振荡 溶液,滴加少量溴水,振荡 | 溶液为黄色 |
ii | 先向试管中加入2mL新制 溶液和0.5mL苯(有机溶剂,不溶于水,浮于液面上),将胶头滴管伸入下层溶液中,滴加0.5mL稀碘水 溶液和0.5mL苯(有机溶剂,不溶于水,浮于液面上),将胶头滴管伸入下层溶液中,滴加0.5mL稀碘水 | 下层溶液为黄色 |
| 再滴加0.5mLKSCN溶液于下层溶液中 | 无红色出现 |
(4)同学甲认为实验i的现象说明溴水能将
 氧化:同学乙认为仅从“溶液为黄色”得出“溴水能将
氧化:同学乙认为仅从“溶液为黄色”得出“溴水能将 氧化”的结论不严谨,原因为
氧化”的结论不严谨,原因为 氧化”。同学乙补充的实验方案是
氧化”。同学乙补充的实验方案是(5)分析实验ii及上述实验,判断
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(6)从“位置—结构—性质”的角度解释
 、
、 、
、 氧化性逐渐减弱的原因
氧化性逐渐减弱的原因
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】氯气是一种重要的工业原料。资料显示:
Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
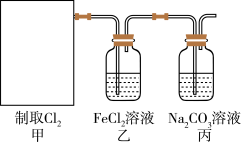
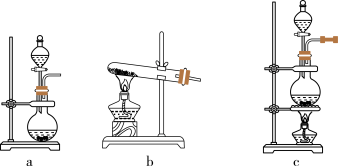
(1)在该实验中,甲部分的装置是________ (填字母)。
(2)乙装置中FeCl2溶液与Cl2反应的离子方程式是___________________________ 。
(3)丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中发生反应的化学方程式是_________________________________ 。
(4)该实验存在明显的缺陷,改进的方法是___________________________________ 。
Ca(ClO)2+CaCl2+2H2SO4
 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
(1)在该实验中,甲部分的装置是

(2)乙装置中FeCl2溶液与Cl2反应的离子方程式是
(3)丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中发生反应的化学方程式是
(4)该实验存在明显的缺陷,改进的方法是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某校化学兴趣小组为研究 Cl2单质的性质,设计如图所示装置进行实验。装置 III中夹持装置已略去,其中a 为干燥的品红试纸,b 为湿润的品红试纸。
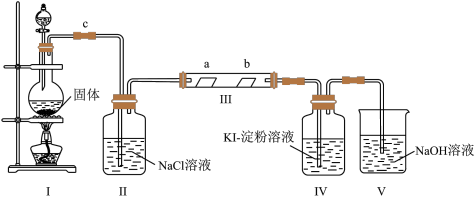
(1)装置I中装固体药品的仪器名称是_______ ;实验室以二氧化锰和浓盐酸制备氯气的离子方程式是:_______ ;
(2)装置Ⅱ的作用是_______ ;
(3)实验过程中,装置Ⅳ中的实验现象为_______ ;发生反应的化学方程式为_______ ;
(4)实验结束后,该组同学在装置Ⅲ中观察 b 的红色退去,但是并未观察到“a 无明显变化”这一预期现象,为了达到这一目的,你认为应在_______ 之间还需添加洗气瓶(选填装置序号),该装置的作用是_______ ;
(5)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式_______ 。

(1)装置I中装固体药品的仪器名称是
(2)装置Ⅱ的作用是
(3)实验过程中,装置Ⅳ中的实验现象为
(4)实验结束后,该组同学在装置Ⅲ中观察 b 的红色退去,但是并未观察到“a 无明显变化”这一预期现象,为了达到这一目的,你认为应在
(5)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
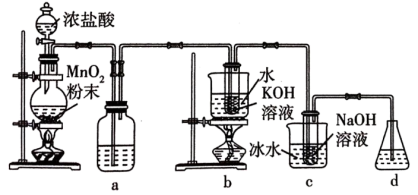
回答下列问题:
(1)盛放 粉末的仪器名称是
粉末的仪器名称是___________ ,a中的试剂为___________ 。
(2)b中采用的加热方式是___________ ,c中化学反应的离子方程式是___________ 。
(3)d的作用是___________ ,可选用试剂___________ (填标号)。
A. B.
B. C.
C. D.
D.
(4)取少量 和
和 溶液分别置于1号和2号试管中,滴加中性
溶液分别置于1号和2号试管中,滴加中性 溶液:
溶液:
1号试管溶液颜色不变。
2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显
层显___________ 色。可知该条件下 的氧化能力
的氧化能力___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
回答下列问题:
(1)盛放
 粉末的仪器名称是
粉末的仪器名称是(2)b中采用的加热方式是
(3)d的作用是
A.
 B.
B. C.
C. D.
D.
(4)取少量
 和
和 溶液分别置于1号和2号试管中,滴加中性
溶液分别置于1号和2号试管中,滴加中性 溶液:
溶液:1号试管溶液颜色不变。
2号试管溶液变为棕色,加入
 振荡,静置后
振荡,静置后 层显
层显 的氧化能力
的氧化能力 (填“大于”或“小于”)。
(填“大于”或“小于”)。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】如图为实验室用二氧化锰和浓盐酸为原料制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为红色的铜网。
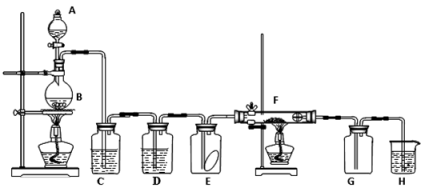
(1)仪器A的名称是___________ 。
(2)写出MnO2与浓盐酸反应的化学方程式___________ 。
(3)装置C中盛装的溶液是___________ ,D中试剂的作用是___________ 。
(4)E中的红色布条是否褪色?___________ (填“是”或“否”),写出F中反应的化学方程式:___________ 。
(5)H中的试剂为___________ ,其作用是___________ ,写出H中发生反应的离子方程式___________ 。

(1)仪器A的名称是
(2)写出MnO2与浓盐酸反应的化学方程式
(3)装置C中盛装的溶液是
(4)E中的红色布条是否褪色?
(5)H中的试剂为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】 是重要的化工产品,主要用作水处理剂,还用作媒染剂、催化剂等,某小组设计如图实验装置制备氯化铁并探究其性质。
是重要的化工产品,主要用作水处理剂,还用作媒染剂、催化剂等,某小组设计如图实验装置制备氯化铁并探究其性质。
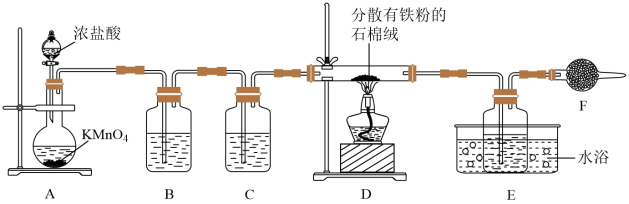
已知:①A中发生反应的生成物有 、
、 、
、 和
和 。
。
② 易升华,遇水蒸气易潮解。
易升华,遇水蒸气易潮解。
③石棉绒是一种耐火材料,不参与反应。
(1)A中反应的离子方程式为___________ ,C中试剂为___________ ,石棉绒的作用是___________ 。
(2)E采用的是___________ (填“热”或“冷”)水浴,目的是___________ 。
(3)F中的试剂可能是___________ (填标号),F的作用为___________ 。
a.氯化钙 b.氯化钠 c.碱石灰
(4)取适量 溶液于试管中,加入几滴硫氰化钾溶液,试管内溶液呈
溶液于试管中,加入几滴硫氰化钾溶液,试管内溶液呈___________ 色;往 溶液中加入适量铜粉,发生反应的化学方程式为
溶液中加入适量铜粉,发生反应的化学方程式为___________ 。
 是重要的化工产品,主要用作水处理剂,还用作媒染剂、催化剂等,某小组设计如图实验装置制备氯化铁并探究其性质。
是重要的化工产品,主要用作水处理剂,还用作媒染剂、催化剂等,某小组设计如图实验装置制备氯化铁并探究其性质。
已知:①A中发生反应的生成物有
 、
、 、
、 和
和 。
。②
 易升华,遇水蒸气易潮解。
易升华,遇水蒸气易潮解。③石棉绒是一种耐火材料,不参与反应。
(1)A中反应的离子方程式为
(2)E采用的是
(3)F中的试剂可能是
a.氯化钙 b.氯化钠 c.碱石灰
(4)取适量
 溶液于试管中,加入几滴硫氰化钾溶液,试管内溶液呈
溶液于试管中,加入几滴硫氰化钾溶液,试管内溶液呈 溶液中加入适量铜粉,发生反应的化学方程式为
溶液中加入适量铜粉,发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某化学研究性学习小组设计了如图所示的实验装置,目的是做钠与水反应的实验并验证①钠的物理性质;②钠和水反应的产物。请回答下列问题:
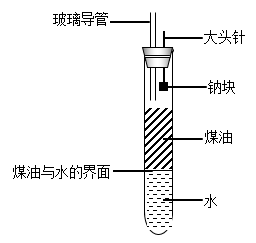
(1)实验开始时,欲使钠与水接触反应,应如何操作?_______ 。
(2)反应开始后,试管中能观察到的实验现象是:_______(填字母)
(3)通过上述现象,能够验证钠的哪些物理 性质:_______

(1)实验开始时,欲使钠与水接触反应,应如何操作?
(2)反应开始后,试管中能观察到的实验现象是:_______(填字母)
| A.钠在水层中反应,熔成小球并四处游动 |
| B.钠在两液体界面处反应,熔成小球并可能上下跳动 |
| C.煤油中有气泡产生 |
| D.钠不断地减小至消失 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】兴趣小组围绕乙醇的性质进行了探究。请完成下列问题:
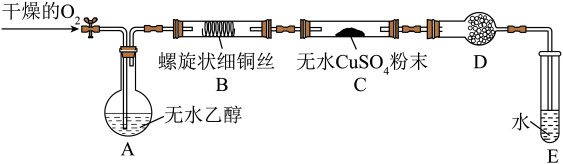
已知:乙醇的沸点为78°C,易溶于水;乙醛的沸点为20.8°C,易溶于水。
(1)乙醇发生催化氧化反应的化学方程式为___________ 。
(2)实验时上述装置需要加热,其中应该首先加热的是装置___________ (填字母),为使装置A中的乙醇形成稳定的蒸气,适宜的加热方法是___________ 。
(3)实验开始后,间歇性地通入氧气,装置B中观察到的现象是___________ 。
(4)装置C的作用是___________ ,若去掉装置D,对该实验是否有影响?__________ (填“是”或“否”),原因是___________ 。

已知:乙醇的沸点为78°C,易溶于水;乙醛的沸点为20.8°C,易溶于水。
(1)乙醇发生催化氧化反应的化学方程式为
(2)实验时上述装置需要加热,其中应该首先加热的是装置
(3)实验开始后,间歇性地通入氧气,装置B中观察到的现象是
(4)装置C的作用是
您最近一年使用:0次

 )制备硫酸。高温条件下
)制备硫酸。高温条件下 发生如下分解反应:
发生如下分解反应: 。为检验
。为检验 、
、 。
。