A、B、C是由短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图所示的关系,完成下列空白:
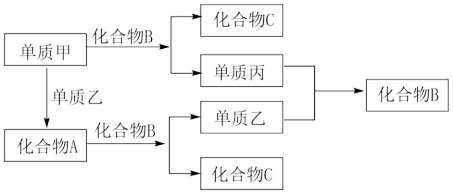
(1)单质甲的原子结构示意图_______ 。
(2)单质甲与化合物B反应的离子方程式为_______ ,5.05 g单质甲-钾合金溶于200 mL水生成0.075 mol H2,确定该合金的化学式为_______ 。
(3)向50 mL某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1 mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况。

①由A确定滴加前60 mL的盐酸时,发生所有反应的离子方程式是_______ 。
②由A图表明,原溶液通入CO2气体后,所得溶液中的溶质的化学式为_______ 。
③原化合物C溶液的物质的量浓度为_______ 。
④由A、B可知,两次实验通入的CO2的体积比为_______ 。

(1)单质甲的原子结构示意图
(2)单质甲与化合物B反应的离子方程式为
(3)向50 mL某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1 mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况。

①由A确定滴加前60 mL的盐酸时,发生所有反应的离子方程式是
②由A图表明,原溶液通入CO2气体后,所得溶液中的溶质的化学式为
③原化合物C溶液的物质的量浓度为
④由A、B可知,两次实验通入的CO2的体积比为
更新时间:2023-01-19 14:26:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】作为高中生,学会利用我们课堂上学到的知识来解决生活中的一些问题,是我们学习的重要目的之一。某中学的化学实验兴趣小组,一行四人,利用实验室老师提供的基本仪器和药品,自行购置了鸡蛋,食醋等生活用品,进行了如下探究。
I.甲同学老家在山西,对儿时在家乡品尝到的山西老陈醋的滋味记忆犹新,而今总是觉得超市买到的醋不如儿时的味道,查阅相关资料后,得知以下信息:
①醋分两种,酿造醋和配制醋。正宗的老陈醋必须经长久时间酿造才得此美味,市场上多充斥着工业醋酸加水勾兑的配制醋;
②酿造醋国家标准为醋酸含量必须大于3.50g/100mL,而配制醋国家标准仅为1.50g~3.50g/100mL;
③在老师的帮助下,测定了超市购买的食醋中,醋酸的物质的量浓度为0.75mol/L。
(1)请帮助甲同学计算从超市购买的食醋中醋酸含量为_____ g/100mL,属于____ 醋(填“酿造”或“配制”,醋酸的化学式为CH3COOH)。
(2)请写出醋酸与鸡蛋壳(主要成分为CaCO3)反应的离子方程式_________________ 。
II.下图是该学校化学实验室浓盐酸试剂标签上的部分内容。

乙同学现用该浓盐酸配制100mL 1mol•L﹣1的稀盐酸。
可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
(1)配制稀盐酸时,还缺少的仪器有________________ 。
(2)经计算,配制100mL1mol•L﹣1的稀盐酸需要用量筒量取上述浓盐酸的体积为_____ mL
(3)对所配制的稀盐酸进行测定,发现其浓度小于1mol•L﹣1,引起误差的原因可能是_______
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
III.丙同学对课堂上学到的胶体的相关知识产生了浓厚兴趣。他将乙同学配制好的盐酸溶液加入到鸡蛋清溶液中,发现出现絮状沉淀,此现象称为________________ 。
I.甲同学老家在山西,对儿时在家乡品尝到的山西老陈醋的滋味记忆犹新,而今总是觉得超市买到的醋不如儿时的味道,查阅相关资料后,得知以下信息:
①醋分两种,酿造醋和配制醋。正宗的老陈醋必须经长久时间酿造才得此美味,市场上多充斥着工业醋酸加水勾兑的配制醋;
②酿造醋国家标准为醋酸含量必须大于3.50g/100mL,而配制醋国家标准仅为1.50g~3.50g/100mL;
③在老师的帮助下,测定了超市购买的食醋中,醋酸的物质的量浓度为0.75mol/L。
(1)请帮助甲同学计算从超市购买的食醋中醋酸含量为
(2)请写出醋酸与鸡蛋壳(主要成分为CaCO3)反应的离子方程式
II.下图是该学校化学实验室浓盐酸试剂标签上的部分内容。

乙同学现用该浓盐酸配制100mL 1mol•L﹣1的稀盐酸。
可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
(1)配制稀盐酸时,还缺少的仪器有
(2)经计算,配制100mL1mol•L﹣1的稀盐酸需要用量筒量取上述浓盐酸的体积为
(3)对所配制的稀盐酸进行测定,发现其浓度小于1mol•L﹣1,引起误差的原因可能是
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
III.丙同学对课堂上学到的胶体的相关知识产生了浓厚兴趣。他将乙同学配制好的盐酸溶液加入到鸡蛋清溶液中,发现出现絮状沉淀,此现象称为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室用固体烧碱配制500mL0.1000mol/L的NaOH溶液。
(1)需称量___ g烧碱,应放在_______ (填仪器名称)中称量。
(2)配制过程中,不需要的仪器(填写代号)_______ 。
a、烧杯 b、量筒 c、玻璃棒 d、500mL容量瓶 e、漏斗 f、胶头滴管
(3)根据实验需要和(2)所列仪器判断,完成实验还缺少的仪器是____ 。
(4)步骤B通常称为转移,步骤A通常称为________ 。
(5)将上述实验步骤A到F按实验过程先后次序排列_______ 。

(1)需称量
(2)配制过程中,不需要的仪器(填写代号)
a、烧杯 b、量筒 c、玻璃棒 d、500mL容量瓶 e、漏斗 f、胶头滴管
(3)根据实验需要和(2)所列仪器判断,完成实验还缺少的仪器是
(4)步骤B通常称为转移,步骤A通常称为
(5)将上述实验步骤A到F按实验过程先后次序排列
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某种胃药的有效成分为碳酸钙,测定其中碳酸钙含量的操作如下(设该药片中的其他成分不与盐酸或者氢氧化钠反应);
①配制0.10mol/L稀盐酸和0.10mol/L NaOH溶液;
②向一粒研碎后的药片(0.10g)中加入20.00mL蒸馏水;
③用0.10mol/L NaOH溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积;
④加入25.00mL0.10mol/L稀盐酸。
请回答下列问题。
(1)正确的操作顺序是(填序号)___________ 。
(2)药片需先研碎的目的是___________ 。
(3)为减少误差,该测定实验共进行了4次。实验室现有50mL、100mL、250mL、500mL四种规格的容量瓶,则配制盐酸应选用的容量瓶的规格为___________ ,理由是___________ 。
(4)某同学4次测定所消耗的 溶液的体积如下:
溶液的体积如下:
根据该同学的实验数据,计算该胃药中碳酸钙的质量分数为___________ 。(写出必要的计算过程)。
①配制0.10mol/L稀盐酸和0.10mol/L NaOH溶液;
②向一粒研碎后的药片(0.10g)中加入20.00mL蒸馏水;
③用0.10mol/L NaOH溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积;
④加入25.00mL0.10mol/L稀盐酸。
请回答下列问题。
(1)正确的操作顺序是(填序号)
(2)药片需先研碎的目的是
(3)为减少误差,该测定实验共进行了4次。实验室现有50mL、100mL、250mL、500mL四种规格的容量瓶,则配制盐酸应选用的容量瓶的规格为
(4)某同学4次测定所消耗的
 溶液的体积如下:
溶液的体积如下:| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V[NaOH溶液]mL | 13.00 | 12.90 | 14.60 | 13.10 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】据下图的转化关系及现象回答下列问题。

(1)固体X的名称______ ;A的化学式____________ 。
(2)写出反应①②③④的化学方程式
①____________________________________________________________________ ;
②____________________________________________________________________ ;
③___________________________________________________________________ ;
④___________________________________________________________________ 。

(1)固体X的名称
(2)写出反应①②③④的化学方程式
①
②
③
④
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D是四种常见的单质,A、B为金属,C、D常温下是气体,且D为黄绿色气体。甲、乙、丙为常见的化合物,甲是黑色且具有磁性的物质。它们之间的转化关系如下图所示:

请回答下列问题:
(1)B与甲反应的化学方程式是__________________________ ,该反应中如得到1molA则反应中转移的电子为_________ mol。
(2)常温下,将A或B的单质放入浓硫酸或浓硝酸中,是否溶解?___________ (填“是”或“否”)。
(3)将丙溶于水配成溶液,检验丙中阳离子的方法是______________________ 。
(4)写出A与水蒸气反应生成C和甲的化学方程式____________________ 。
(5)将A、B两种金属按一定的质量比组成混合物。取一定质量的该混合物,向其中加入足量的NaOH溶液,生成气体的体积在标准状况下为n L,B与NaOH溶液反应的离子方程式是______________ ,混合物中B的物质的量为______________ mol(用含字母的分数式表示)。、

请回答下列问题:
(1)B与甲反应的化学方程式是
(2)常温下,将A或B的单质放入浓硫酸或浓硝酸中,是否溶解?
(3)将丙溶于水配成溶液,检验丙中阳离子的方法是
(4)写出A与水蒸气反应生成C和甲的化学方程式
(5)将A、B两种金属按一定的质量比组成混合物。取一定质量的该混合物,向其中加入足量的NaOH溶液,生成气体的体积在标准状况下为n L,B与NaOH溶液反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色实验均为黄色。
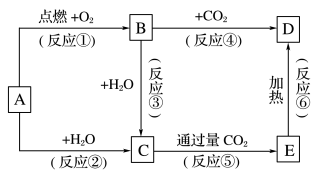
请填写下列空白:
(1)写出下列化学式:A____________ ,D____________
(2)以上反应中,不属于氧化还原反应的有________________ (填序号)。
(3)完成方程式

请填写下列空白:
(1)写出下列化学式:A
(2)以上反应中,不属于氧化还原反应的有
(3)完成方程式
①A→C反应的离子方程式:
②B→D反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】侯氏制碱法的主要产品是Na2CO3(可能含有碳酸氢钠杂质)。某兴趣小组为测定制得纯碱样品中碳酸钠的质量分数,设计了如下实验方案:
方案一:采用如图所示实验装置,加热mg样品至恒重,测定相关数据。

方案二:称量3.600g样品,配制成100mL溶液;取其中20.00mL溶液置于锥形瓶中,滴加甲基橙作指示剂;用1moL·L-1的盐酸标准溶液滴定,达滴定终点时消耗盐酸体积为13.00mL。
回答下列问题:
(1)方案一中:
①X气体选择N2、不选空气的原因是___________ 。
②仪器a的名称是___________ 。
③实验需先通一段时间X气体,再加热样品。若要准确计算样品中碳酸钠的质量分数,还需要提供一个数据,它可以是___________ (填字母)。
A.加热前后,甲装置的质量变化
B.加热前后,乙、丙装置的质量变化总和
C.加热前后,a处的质量变化
(2)方案二中:
①发生反应的化学程式是___________ (写出一种即可)。
②根据该实验方案计算样品中碳酸钠的质量分数________ (写出计算过程,结果保留一位小数)。
方案一:采用如图所示实验装置,加热mg样品至恒重,测定相关数据。

方案二:称量3.600g样品,配制成100mL溶液;取其中20.00mL溶液置于锥形瓶中,滴加甲基橙作指示剂;用1moL·L-1的盐酸标准溶液滴定,达滴定终点时消耗盐酸体积为13.00mL。
回答下列问题:
(1)方案一中:
①X气体选择N2、不选空气的原因是
②仪器a的名称是
③实验需先通一段时间X气体,再加热样品。若要准确计算样品中碳酸钠的质量分数,还需要提供一个数据,它可以是
A.加热前后,甲装置的质量变化
B.加热前后,乙、丙装置的质量变化总和
C.加热前后,a处的质量变化
(2)方案二中:
①发生反应的化学程式是
②根据该实验方案计算样品中碳酸钠的质量分数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】为测定出Na2CO3和NaHCO3的混合物中Na2CO3质量分数,请你完善下列方案。
方案一:称取一定质量样品,置于坩埚中高温加热至恒重后冷却,称量剩余固体质量,进行计算。
(1)发生反应的化学方程式为:_______
(2)实验中需加热至恒重的目的是:_______
方案二:按如图所示装置进行实验
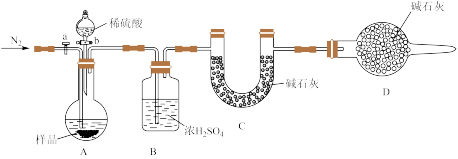
(3)B装置的作用是_______
(4)反应完毕后还要通一段时间N2的目的是_______
(5)实验前称取混合物样品19.00 g,实验后测得C装置增重8.80 g,则样品中碳酸钠的质量分数为_______ %(保留小数点后两位)。
方案一:称取一定质量样品,置于坩埚中高温加热至恒重后冷却,称量剩余固体质量,进行计算。
(1)发生反应的化学方程式为:
(2)实验中需加热至恒重的目的是:
方案二:按如图所示装置进行实验

(3)B装置的作用是
(4)反应完毕后还要通一段时间N2的目的是
(5)实验前称取混合物样品19.00 g,实验后测得C装置增重8.80 g,则样品中碳酸钠的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】现有一不纯的小苏打样品(含杂质 、
、 ),为测定
),为测定 的质量分数,设计如图所示的实验装置(夹持仪器未画出)。
的质量分数,设计如图所示的实验装置(夹持仪器未画出)。
说明:碱石灰为 、
、 的混合物,常用作干燥剂,也可以吸收
的混合物,常用作干燥剂,也可以吸收 气体。
气体。

实验步骤如下:
①按图组装好实验装置并检查气密性。
②称取一定质量的样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞 、
、 ,关闭
,关闭 ,缓缓鼓入空气数分钟。
,缓缓鼓入空气数分钟。
④关闭活塞 、
、 ,打开
,打开 ,点燃酒精灯加热至不再产生气体。
,点燃酒精灯加热至不再产生气体。
⑤打开活塞 ,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
回答下列问题:
(1)仪器E的名称是___________ ,其中盛放的药品是___________ ;若无该装置,则会导致测得的 的质量分数
的质量分数__________ 。(填“偏大”“偏小”或“无影响”)
(2)步骤③的目的是_____________________________________________________ 。
(3)装置B中发生反应的化学方程式为___________________ ,________________ 。
(4)若实验中称取样品的质量为50.0g,反应后C、D装置增加的质量分别为12.6g、8.8g,则混合物中 的质量分数为
的质量分数为________ ,杂质 的质量为
的质量为________ g。
 、
、 ),为测定
),为测定 的质量分数,设计如图所示的实验装置(夹持仪器未画出)。
的质量分数,设计如图所示的实验装置(夹持仪器未画出)。说明:碱石灰为
 、
、 的混合物,常用作干燥剂,也可以吸收
的混合物,常用作干燥剂,也可以吸收 气体。
气体。
实验步骤如下:
①按图组装好实验装置并检查气密性。
②称取一定质量的样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞
 、
、 ,关闭
,关闭 ,缓缓鼓入空气数分钟。
,缓缓鼓入空气数分钟。④关闭活塞
 、
、 ,打开
,打开 ,点燃酒精灯加热至不再产生气体。
,点燃酒精灯加热至不再产生气体。⑤打开活塞
 ,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。回答下列问题:
(1)仪器E的名称是
 的质量分数
的质量分数(2)步骤③的目的是
(3)装置B中发生反应的化学方程式为
(4)若实验中称取样品的质量为50.0g,反应后C、D装置增加的质量分别为12.6g、8.8g,则混合物中
 的质量分数为
的质量分数为 的质量为
的质量为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】立方晶系二元合金
有一立方晶系二元合金,单胞参数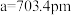 。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体
。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体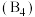 ,已知晶胞中
,已知晶胞中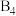 的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
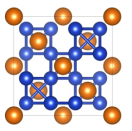
(1)写出二元合金的化学式_______ 。
(2)已知金属A和B的原子量分别为24.31和53.55,计算合金的理论密度_______ 。
(3)晶胞的单位点阵型式_______ 。
(4)实际上,大部分该类结构二元合金的原子半径比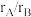 处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和
处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和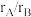 值
值_______ 、_______ 。
有一立方晶系二元合金,单胞参数
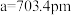 。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体
。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体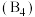 ,已知晶胞中
,已知晶胞中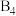 的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
(1)写出二元合金的化学式
(2)已知金属A和B的原子量分别为24.31和53.55,计算合金的理论密度
(3)晶胞的单位点阵型式
(4)实际上,大部分该类结构二元合金的原子半径比
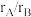 处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和
处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和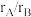 值
值
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】分现有某铁碳合金(铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究。

(1)A中铁与浓硫酸发生反应的化学方程式是___________ ,反应中浓硫酸表现出的性质是___________ 、___________ 。
(2)连接好装置后,首先应进行的操作是___________ 。
(3)装置C溶液反应时,体现气体的___________ 性。
(4)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g。铁碳合金中铁的质量分数为___________ (写表达式).
(5)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数会偏低,原因是空气中CO2、H2O进入E管使b增大.你认为改进的方法是___________ 。
(6)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分数还会偏高.你认为其中的原因是___________ 。

(1)A中铁与浓硫酸发生反应的化学方程式是
(2)连接好装置后,首先应进行的操作是
(3)装置C溶液反应时,体现气体的
(4)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g。铁碳合金中铁的质量分数为
(5)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数会偏低,原因是空气中CO2、H2O进入E管使b增大.你认为改进的方法是
(6)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分数还会偏高.你认为其中的原因是
您最近一年使用:0次




