立方晶系二元合金
有一立方晶系二元合金,单胞参数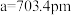 。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体
。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体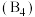 ,已知晶胞中
,已知晶胞中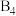 的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
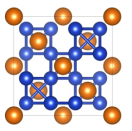
(1)写出二元合金的化学式_______ 。
(2)已知金属A和B的原子量分别为24.31和53.55,计算合金的理论密度_______ 。
(3)晶胞的单位点阵型式_______ 。
(4)实际上,大部分该类结构二元合金的原子半径比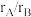 处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和
处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和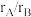 值
值_______ 、_______ 。
有一立方晶系二元合金,单胞参数
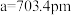 。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体
。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体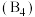 ,已知晶胞中
,已知晶胞中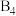 的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
(1)写出二元合金的化学式
(2)已知金属A和B的原子量分别为24.31和53.55,计算合金的理论密度
(3)晶胞的单位点阵型式
(4)实际上,大部分该类结构二元合金的原子半径比
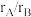 处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和
处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和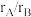 值
值
更新时间:2022-10-30 22:55:58
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】翡翠是玉石中的一种,其主要成分为硅酸铝钠NaAl(Si2O6),常含微量Cr、Ni、Mn、Mg、Fe等元素。回答下列问题:
(1)Cr3+电子排布式为______________________ ,基态Si原子中,电子占据的最高能层符号为______________________ 。
(2)翡翠中主要成分为硅酸铝钠,四种元素的第一电离能由大到小的顺序___________ 。
(3)锰的一种化合物的化学式为Mn(BH4)2(THF)3,THT的结构简式如图所示:
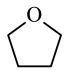
①THF中C原子的杂化轨道类型为___________ ,②BH4-的空间构型为___________
③NaBH4所含化学键类型有_____________
A、离子键 B、共价键 C、氢键 D、配位键
(4)MnO的熔点(1660℃)比MnS的熔点(1610℃)高,原因______________________ 。
(5)Ni可以形成多种氧化物,其中一种NixO晶体的晶胞结构为NaCl型,由于晶体缺陷,x为0.88,且晶体中Ni的存在形式为Ni2+、Ni3+,则晶体中N i2+和Ni3+最简整数比为___________ ,该晶体的晶胞参数为428pm,则晶体密度为___________ g·cm-3(NA表示阿伏伽德罗常数的值,列出表达式即可)
(1)Cr3+电子排布式为
(2)翡翠中主要成分为硅酸铝钠,四种元素的第一电离能由大到小的顺序
(3)锰的一种化合物的化学式为Mn(BH4)2(THF)3,THT的结构简式如图所示:

①THF中C原子的杂化轨道类型为
③NaBH4所含化学键类型有
A、离子键 B、共价键 C、氢键 D、配位键
(4)MnO的熔点(1660℃)比MnS的熔点(1610℃)高,原因
(5)Ni可以形成多种氧化物,其中一种NixO晶体的晶胞结构为NaCl型,由于晶体缺陷,x为0.88,且晶体中Ni的存在形式为Ni2+、Ni3+,则晶体中N i2+和Ni3+最简整数比为
您最近一年使用:0次
【推荐2】 、
、 、
、 、
、 组成的化合物
组成的化合物 通过
通过 空位的掺杂可引入载流子诱发超导,
空位的掺杂可引入载流子诱发超导, 的晶体结构和氧原子沿
的晶体结构和氧原子沿 轴的投影如图所示。回答下列问题:
轴的投影如图所示。回答下列问题: 原子中
原子中 层上的电子空间运动状态有
层上的电子空间运动状态有___________ 种;O、S、Cl电负性由大到小的顺序是___________ 。
(2)氮族元素氢化物(MH3)NH3、PH3、AsH3、SbH3、BiH3键角H-M-H最大的是___________ (填化学式);键长 最长的是
最长的是___________ (填化学式)。已知:配离子的颜色与 电子跃迁的分裂能大小有关,1个电子从较低的
电子跃迁的分裂能大小有关,1个电子从较低的 轨道跃迁到较高能量的
轨道跃迁到较高能量的 轨道所需的能量为
轨道所需的能量为 的分裂能,用符号
的分裂能,用符号 表示。分裂能
表示。分裂能
___________  (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是___________ 。
(3)A属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为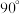 ,该晶胞中Bi原子的配位数为
,该晶胞中Bi原子的配位数为___________ 。若阿伏加德罗常数的值为 ,化合物
,化合物 的密度
的密度
___________  (用含
(用含 的代数式表示)。
的代数式表示)。
 、
、 、
、 、
、 组成的化合物
组成的化合物 通过
通过 空位的掺杂可引入载流子诱发超导,
空位的掺杂可引入载流子诱发超导, 的晶体结构和氧原子沿
的晶体结构和氧原子沿 轴的投影如图所示。回答下列问题:
轴的投影如图所示。回答下列问题: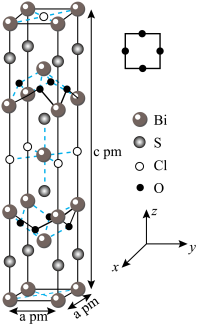
 原子中
原子中 层上的电子空间运动状态有
层上的电子空间运动状态有(2)氮族元素氢化物(MH3)NH3、PH3、AsH3、SbH3、BiH3键角H-M-H最大的是
 最长的是
最长的是 电子跃迁的分裂能大小有关,1个电子从较低的
电子跃迁的分裂能大小有关,1个电子从较低的 轨道跃迁到较高能量的
轨道跃迁到较高能量的 轨道所需的能量为
轨道所需的能量为 的分裂能,用符号
的分裂能,用符号 表示。分裂能
表示。分裂能
 (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是(3)A属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
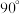 ,该晶胞中Bi原子的配位数为
,该晶胞中Bi原子的配位数为 ,化合物
,化合物 的密度
的密度
 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】AlN 氮化铝是重要的半导体材料,Ga(镓)、P、As(砷)都是形成化合物半导体材料的重要元素。回答下列问题:
(1)As基态原子的电子占据了______ 个能层,最高能级的电子排布式为______ 。和As位于同一周期,且未成对电子数也相同的元素还有______ 种。
(2)元素周期表中,与P紧邻的4种元素中电负性最大的是______ (填元素符号)。Si、P、S三种元素的 第一电离能由大到小的顺序是______ 。
(3)NH3、PH3、AsH3三者的沸点由高到低的顺序是______ 。原因是______ 。
(4)白磷是由P4分子形成的分子晶体,P4分子呈正四面体结构,P原子位于正四面体的四个顶点,则P原子的杂化形式为_____ ,白磷易溶于CS2,难溶于水,原因是__________________ 。
(5)采用GaxIn1-xAs(镓铟砷)等材料,可提高太阳能电池的效率。GaxIn1-xAs立方体形晶胞中每个顶点和面心都有一个原子,晶胞内部有4 个原子,则该晶胞中含有_________ 个砷原子。
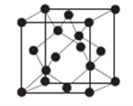
(6)AlN晶体的晶胞结构与金刚石相似(见下图),设晶胞的边长为ɑ pm,NA表示阿伏伽德罗常数,则该晶体的密度为__________ g·cm-3。
(1)As基态原子的电子占据了
(2)元素周期表中,与P紧邻的4种元素中电负性最大的是
(3)NH3、PH3、AsH3三者的沸点由高到低的顺序是
(4)白磷是由P4分子形成的分子晶体,P4分子呈正四面体结构,P原子位于正四面体的四个顶点,则P原子的杂化形式为
(5)采用GaxIn1-xAs(镓铟砷)等材料,可提高太阳能电池的效率。GaxIn1-xAs立方体形晶胞中每个顶点和面心都有一个原子,晶胞内部有4 个原子,则该晶胞中含有
(6)AlN晶体的晶胞结构与金刚石相似(见下图),设晶胞的边长为ɑ pm,NA表示阿伏伽德罗常数,则该晶体的密度为

您最近一年使用:0次
【推荐1】按要求回答下列问题:
(1)Fe单质的晶体在不同温度下有两种堆积方式,分别如图1、如图2所示。面心立方晶胞和体心立方晶胞的边长分别为a、b,则铁单质的面心立方晶胞和体心立方晶胞的密度之比为________ ,铁原子的配位数之比为________ 。

(2)Mg为六方最密堆积,其晶胞结构如图所示,若在晶胞中建立如图3所示的坐标系,以A为坐标原点,把晶胞的底边边长视作单位长度1,则C点的坐标:________ 。
(3)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图5所示,则铁镁合金的化学式为________ 。若该晶胞的边长为d nm,则该合金的密度为________ g·cm-3(列出计算式即可,用NA表示阿伏加 德罗常数的值)。
(1)Fe单质的晶体在不同温度下有两种堆积方式,分别如图1、如图2所示。面心立方晶胞和体心立方晶胞的边长分别为a、b,则铁单质的面心立方晶胞和体心立方晶胞的密度之比为

(2)Mg为六方最密堆积,其晶胞结构如图所示,若在晶胞中建立如图3所示的坐标系,以A为坐标原点,把晶胞的底边边长视作单位长度1,则C点的坐标:
(3)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图5所示,则铁镁合金的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】磷元素的化合物在科学研究和工业生产中有许多重要用途。回答下列问题:
(1)下列状态的P中,电离最外层一个电子所需能量最小的是_______(填标号)。
(2)白磷在空气中缓慢氧化生成P4O6,P4O6的结构如图1所示。P4O6中氧原子的杂化轨道类型为_______ ,每个P4O6分子中含孤电子对的数目为_______ 。
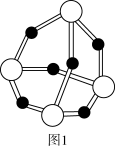
(3)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图2所示。在一个晶胞中磷原子空间堆积方式为_______ ,磷原子的配位数为_______ 。
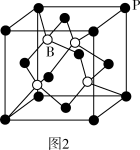
(4)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的空间构型为_______ 。
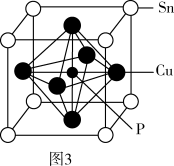
(5)磷青铜晶体的晶胞结构如图3所示,该晶体中P原子位于由铜原子形成的_______ 的空隙中。若晶体密度为ag·cm-3,P原子与最近的Cu原子的核间距为_______ nm(用含NA的代数式表示,NA为阿伏加德罗常数的值)。
(1)下列状态的P中,电离最外层一个电子所需能量最小的是_______(填标号)。
A.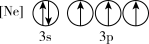 | B.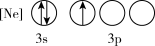 |
C.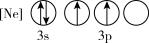 | D.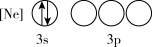 |

(3)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图2所示。在一个晶胞中磷原子空间堆积方式为

(4)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的空间构型为
(5)磷青铜晶体的晶胞结构如图3所示,该晶体中P原子位于由铜原子形成的

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(1)钛镁合金是制造高性能飞机的重要材料。金属钛、镁均采用六方最密堆积,下列说法正确的是_____ (填序号)。
A.钛镁合金用于制造高性能飞机主要是由于它们的价格昂贵,制造出的飞机能卖好价钱
B.钛、镁金属晶体中,其配位数均为12
C.金属钛的熔点(1668℃)很高,与金属键无关
(2)钙钛型复合氧化物可用于制造航母中的热敏传感器,其晶胞结构如图所示,其中A为晶胞的顶点,A可以是Ca、Sr、Ba或Pb,当B是V、Cr、Mn或Fe时,这种化合物具有很好的电学性能。下列说法正确的是______ (填序号)。
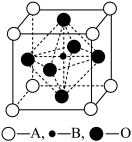
A.金属Ca、Sr、Ba采用体心立方密堆积
B.用A、B、O表示的钙钛型复合氧化物晶体的化学式可表示为ABO3
C.在制造Fe薄片时,金属键完全断裂
D.V、Cr、Mn、Fe晶体中均存在金属阳离子和阴离子
(3)辽宁号航母飞行甲板等都是由铁及其合金制造的。铁有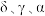 三种同素异形体,其晶胞结构如图所示。
三种同素异形体,其晶胞结构如图所示。
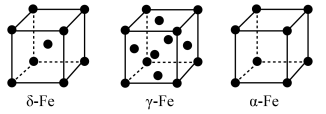
① 晶胞中含有的铁原子数为
晶胞中含有的铁原子数为___________ 。
②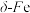 、
、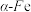 两种晶体中铁原子的配位数之比为
两种晶体中铁原子的配位数之比为___________ 。
③若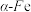 晶胞的边长为a cm,
晶胞的边长为a cm,  晶胞的边长为b cm,则两种晶体的密度之比为
晶胞的边长为b cm,则两种晶体的密度之比为___________ 。
A.钛镁合金用于制造高性能飞机主要是由于它们的价格昂贵,制造出的飞机能卖好价钱
B.钛、镁金属晶体中,其配位数均为12
C.金属钛的熔点(1668℃)很高,与金属键无关
(2)钙钛型复合氧化物可用于制造航母中的热敏传感器,其晶胞结构如图所示,其中A为晶胞的顶点,A可以是Ca、Sr、Ba或Pb,当B是V、Cr、Mn或Fe时,这种化合物具有很好的电学性能。下列说法正确的是

A.金属Ca、Sr、Ba采用体心立方密堆积
B.用A、B、O表示的钙钛型复合氧化物晶体的化学式可表示为ABO3
C.在制造Fe薄片时,金属键完全断裂
D.V、Cr、Mn、Fe晶体中均存在金属阳离子和阴离子
(3)辽宁号航母飞行甲板等都是由铁及其合金制造的。铁有
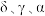 三种同素异形体,其晶胞结构如图所示。
三种同素异形体,其晶胞结构如图所示。
①
 晶胞中含有的铁原子数为
晶胞中含有的铁原子数为②
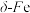 、
、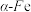 两种晶体中铁原子的配位数之比为
两种晶体中铁原子的配位数之比为③若
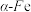 晶胞的边长为a cm,
晶胞的边长为a cm,  晶胞的边长为b cm,则两种晶体的密度之比为
晶胞的边长为b cm,则两种晶体的密度之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】分现有某铁碳合金(铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究。

(1)A中铁与浓硫酸发生反应的化学方程式是___________ ,反应中浓硫酸表现出的性质是___________ 、___________ 。
(2)连接好装置后,首先应进行的操作是___________ 。
(3)装置C溶液反应时,体现气体的___________ 性。
(4)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g。铁碳合金中铁的质量分数为___________ (写表达式).
(5)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数会偏低,原因是空气中CO2、H2O进入E管使b增大.你认为改进的方法是___________ 。
(6)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分数还会偏高.你认为其中的原因是___________ 。

(1)A中铁与浓硫酸发生反应的化学方程式是
(2)连接好装置后,首先应进行的操作是
(3)装置C溶液反应时,体现气体的
(4)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g。铁碳合金中铁的质量分数为
(5)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数会偏低,原因是空气中CO2、H2O进入E管使b增大.你认为改进的方法是
(6)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分数还会偏高.你认为其中的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某学习小组用如图装置测定锌铜合金中铜的质量分数:


(1)实验前,先将铜合金在稀酸中浸泡片刻,目的是_______ ;
(2)实验开始首先应对装置进行气密性检查,简述检查方法:_______ ;
(3)为了较准确地测量气体体积,反应后量气管读数前,应注意:_______ ;
(4)查阅数据获知在实验条件下,气体摩尔体积为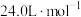 ,若样品质量为0.200g,测得氢气体积为40.00mL,合金中铜的质量分数为
,若样品质量为0.200g,测得氢气体积为40.00mL,合金中铜的质量分数为_______ (保留3位有效数字);
(5)下列哪些因素会造成合金中铜的质量分数偏低_______ 。
a.稀硫酸的量不足 b.将稀硫酸替换为盐酸
c.量气管末读数时仰视刻度线 d.末读数时水准管的液面高于量气管的液面


(1)实验前,先将铜合金在稀酸中浸泡片刻,目的是
(2)实验开始首先应对装置进行气密性检查,简述检查方法:
(3)为了较准确地测量气体体积,反应后量气管读数前,应注意:
(4)查阅数据获知在实验条件下,气体摩尔体积为
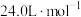 ,若样品质量为0.200g,测得氢气体积为40.00mL,合金中铜的质量分数为
,若样品质量为0.200g,测得氢气体积为40.00mL,合金中铜的质量分数为(5)下列哪些因素会造成合金中铜的质量分数偏低
a.稀硫酸的量不足 b.将稀硫酸替换为盐酸
c.量气管末读数时仰视刻度线 d.末读数时水准管的液面高于量气管的液面
您最近一年使用:0次
【推荐1】填写下列空白:
(1)某金属既有ccp堆积,又有hcp堆积的晶体。若ccp堆积的晶胞参数为ac,则hcp堆积的晶胞参数为:a=__________ ac,c=_________ ac。
(2)一些金属间化合物结构可看作由CsCl结构堆叠而成,例如Cr2Al。试分别以Cr原子和Al原子为顶点,画出两种晶胞___________ ,写出晶胞中原子的分数坐标___________ 、___________ 。
(1)某金属既有ccp堆积,又有hcp堆积的晶体。若ccp堆积的晶胞参数为ac,则hcp堆积的晶胞参数为:a=
(2)一些金属间化合物结构可看作由CsCl结构堆叠而成,例如Cr2Al。试分别以Cr原子和Al原子为顶点,画出两种晶胞
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】某单质M是一种常见金属,它在日常生活中有极其重要的作用,如电线、合金等。将M溶于浓硝酸得含A的绿色水溶液。A受热分解得到黑色固体B, B溶于稀硫酸后经蒸发、浓缩、冷却得到蓝色晶体C.将一定量的C溶解并分成两份,一 份加入少量氨水,生成浅蓝色沉淀D,已知D中M元素的百分含量为49.42%,硫为12.47%,氧为37.33%;另一份加入少量NaCN溶液(氰根离子是一种类卤素) ,产生一种棕黄色沉淀E和气体F,再往沉淀E中加入过量NaCN溶液,生成含G的溶液,该溶液是用作电镀M的电镀液,污染大。
(1)写出以下物质的化学式: B___________ ,C ___________ , D___________ , G ___________ ;
(2)写出C →E的离子方程式:___________ 。
(3)A的熔点较低,真空时易升华,这与一般离子晶体的性质不相符,简述理由:______ 。
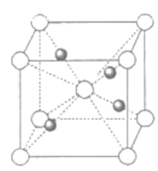
(4)M在一定温度下与氧作用得到固体H。H属立方晶系,其正当晶胞如图所示,密度为6.00 g·cm-3.通过计算给出M-O的距离______ 。
(1)写出以下物质的化学式: B
(2)写出C →E的离子方程式:
(3)A的熔点较低,真空时易升华,这与一般离子晶体的性质不相符,简述理由:
(4)M在一定温度下与氧作用得到固体H。H属立方晶系,其正当晶胞如图所示,密度为6.00 g·cm-3.通过计算给出M-O的距离

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】C60固体可以看作由C60分子密堆积形成的。C60固体中,有一种属面心立方最密堆积。其晶胞边长为1417 pm,两个最邻近分子之间的距离为296 pm。C固体暴露到碱金属蒸气中,形成通式为MnC60的一系列化合物。请回答下列问题:
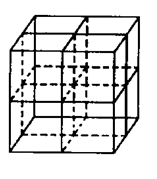
(1)面心立方最密堆积的C60 固体的密度为_______ g/cm3 ;C60固体中一个C60分子的半径为_______ pm( 视C60分子为球体)。
(2)有一种K6C60化合物,属体心立方晶系。
①以“ ”表示离子C
”表示离子C ,以“×”表示离子K+ ,试在图中画出K6C60化合物的晶胞
,以“×”表示离子K+ ,试在图中画出K6C60化合物的晶胞_______ 。
②K+和C 的配位数分别为
的配位数分别为_______ 、_______ 。
(3)C60分子是形如球状的多面体,该结构的建立基于以下考虑:①C60分子中每个碳原只跟相邻的3个碳原子形成化学键;②C60分子只含有五边形和六边形;③多面体的顶点数、面数和棱边数的关系遵循欧拉定理。
①固体C60与金刚石相比较,熔点较高者应是_______ , 理由是:_______ 。
②试估计C60跟F2在 一定条件下能否发生反应生成C60F60(填“可能”或“不可能”)_______ ,理由是:_______ 。
③C60分子中所含五边形数为_______ ,六边形数为_______ 。

(1)面心立方最密堆积的C60 固体的密度为
(2)有一种K6C60化合物,属体心立方晶系。
①以“
 ”表示离子C
”表示离子C ,以“×”表示离子K+ ,试在图中画出K6C60化合物的晶胞
,以“×”表示离子K+ ,试在图中画出K6C60化合物的晶胞②K+和C
 的配位数分别为
的配位数分别为(3)C60分子是形如球状的多面体,该结构的建立基于以下考虑:①C60分子中每个碳原只跟相邻的3个碳原子形成化学键;②C60分子只含有五边形和六边形;③多面体的顶点数、面数和棱边数的关系遵循欧拉定理。
①固体C60与金刚石相比较,熔点较高者应是
②试估计C60跟F2在 一定条件下能否发生反应生成C60F60(填“可能”或“不可能”)
③C60分子中所含五边形数为
您最近一年使用:0次




