填写下列空白:
(1)某金属既有ccp堆积,又有hcp堆积的晶体。若ccp堆积的晶胞参数为ac,则hcp堆积的晶胞参数为:a=__________ ac,c=_________ ac。
(2)一些金属间化合物结构可看作由CsCl结构堆叠而成,例如Cr2Al。试分别以Cr原子和Al原子为顶点,画出两种晶胞___________ ,写出晶胞中原子的分数坐标___________ 、___________ 。
(1)某金属既有ccp堆积,又有hcp堆积的晶体。若ccp堆积的晶胞参数为ac,则hcp堆积的晶胞参数为:a=
(2)一些金属间化合物结构可看作由CsCl结构堆叠而成,例如Cr2Al。试分别以Cr原子和Al原子为顶点,画出两种晶胞
更新时间:2021-08-12 21:53:09
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】硅材料和铝材料在生产生活中应用广泛。回答下列问题:
(1)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:a.([Ne]3s23p2)、b.([Ne]3s23p1)、c.([Ne]3s23p14s1),半径由大到小的顺序为_______ (填标号);第三周期元素中,第一电离能介于Al和P之间的元素有_______ 种。
(2)N(SiH3)3是一种高介电常数材料。已知:N(SiH3)3中Si-N-Si键角120°,N(CH3)3中C-N-C键角111°。共价键的极性Si-N_______ C-N(填“>”、“=”或“<”)。下列划线原子与N(SiH3)3中N原子杂化类型相同的是_______ (填标号)。
A.Al(OCH3)3 B.NH3BH3 C.N(CH3)3 D.NH4NO3
(3)铝硼中间合金在铝生产中应用广泛。金属铝熔点为660.3℃,晶体硼熔点为2300℃,晶体硼熔点高于铝的原因是_______ 。
(4)已知合金Na2AlAu3的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入Au3Al四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。
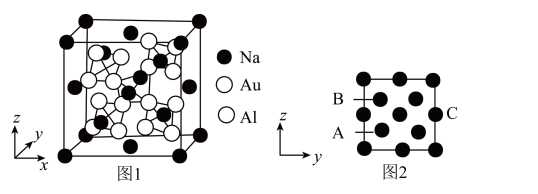
每个Na周围距离其最近的Na有_______ 个;以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点的分数坐标为( ,
, ,
, ),则B点的分数坐标为
),则B点的分数坐标为_______ ;设NA为阿伏加德罗常数的值,Na2AlAu3的摩尔质量为Mg•mol-1,晶体的密度为ρg•cm-3,则A、C两原子间的距离为_______ pm(列出计算表达式)。
(1)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:a.([Ne]3s23p2)、b.([Ne]3s23p1)、c.([Ne]3s23p14s1),半径由大到小的顺序为
(2)N(SiH3)3是一种高介电常数材料。已知:N(SiH3)3中Si-N-Si键角120°,N(CH3)3中C-N-C键角111°。共价键的极性Si-N
A.Al(OCH3)3 B.NH3BH3 C.N(CH3)3 D.NH4NO3
(3)铝硼中间合金在铝生产中应用广泛。金属铝熔点为660.3℃,晶体硼熔点为2300℃,晶体硼熔点高于铝的原因是
(4)已知合金Na2AlAu3的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入Au3Al四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。

每个Na周围距离其最近的Na有
 ,
, ,
, ),则B点的分数坐标为
),则B点的分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铁被誉为“第一金属”,铁及其化合物广泛应用于生活、生产、国防等领域。
(1)基态Fe原子的价层电子的电子排布图为_______ ;其最外层电子的电子云形状为_______ 。
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为_______ 晶体。
(3) 俗称摩尔盐,其阴离子的立体构型名称为
俗称摩尔盐,其阴离子的立体构型名称为_______ 。写出一种与 互为等电子体的分子的电子式:
互为等电子体的分子的电子式:_______ 。
(4) 可用作催化剂、汽油抗爆剂等,其分子中
可用作催化剂、汽油抗爆剂等,其分子中 键和
键和 键的数目之比为
键的数目之比为_______ 。
(5)铁晶体有面心立方最密堆积和体心立方堆积两种晶体,这两种晶体铁原子的配位数之比为_______ 。
(6)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为_______ 。

(1)基态Fe原子的价层电子的电子排布图为
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为
(3)
 俗称摩尔盐,其阴离子的立体构型名称为
俗称摩尔盐,其阴离子的立体构型名称为 互为等电子体的分子的电子式:
互为等电子体的分子的电子式:(4)
 可用作催化剂、汽油抗爆剂等,其分子中
可用作催化剂、汽油抗爆剂等,其分子中 键和
键和 键的数目之比为
键的数目之比为(5)铁晶体有面心立方最密堆积和体心立方堆积两种晶体,这两种晶体铁原子的配位数之比为
(6)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】选修已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数是D的2倍。F元素在地壳中含量位于金属元素的第二位。回答下列问题:
(1)F元素价层电子排布式为_______________________ 。
(2)关于B2A2的下列说法中正确的是___________
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中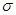 键和
键和 键数目比为1:1
键数目比为1:1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的A—B键属于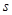 —
— 键
键
(3)B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的结构式为___________________
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能都高的主要原因是
__________________________________________________________________
(5)D的氢化物比E的氢化物沸点高,其主要原因是________________________ ;E的氢化物的价层电子对互斥模型为____________________ ,E原子的杂化方式为__________ 。
(6)F单质的晶体在不同温度下有两种堆积方式,即面心立方堆积和体心立方堆积,其晶胞的棱边长分别为a cm、b cm,则F单质的这两种晶体密度之比为_________ ,F原子的配位数之比为________________ 。
(1)F元素价层电子排布式为
(2)关于B2A2的下列说法中正确的是
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中
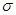 键和
键和 键数目比为1:1
键数目比为1:1C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的A—B键属于
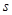 —
— 键
键(3)B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的结构式为
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能都高的主要原因是
(5)D的氢化物比E的氢化物沸点高,其主要原因是
(6)F单质的晶体在不同温度下有两种堆积方式,即面心立方堆积和体心立方堆积,其晶胞的棱边长分别为a cm、b cm,则F单质的这两种晶体密度之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】现有七种元素A、B、C、D、E、F、G,其中A、B、C为三个不同周期的短周期元素,E、F、G为第四周期元素。请根据下列相关信息,回答问题。
(1)C基态原子中能量最高的电子,其电子云在空间有___________ 个方向,C简单离子核外有___________ 种运动状态不同的电子。
(2)A2B2难溶于CS2,简要说明理由:___________ 。
(3)G的一种氧化物常用于工业生产硫酸的催化剂,已知G在该氧化物中的化合价等于其价电子数,则该氧化物的化学式为___________ ;F晶体的空间堆积方式为___________ 。
(4)ED3分子的VSEPR模型名称为___________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数与s电子数相等 |
| C基态原子的价电子排布为nsn-1npn+1 |
| D的能层数与C相同,且电负性比C大 |
| E元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第五列 |
(1)C基态原子中能量最高的电子,其电子云在空间有
(2)A2B2难溶于CS2,简要说明理由:
(3)G的一种氧化物常用于工业生产硫酸的催化剂,已知G在该氧化物中的化合价等于其价电子数,则该氧化物的化学式为
(4)ED3分子的VSEPR模型名称为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铁元素是最重要的金属元素之一,其不仅是各种钢材的主要成分,很多含铁化合物也具有重要意义。
(1)按照电子排布,可把元素周期表中的元素划分成五个区,铁元素属于_________ 区。
(2)Mn2+在水溶液中难被氧化,而Fe2+则易被氧化为Fe3+ ,请从离子的价电子式角度解释Mn2+与Fe2+还原能力的差别:_________ 。Mn2+的半径_________ Fe3+的半径(填“>”、“<”或“=”)。
(3)金属铁晶体中铁原子采用体心立方堆积,该铁晶体的空间利用率为_________ (用含π的式子表示)。
(4)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。N、H、O三种元素的电负性由大到小的顺序为_________ ;[Fe(SCN)(H2O)5]2+中Fe3+的配位数为_________ ,H2O中氧原子的杂化方式为_________ 。
(5)二茂铁是一种含铁的有机化合物,其化学式为Fe(C5H5)2,可看作是Fe2+离子与两个正五边形的环戊二烯负离子(C5H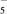 )配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π
)配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则C5H
),则C5H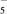 的大π键表示为
的大π键表示为________ 。二茂铁是黄色针状晶体,熔点173 ℃(在100 ℃时开始升华),沸点249 ℃,在水中难溶,但可溶于很多有机溶剂。下列相互作用中,二茂铁晶体中不存在的是________ (填标号)。
A 离子键 B 配位键 C σ 键 D 范德华力
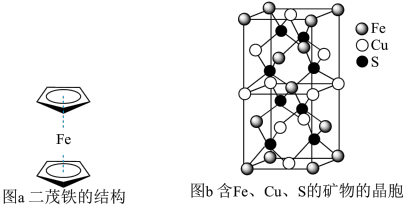
(6)一种含有Fe、Cu、S三种元素的矿物的晶胞(如上图b所示),属于四方晶系(晶胞底面为正方形),晶胞中S原子位于内部,Fe原子位于体心和晶胞表面,Cu原子位于晶胞表面。此矿物的化学式为_________ 。若晶胞的底面边长为A pm,高为C pm,阿伏加 德罗常数为NA,则该晶体的密度为__________ g/cm3(写出表达式)。
(1)按照电子排布,可把元素周期表中的元素划分成五个区,铁元素属于
(2)Mn2+在水溶液中难被氧化,而Fe2+则易被氧化为Fe3+ ,请从离子的价电子式角度解释Mn2+与Fe2+还原能力的差别:
(3)金属铁晶体中铁原子采用体心立方堆积,该铁晶体的空间利用率为
(4)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。N、H、O三种元素的电负性由大到小的顺序为
(5)二茂铁是一种含铁的有机化合物,其化学式为Fe(C5H5)2,可看作是Fe2+离子与两个正五边形的环戊二烯负离子(C5H
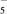 )配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π
)配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则C5H
),则C5H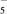 的大π键表示为
的大π键表示为A 离子键 B 配位键 C σ 键 D 范德华力

(6)一种含有Fe、Cu、S三种元素的矿物的晶胞(如上图b所示),属于四方晶系(晶胞底面为正方形),晶胞中S原子位于内部,Fe原子位于体心和晶胞表面,Cu原子位于晶胞表面。此矿物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】新材料技术的发展促进了信息技术和生物技术的革命,并对制造业.物资供应和个人生活方式产生了重大影响。回答下列问题:
(1)近期,PNAS报道了无规超支化聚合物RHP的自愈过程,合成RHP的基础原料为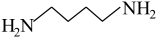 和
和 ,RHP结构表示如下(
,RHP结构表示如下(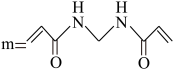 ):
):
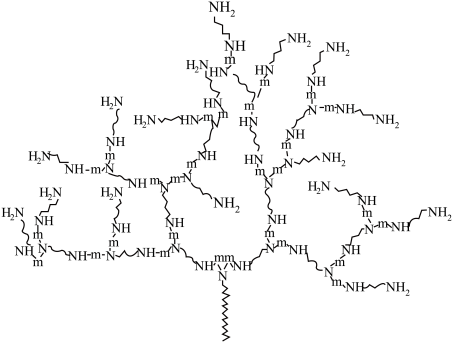
①"自愈”是指材料断裂后,再次接触使其抗拉能力部分恢复,由RHP结构推测其具有自愈能力的主要原因为_________________ 。
②沸点: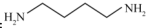
_____  (填“<”或“>”),理由为
(填“<”或“>”),理由为________________________________________ 。
③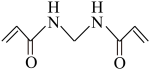 中含有各元素的电负性由小到大的顺序为
中含有各元素的电负性由小到大的顺序为______ ;该物质中,含有σ键和π键数目之比为______________________ 。
(2)纳米材料Cu—SiO2用于催化DMO和氢气反应获得EG,示意图如下:
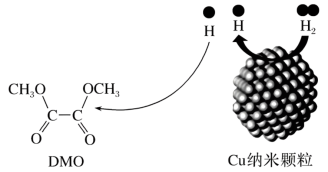
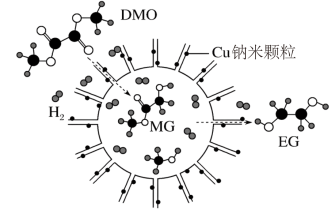
①基态铜原子的核外电子排布式为________ ,基态碳原子核外电子占据的最高能级的电子云形状为_______________ 。
②CuSCN是一种生物防腐涂料,可用CuSO4、NaSCN、Na2SO4作原料,并用EG作分散剂进行制备。与SCN-互为等电子体的分子为____ ; 中心原子的杂化方式为
中心原子的杂化方式为_____________ 。
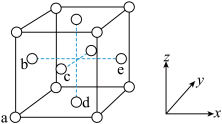
③铜的晶胞如图。它的空间利用率为______ ;原子分数坐标:a为(0,0,0);d分子坐标为( ,
, ,0),则b处的分数坐标为
,0),则b处的分数坐标为____________
(1)近期,PNAS报道了无规超支化聚合物RHP的自愈过程,合成RHP的基础原料为
 和
和 ,RHP结构表示如下(
,RHP结构表示如下( ):
):
①"自愈”是指材料断裂后,再次接触使其抗拉能力部分恢复,由RHP结构推测其具有自愈能力的主要原因为
②沸点:

 (填“<”或“>”),理由为
(填“<”或“>”),理由为③
 中含有各元素的电负性由小到大的顺序为
中含有各元素的电负性由小到大的顺序为(2)纳米材料Cu—SiO2用于催化DMO和氢气反应获得EG,示意图如下:


①基态铜原子的核外电子排布式为
②CuSCN是一种生物防腐涂料,可用CuSO4、NaSCN、Na2SO4作原料,并用EG作分散剂进行制备。与SCN-互为等电子体的分子为
 中心原子的杂化方式为
中心原子的杂化方式为③铜的晶胞如图。它的空间利用率为
 ,
, ,0),则b处的分数坐标为
,0),则b处的分数坐标为
您最近一年使用:0次
【推荐1】电解铜的阳极泥中含有一定量X元素,它和硫同主族,是人体内不可缺少的微量元素之一,人体缺少X就会得“克山病”,X也是制光电池的 一种原料。从阳极泥中可以提取X。

(1)X的元素符号是_______ , 它的基态原子核外电子排布式(或原子结构示意图)为_______ 。
(2)阳极泥中X以X单质Ag2X、Cu2X等形式存在,X单质与浓硫酸反应的化学方程式为_______ ,Cu2X 与浓硫酸反应的化学方程式为_______ 。
(3)H2XO3与SO2反应得到X的化学方程式为_______ 。

(1)X的元素符号是
(2)阳极泥中X以X单质Ag2X、Cu2X等形式存在,X单质与浓硫酸反应的化学方程式为
(3)H2XO3与SO2反应得到X的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】钒酸根在溶液中以多种离子形式存在,如VO 、V2O
、V2O 、V3O
、V3O 、VO
、VO 等,pH值决定着其主要以什么形式存在。
等,pH值决定着其主要以什么形式存在。
(1)你认为pH越小,_______ 离子越多,pH越大,_______ 离子越多。
(2)画出下列离子的结构图:VO
_______ 、V2O
_______ 、V3O
_______ 。
(3)某同学在研究金属钒晶体时,以1个金属原子为中心,考查其它原子与它的距离。已知该晶体属于立方晶系,与该金属原子最近的原子核间距离为262.0pm,次近距离为302.5pm。请计算等放入金属钒晶体空隙中的最大原子半径_______ 。
 、V2O
、V2O 、V3O
、V3O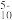 、VO
、VO 等,pH值决定着其主要以什么形式存在。
等,pH值决定着其主要以什么形式存在。(1)你认为pH越小,
(2)画出下列离子的结构图:VO


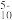
(3)某同学在研究金属钒晶体时,以1个金属原子为中心,考查其它原子与它的距离。已知该晶体属于立方晶系,与该金属原子最近的原子核间距离为262.0pm,次近距离为302.5pm。请计算等放入金属钒晶体空隙中的最大原子半径
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】下图是X、Y两种元素化合物的六方晶胞图。X用小黑球表示,Y用大白球表示。

(1)试写出该化合物的化学式(用X、Y表示)____ 。
(2)X占有Y围成的何类空隙中____ ?空隙占有率是多少___ ?
(3)试写出X、Y单独存在时的堆积方式____ 。(X用小写英文字母表示,Y用大写英文字母表示)并写出该化合物晶体的堆积方式_____ 。
(4)试写出该晶体密度的表达式_____ 。(晶胞参数用a(pm),c(pm)表示。Mx与My表示X与Y的摩尔质量)↓
(5)试写出该晶体的结构基元化学式___ ,画出点阵形式__ 。

(1)试写出该化合物的化学式(用X、Y表示)
(2)X占有Y围成的何类空隙中
(3)试写出X、Y单独存在时的堆积方式
(4)试写出该晶体密度的表达式
(5)试写出该晶体的结构基元化学式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】金属钠晶体为体心立方结构,钠原子在晶胞的体对角线上互相接触,晶胞参数a=429pm(即每个体心立方晶胞的边长为429pm)。
(1) 计算可知钠的原子半径为___________ pm,金属钠的理论密度___________ g· cm-3。
(2) 1982 年,我国化学家以NaCl为固体分散剂,对熔融金属钠直接氢化合成了晶体NaH,大大地降低了生产成本。NaH具有NaCl型结构,晶胞参数a= 488pm,已知Na +的离子半径为102pm ,则H- 的离子半径为___________ pm。
(3) NaH是合成氢化铝钠NaAlH4的关键材料NaAlH4是很有前途的储氢材料,密度为1. 2 g· cm-3,请估算NaAlH4的储氢性能(以H的密度表示)___________ 。
(1) 计算可知钠的原子半径为
(2) 1982 年,我国化学家以NaCl为固体分散剂,对熔融金属钠直接氢化合成了晶体NaH,大大地降低了生产成本。NaH具有NaCl型结构,晶胞参数a= 488pm,已知Na +的离子半径为102pm ,则H- 的离子半径为
(3) NaH是合成氢化铝钠NaAlH4的关键材料NaAlH4是很有前途的储氢材料,密度为1. 2 g· cm-3,请估算NaAlH4的储氢性能(以H的密度表示)
您最近一年使用:0次



