次氯酸盐相比次氯酸更稳定,更容易保存,所以,通常用氯气与氢氧化钠、氯气与消石灰反应制备“84”消毒液和漂粉精,然后再用于杀菌漂白。
(1)漂粉精的主要成分_______
(2)漂粉精的制法_______
(3)漂粉精的漂白原理_______
(1)漂粉精的主要成分
(2)漂粉精的制法
(3)漂粉精的漂白原理
22-23高一上·上海杨浦·期末 查看更多[2]
(已下线)专题04 海水中的氯-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(上海专用) 上海理工大学附属杨浦少云中学2022-2023学年高一上学期期末考试化学试卷
更新时间:2023-01-20 23:46:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】金属和非金属被广泛应用于人类生产生活中。
(1)实验室一般将Na保存在__________ 中;Na的一种化合物在生活中常用作面粉发泡剂,它在受热时会发生分解,它的化学式为______________ ;Na的另外一种化合物常用于潜艇中处理CO2和供氧,它处理CO2的化学方程式为__________________ 。
(2)实验室中FeSO4是否变质,常用试剂________ (填化学式)溶液来检验;为防止FeSO4变质,常在其中加入几根铁钉,理由是(以离子方程式表示)______________ 。
(3)工业上将氯气通入石灰乳制取漂白粉,漂白粉的有效成分 是________ (填化学式)。
(4)盛NaOH的试剂瓶不能用玻璃塞的原因是(以离子方程式表示)______________ 。
(1)实验室一般将Na保存在
(2)实验室中FeSO4是否变质,常用试剂
(3)工业上将氯气通入石灰乳制取漂白粉,漂白粉的
(4)盛NaOH的试剂瓶不能用玻璃塞的原因是(以离子方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】利用图象,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为__________ ,用途之一是__________ ;丁属于__________ (“酸性”或”碱性”)氧化物。
(2)根据氯元素的化合价判断,乙物质__________ 。
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)电解甲溶液制备己的化学反应为甲+H2O 己+H2↑(未配平),配平后参与反应的甲与H2O的计量数之比是
己+H2↑(未配平),配平后参与反应的甲与H2O的计量数之比是__________ 。
(4)若庚是漂粉精的有效成分,存放不当,在空气中易失效。原因是________ (用化学方程式表示)。

(1)丙的化学式为
(2)根据氯元素的化合价判断,乙物质
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)电解甲溶液制备己的化学反应为甲+H2O
 己+H2↑(未配平),配平后参与反应的甲与H2O的计量数之比是
己+H2↑(未配平),配平后参与反应的甲与H2O的计量数之比是(4)若庚是漂粉精的有效成分,存放不当,在空气中易失效。原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶“84”消毒液,该消毒液通常稀释到100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如图信息:

回答下列问题:
(1)该“84”消毒液 物质的量浓度约为
物质的量浓度约为_______  (保留1位小数)。
(保留1位小数)。
(2)某同学欲配制上述浓度的“84”消毒液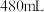 。请你帮他将下列过程补充完整:
。请你帮他将下列过程补充完整:
①计算并用托盘天平称量 固体
固体_______ g;
②将称量好的 固体放在烧杯中,加适量蒸馏水,用玻璃棒搅拌,使
固体放在烧杯中,加适量蒸馏水,用玻璃棒搅拌,使 全部溶解;
全部溶解;
③将烧杯中的溶液沿着玻璃棒注入容量瓶中;
④用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也都注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀;
⑤将蒸馏水注入容量瓶中,当液面距离容量瓶颈部的刻度线1~2cm时,改用_______ 滴加蒸馏水至凹液面与刻度线相切,盖好瓶塞,反复上下颠倒,摇匀;
⑥将配好的溶液倒入试剂瓶中,并贴好标签。
(3)在配制过程中,下列操作中能使所配溶液的浓度偏高的有_______ (填序号)。
①用托盘天平称量时物品和砝码放反(托盘天平的最小砝码为1g)
②烧杯中固体溶解后未冷却直接转移定容
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
(4)一瓶上述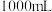 的“84”消毒液的消毒能力相当于
的“84”消毒液的消毒能力相当于_______ 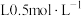 的
的 溶液(消毒能力为:氧化病毒时消毒剂所得电子数目,
溶液(消毒能力为:氧化病毒时消毒剂所得电子数目, 消毒后
消毒后 元素变为
元素变为 价)。
价)。
(5)“84”消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因:_______ 。某消毒小组人员用 的浓硫酸配制
的浓硫酸配制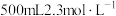 的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为_______  。
。

回答下列问题:
(1)该“84”消毒液
 物质的量浓度约为
物质的量浓度约为 (保留1位小数)。
(保留1位小数)。(2)某同学欲配制上述浓度的“84”消毒液
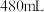 。请你帮他将下列过程补充完整:
。请你帮他将下列过程补充完整:①计算并用托盘天平称量
 固体
固体②将称量好的
 固体放在烧杯中,加适量蒸馏水,用玻璃棒搅拌,使
固体放在烧杯中,加适量蒸馏水,用玻璃棒搅拌,使 全部溶解;
全部溶解;③将烧杯中的溶液沿着玻璃棒注入容量瓶中;
④用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也都注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀;
⑤将蒸馏水注入容量瓶中,当液面距离容量瓶颈部的刻度线1~2cm时,改用
⑥将配好的溶液倒入试剂瓶中,并贴好标签。
(3)在配制过程中,下列操作中能使所配溶液的浓度偏高的有
①用托盘天平称量时物品和砝码放反(托盘天平的最小砝码为1g)
②烧杯中固体溶解后未冷却直接转移定容
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
(4)一瓶上述
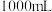 的“84”消毒液的消毒能力相当于
的“84”消毒液的消毒能力相当于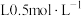 的
的 溶液(消毒能力为:氧化病毒时消毒剂所得电子数目,
溶液(消毒能力为:氧化病毒时消毒剂所得电子数目, 消毒后
消毒后 元素变为
元素变为 价)。
价)。(5)“84”消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因:
 的浓硫酸配制
的浓硫酸配制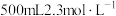 的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.NaClO是“84”消毒液的有效成分。请回答下列问题。
(1)NaClO中Cl元素的化合价是__ 。
(2)浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,结合离子方程式解释原因:__ 。
(已知酸性:H2CO3>HClO>HCO3-)。
(3)若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是:__ 。
Ⅱ.Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知:3Cl2+8NH3=6NH4Cl+N2,化工厂可用浓氨水来检验Cl2是否泄漏。该反应中氧化剂和还原剂的物质的量比为__ 。
(5)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是__ 。
(6)实验室常用烧碱溶液吸收Cl2。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时,混合液中NaClO和NaClO3的物质的量之比为___ 。
(1)NaClO中Cl元素的化合价是
(2)浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,结合离子方程式解释原因:
(已知酸性:H2CO3>HClO>HCO3-)。
(3)若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是:
Ⅱ.Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知:3Cl2+8NH3=6NH4Cl+N2,化工厂可用浓氨水来检验Cl2是否泄漏。该反应中氧化剂和还原剂的物质的量比为
(5)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是
(6)实验室常用烧碱溶液吸收Cl2。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时,混合液中NaClO和NaClO3的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是__________ (填“CaCl2”或“Ca(ClO)2”)。
(2)漂白粉露置在空气中容易失效,请用化学方程式表示其失效原理______________________________________________ 、_____________________________ 。
(3)氯水具有漂白作用,是由于其中含有___________ (填“HCl”或“HClO”)。
(2)漂白粉露置在空气中容易失效,请用化学方程式表示其失效原理
(3)氯水具有漂白作用,是由于其中含有
您最近一年使用:0次



