Ⅰ.NaClO是“84”消毒液的有效成分。请回答下列问题。
(1)NaClO中Cl元素的化合价是__ 。
(2)浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,结合离子方程式解释原因:__ 。
(已知酸性:H2CO3>HClO>HCO3-)。
(3)若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是:__ 。
Ⅱ.Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知:3Cl2+8NH3=6NH4Cl+N2,化工厂可用浓氨水来检验Cl2是否泄漏。该反应中氧化剂和还原剂的物质的量比为__ 。
(5)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是__ 。
(6)实验室常用烧碱溶液吸收Cl2。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时,混合液中NaClO和NaClO3的物质的量之比为___ 。
(1)NaClO中Cl元素的化合价是
(2)浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,结合离子方程式解释原因:
(已知酸性:H2CO3>HClO>HCO3-)。
(3)若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是:
Ⅱ.Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知:3Cl2+8NH3=6NH4Cl+N2,化工厂可用浓氨水来检验Cl2是否泄漏。该反应中氧化剂和还原剂的物质的量比为
(5)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是
(6)实验室常用烧碱溶液吸收Cl2。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时,混合液中NaClO和NaClO3的物质的量之比为
更新时间:2020-03-17 11:18:34
|
相似题推荐
【推荐1】按要求填空:
(1)在S2-、Fe2+、Mg2+、S、I- 、H+ 中,既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO +HNO3 →N2O3+ H2O;②NH3 +NO→HNO2+ H2O;③N2O4 +H2O→HNO3 + HNO2
其中你认为一定不可能实现的是___________ 。
(3)用双线桥标出方程式6HCl+KClO3=KCl+3Cl2↑+3H2O 中电子转移的方向和数目___________ ,该反应中若生成 426g Cl2,则被氧化的HCl的有多少___________ g。
(4)As2O3、Zn、AsH3 (气态)、ZnSO4、H2SO4、H2O组成的一个氧化还原反应体系中,已知As2O3作氧化剂, ZnSO4 作氧化产物。该反应的化学反应方程式为:___________ 。
(5)已知氧化性:Cl2 > Br2 > Fe3+ > I2,写出下列离子方程式:
a.少量氯气与FeI2溶液反应:___________ 。
b.氯气与FeBr2溶液以按个数比 1∶1 反应:___________ 。
(6)新型纳米材料氧缺位铁酸盐(MFe2Ox,3 < x < 4,M=Mn,Zn,Ni且均为+2 价,下同)是由铁酸盐 MFe2O4 经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于___________ ,铁酸盐MFe2O4经过高温反应得到 MFe2Ox的反应属于___________ (填“氧化还原”或“非氧化还原”)反应。
(7)在酸性条件下。 容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子,
容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子, 、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是
、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是___________ 。
(1)在S2-、Fe2+、Mg2+、S、I- 、H+ 中,既有氧化性又有还原性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO +HNO3 →N2O3+ H2O;②NH3 +NO→HNO2+ H2O;③N2O4 +H2O→HNO3 + HNO2
其中你认为一定不可能实现的是
(3)用双线桥标出方程式6HCl+KClO3=KCl+3Cl2↑+3H2O 中电子转移的方向和数目
(4)As2O3、Zn、AsH3 (气态)、ZnSO4、H2SO4、H2O组成的一个氧化还原反应体系中,已知As2O3作氧化剂, ZnSO4 作氧化产物。该反应的化学反应方程式为:
(5)已知氧化性:Cl2 > Br2 > Fe3+ > I2,写出下列离子方程式:
a.少量氯气与FeI2溶液反应:
b.氯气与FeBr2溶液以按个数比 1∶1 反应:
(6)新型纳米材料氧缺位铁酸盐(MFe2Ox,3 < x < 4,M=Mn,Zn,Ni且均为+2 价,下同)是由铁酸盐 MFe2O4 经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于
(7)在酸性条件下。
 容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子,
容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子, 、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是
、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】阅读下面科普信息,回答问题:
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。Fe2+易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如琥珀酸亚铁。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是_______ (填字母)
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2能把人体内的Fe2+转化为Fe3+而使Fe2+失去与O2结合的能力,这说明NaNO2具有_______ 性。
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有_______ 性。
(4)在Fe+4HNO3 = Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了_______ 性,若1 mol Fe参加反应时,被还原的HNO3为_______ mol。
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。Fe2+易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如琥珀酸亚铁。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2能把人体内的Fe2+转化为Fe3+而使Fe2+失去与O2结合的能力,这说明NaNO2具有
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在Fe+4HNO3 = Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
您最近一年使用:0次
【推荐3】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是___________ 。
(2)该反应中,发生还原反应的过程是_____________ →_____________ 。
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目:_________ 。
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为_________ L。
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目:
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】前一段时间,各地报刊纷纷转载了不要将不同品牌洁污剂混合使用的警告。据报道,在全国各地发生了多起混合洁污剂发生氯气中毒的事件。发生反应的离子方程式是:ClO+Cl+2H+=Cl2↑+H2O。根据你所掌握的化学知识作出如下判断:当事人使用的液态洁污剂之一必定含氯,其中氯最可能的存在形式是_________ 和_______ (填离子),当另一种具有_______ (性质)的液态洁污剂与之混合,可能发生上述反应而产生氯气。举例说明这两种洁污剂的名称(家用洁污剂的商品名称)___________ 、____________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】对物质进行分类是研究物质性质的重要方法。
现有如下含氯元素的物质:①液氯 ②氯水 ③盐酸 ④氯酸钾 ⑤漂白粉。
(1)这些物质中,属于纯净物的是(填编号,下同)_______ ,含有Cl2的有_______ 。
(2)下列各组分类中,错误 的是_______
(3)加热氯酸钾(不加催化剂),部分分解后停止加热,得到一种固体混合物,按照不同的分类标准,该混合物中的两种物质既可以是同类物质,也可以是不同类物质。若属于同类物质,你的分类标准是_______ ;若属于不同类物质,你的分类标准是_______ 。
(4)对物质进行分类,能够根据类别通性预测物质的性质。Cl2O属于酸性氧化物,写出Cl2O与水反应的化学方程式_______ 。
现有如下含氯元素的物质:①液氯 ②氯水 ③盐酸 ④氯酸钾 ⑤漂白粉。
(1)这些物质中,属于纯净物的是(填编号,下同)
(2)下列各组分类中,
| A.液氯:单质 | B.氯酸钾:含氧酸盐 |
| C.盐酸:有机酸 | D.漂白粉:混合物 |
(4)对物质进行分类,能够根据类别通性预测物质的性质。Cl2O属于酸性氧化物,写出Cl2O与水反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列10种物质: ①硫酸 ②CO2 ③Ba(OH)2固体 ④NH4Al(SO4)2固体 ⑤葡萄糖 ⑥Al ⑦氢氧化铁胶体 ⑧CH3COOH ⑨熔融氯化钾 ⑩氯水
请回答下列问题:
(1)上述物质中属于电解质的是______ (填序号),属于非电解质的是___________ (填序号),能导电的是___________ (填序号)。
(2)将①的稀溶液加入⑦中,实验现象为___________ 。
(3)向④的溶液中加入过量③的稀溶液,发生的离子反应方程式为:_____ 。
(4)久置的氯水酸性增强的原因:(化学方程式表示)___________ 。
请回答下列问题:
(1)上述物质中属于电解质的是
(2)将①的稀溶液加入⑦中,实验现象为
(3)向④的溶液中加入过量③的稀溶液,发生的离子反应方程式为:
(4)久置的氯水酸性增强的原因:(化学方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl-、ClO-、ClO 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
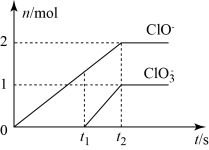
(1)t1时刻之前发生的反应是:___________
(2)t2时,Ca(OH)2与Cl2发生反应的总化学方程式为10Ca(OH)2+10Cl2=2Ca(ClO)2+Ca(ClO3)2+7CaCl2+10H2O,则该石灰乳中含有Ca(OH)2的物质的量是___________ mol。
(3)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入Cl2的速度不同,ClO-和ClO 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
___________ 2(填“>”、“<”或“=”);氯酸钙(Ca(ClO3)2)为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施___________ (写一条即可)。
(4)请配平化学方程式:KClO3+HCl--KCl+Cl2↑+H2O___________ 。若反应过程中转移2mol e-,则生成标准状况下Cl2的体积为___________ L。
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①3FeCl3+2KI=2FeCl2+2KCl+I2;
②2FeCl2+Cl2=2FeCl3;
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(5)FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是___________ 。
(6)在酸性溶液中存在大量的I-,则Cr2O 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是___________ 。
 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
(1)t1时刻之前发生的反应是:
(2)t2时,Ca(OH)2与Cl2发生反应的总化学方程式为10Ca(OH)2+10Cl2=2Ca(ClO)2+Ca(ClO3)2+7CaCl2+10H2O,则该石灰乳中含有Ca(OH)2的物质的量是
(3)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入Cl2的速度不同,ClO-和ClO
 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
(4)请配平化学方程式:KClO3+HCl--KCl+Cl2↑+H2O
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①3FeCl3+2KI=2FeCl2+2KCl+I2;
②2FeCl2+Cl2=2FeCl3;
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(5)FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是
(6)在酸性溶液中存在大量的I-,则Cr2O
 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】NaCl是一种基础化工原料,通过电解饱和食盐水可以制得NaOH、H2、Cl2。完成下列填空:
(1)写出电解饱和食盐水的化学方程式_______ 。开始时_______ 极(阴、阳)碱性增强。
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式_______ 。
(3)氯气压缩成为液氯属于_______ 变化(选填“物理”“化学”)。常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),其中一步反应是:2NH3+3Cl2→N2+6HCl,该反应也表明氯和氮的非金属性_______ > _______ 。写出产生白烟的化学方程式:_______ 。该白烟的成分溶于水,溶液呈_______ 性。(酸、碱或中性),用离子方程式解释原因_______ 。
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
(5)取25 mLpH=2的醋酸溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为c(Na+)_______ c(CH3COO-)。
(1)写出电解饱和食盐水的化学方程式
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式
(3)氯气压缩成为液氯属于
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
| A.都被促进 | B.都被抑制 |
| C.甲中被促进,乙中被抑制 | D.甲中被抑制,乙中被促进 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】正误判断
1.1molCa变成Ca2+时失去的电子数为2NA。(_______)
2.1molCl2与足量Fe反应,转移的电子数为3NA。(_______)
3.1molCl2参加反应转移电子数一定为2NA。(_______)
4.在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为6NA。(_______)
5.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA。(_______)
1.1molCa变成Ca2+时失去的电子数为2NA。(_______)
2.1molCl2与足量Fe反应,转移的电子数为3NA。(_______)
3.1molCl2参加反应转移电子数一定为2NA。(_______)
4.在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为6NA。(_______)
5.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】高三一年的化学复习,学生要抓住两方面,一方面是教材,另一方面是历年的高考真题。每年的高考题,在教材中几乎都能找到影子,所以同学们一定要紧紧抓住教材,根据《必修一》第三章和第四章的内容回答下列问题:
(1)实验3-1是取用钠单质的实验,用品有小刀,_____ 、_____ 、培养皿。
(2)铁是人类应用最广泛,铁的氧化物有三种,其中Fe3O4是一种具有_____ 的黑色晶体,俗称磁性氧化铁.Fe2O3的用途________ (举一例)。
(3)氢氧化铝其有两性,写出氢氧化铝分别溶于强酸和强碱的离子方程式_____ ,_______ 。
(4)在抗震救灾中要用到大量漂白粉和漂白液杀菌消毒,漂白粉的制取过程如下:通过煅烧石灰石得到生石灰,生石灰溶于水得石灰乳,在向石灰乳中通入氯气反应得漂白粉,有关的反应化学方程式为:CaCO3 CaO+CO2↑
CaO+CO2↑_________ 、_________ 。
(1)实验3-1是取用钠单质的实验,用品有小刀,
(2)铁是人类应用最广泛,铁的氧化物有三种,其中Fe3O4是一种具有
(3)氢氧化铝其有两性,写出氢氧化铝分别溶于强酸和强碱的离子方程式
(4)在抗震救灾中要用到大量漂白粉和漂白液杀菌消毒,漂白粉的制取过程如下:通过煅烧石灰石得到生石灰,生石灰溶于水得石灰乳,在向石灰乳中通入氯气反应得漂白粉,有关的反应化学方程式为:CaCO3
 CaO+CO2↑
CaO+CO2↑
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯气与碱的反应
(1)与氢氧化钠溶液反应——制取漂白液
①制取反应的化学方程式:___________ 。
②离子方程式:___________ 。
③漂白液的有效成分是次氯酸钠。
(2)与冷的石灰乳反应——制取漂白粉
①制取反应的化学方程式:___________ 。
②漂白粉的主要成分是___________ ,有效成分是___________ 。
【注意】漂白液、漂白粉和漂粉精既可作漂白剂,又可作消毒剂。
(1)与氢氧化钠溶液反应——制取漂白液
①制取反应的化学方程式:
②离子方程式:
③漂白液的有效成分是次氯酸钠。
(2)与冷的石灰乳反应——制取漂白粉
①制取反应的化学方程式:
②漂白粉的主要成分是
【注意】漂白液、漂白粉和漂粉精既可作漂白剂,又可作消毒剂。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】从某超市中查询到某品牌消毒液包装说明的部分内容,摘录如下:
主要有效成分为次氯酸钠,有效氯含量8 000~10000mg·L-1.可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用。切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品。本品须密封,置阴凉暗处保存。
请完成以下实验探究过程:
阅读材料,根据学过的知识判断问题
(1)该消毒液是怎样制取的(用离子方程式表示)________ 消毒液的成分中只有NaClO吗?_________
(2)该消毒液还具有的化学性质是___________ (填序号)。
A.强氧化性 B.强还原性 C.不稳定性 D.漂白性 E。弱酸性 F。中性 G。碱性
(3)从该消毒液的保存要求分析,导致其失效的主要原因是(用化学方程式表示)___________ 。
主要有效成分为次氯酸钠,有效氯含量8 000~10000mg·L-1.可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用。切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品。本品须密封,置阴凉暗处保存。
请完成以下实验探究过程:
阅读材料,根据学过的知识判断问题
(1)该消毒液是怎样制取的(用离子方程式表示)
(2)该消毒液还具有的化学性质是
A.强氧化性 B.强还原性 C.不稳定性 D.漂白性 E。弱酸性 F。中性 G。碱性
(3)从该消毒液的保存要求分析,导致其失效的主要原因是(用化学方程式表示)
您最近一年使用:0次



