高三一年的化学复习,学生要抓住两方面,一方面是教材,另一方面是历年的高考真题。每年的高考题,在教材中几乎都能找到影子,所以同学们一定要紧紧抓住教材,根据《必修一》第三章和第四章的内容回答下列问题:
(1)实验3-1是取用钠单质的实验,用品有小刀,_____ 、_____ 、培养皿。
(2)铁是人类应用最广泛,铁的氧化物有三种,其中Fe3O4是一种具有_____ 的黑色晶体,俗称磁性氧化铁.Fe2O3的用途________ (举一例)。
(3)氢氧化铝其有两性,写出氢氧化铝分别溶于强酸和强碱的离子方程式_____ ,_______ 。
(4)在抗震救灾中要用到大量漂白粉和漂白液杀菌消毒,漂白粉的制取过程如下:通过煅烧石灰石得到生石灰,生石灰溶于水得石灰乳,在向石灰乳中通入氯气反应得漂白粉,有关的反应化学方程式为:CaCO3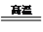 CaO+CO2↑
CaO+CO2↑_________ 、_________ 。
(1)实验3-1是取用钠单质的实验,用品有小刀,
(2)铁是人类应用最广泛,铁的氧化物有三种,其中Fe3O4是一种具有
(3)氢氧化铝其有两性,写出氢氧化铝分别溶于强酸和强碱的离子方程式
(4)在抗震救灾中要用到大量漂白粉和漂白液杀菌消毒,漂白粉的制取过程如下:通过煅烧石灰石得到生石灰,生石灰溶于水得石灰乳,在向石灰乳中通入氯气反应得漂白粉,有关的反应化学方程式为:CaCO3
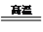 CaO+CO2↑
CaO+CO2↑
更新时间:2017-08-13 18:23:45
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是___________ ;过一会儿,溶液颜色逐渐褪去,起作用的微粒是___________ 。
(2)工业氯气泄漏后,可向空气中喷洒氨水,生成大量白烟及空气中含量最多的气体。试写出该过程的化学反应方程式:___________ 。
(3)工业上制取漂白粉的反应方程式为:___________ 。
(4)已知:Na2Cr2O7+14HCl(浓)=2CrCl3+2NaCl+3Cl2↑+7H2O,该反应过程中每生成标况下3.36LCl2,转移的电子数是___________ ;被还原掉的物质的物质的量是:___________
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是
(2)工业氯气泄漏后,可向空气中喷洒氨水,生成大量白烟及空气中含量最多的气体。试写出该过程的化学反应方程式:
(3)工业上制取漂白粉的反应方程式为:
(4)已知:Na2Cr2O7+14HCl(浓)=2CrCl3+2NaCl+3Cl2↑+7H2O,该反应过程中每生成标况下3.36LCl2,转移的电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)根据题意选择以下四种物质的字母序号填空:
A.Si B.Na2SiO3 C.Ca(ClO)2 D.KAl(SO4)2·12H2O
①漂白粉的有效成分是_______ 。
②可用于制备硅胶和木材防火剂的是_______ 。
③可用于制计算机芯片的是_______ 。
④可用于作净水剂的是_______ 。
(2)物质的量是化学中常用的物理量,请完成以下有关计算:
①标准状况下,含有相同氧原子数的CO和CO2的体积之比为_______ 。
②100 mL硫酸钠溶液中n(Na+)=0.20 mol,则其中c( )=
)=_______ 。
③配制1.0 mol/L硫酸溶液250 mL ,需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为_______ mL(计算结果保留一位小数)。如果实验室有15 mL、20 mL、50 mL量筒,应选用_______ mL的量筒最好。若定容时仰视刻度线,所配溶液浓度_______ 。(填偏大、偏小或无影响)
A.Si B.Na2SiO3 C.Ca(ClO)2 D.KAl(SO4)2·12H2O
①漂白粉的有效成分是
②可用于制备硅胶和木材防火剂的是
③可用于制计算机芯片的是
④可用于作净水剂的是
(2)物质的量是化学中常用的物理量,请完成以下有关计算:
①标准状况下,含有相同氧原子数的CO和CO2的体积之比为
②100 mL硫酸钠溶液中n(Na+)=0.20 mol,则其中c(
 )=
)=③配制1.0 mol/L硫酸溶液250 mL ,需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】学习小组利用如下流程制备过氧化钠,并设计实验验证其相关性质。
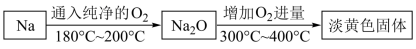
回答下列问题:
(1)金属钠被氧化失去金属光泽,颜色变为_______ 。
(2)流程中生成淡黄色固体的化学方程式为_______ 。
(3)小组同学取一定量淡黄色固体溶于冷水中,待固体全部反应后,仍可缓慢释放氧气。为探究固体溶解后溶液成分,设计如下实验方案进行验证:

①甲中产生较多气泡,证明固体溶解后溶液中有_______ (填化学式),写出甲中发生反应的化学方程式_______ 。
②向乙中滴入酚酞,溶液变红的原因是_______
(4)小组同学将金属钠加热至熔化后,误通入了干燥的CO2进行反应,将反应后固体产物溶于稀盐酸,产生气泡,观察到难溶于水的黑色固体。
①产物中与盐酸反应的物质可能为_______ (填化学式)。
②经检验,黑色固体为单质碳。写出CO2与Na反应的化学方程式_______ 。

回答下列问题:
(1)金属钠被氧化失去金属光泽,颜色变为
(2)流程中生成淡黄色固体的化学方程式为
(3)小组同学取一定量淡黄色固体溶于冷水中,待固体全部反应后,仍可缓慢释放氧气。为探究固体溶解后溶液成分,设计如下实验方案进行验证:

①甲中产生较多气泡,证明固体溶解后溶液中有
②向乙中滴入酚酞,溶液变红的原因是
(4)小组同学将金属钠加热至熔化后,误通入了干燥的CO2进行反应,将反应后固体产物溶于稀盐酸,产生气泡,观察到难溶于水的黑色固体。
①产物中与盐酸反应的物质可能为
②经检验,黑色固体为单质碳。写出CO2与Na反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空:
(1)写出钠与水反应的离子方程式:___________ 。
(2)过氧化钠的颜色为:___________ ,其阳离子和阴离子的个数比为___________ ,写出过氧化钠与水反应的化学方程式:___________ 。
(3)写出氯的原子结构示意图:___________ , 写出工业制漂白粉的化学方程式:___________ 。
(4)向碳酸氢钠溶液中滴加少量的氢氧化钙,写出反应的离子方程式:___________ 。
(1)写出钠与水反应的离子方程式:
(2)过氧化钠的颜色为:
(3)写出氯的原子结构示意图:
(4)向碳酸氢钠溶液中滴加少量的氢氧化钙,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请按要求完成下列各题:
(1)将一小块钠投入到盛CuSO4溶液的烧杯中,剧烈反应,放出气体并生成蓝色沉淀,其反应的离子方程式为___ 。
(2)将FeSO4溶液与过量NaOH溶液混合并在空气中放置一段时间,整个过程中的现象为___ ,反应过程分两步,其中第2步反应的化学方程式为___ 。
(3)写出溶液中硫酸氢钠的电离方程式___ 。
(4)配制某浓度的稀硫酸,用10mL量筒量取浓硫酸的体积如图Ⅰ所示,A与B,B与C刻度间相差1mL,如果刻度A为8,量筒中浓硫酸的体积是___ mL。
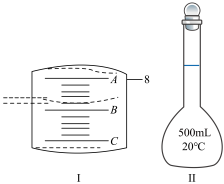
(5)要用CuSO4·5H2O晶体配制500mL0.01mol/LCuSO4溶液,应该用托盘天平称取CuSO4·5H2O___ g(读到小数点后两位)
(6)图Ⅱ所示仪器的名称是___ 。
(1)将一小块钠投入到盛CuSO4溶液的烧杯中,剧烈反应,放出气体并生成蓝色沉淀,其反应的离子方程式为
(2)将FeSO4溶液与过量NaOH溶液混合并在空气中放置一段时间,整个过程中的现象为
(3)写出溶液中硫酸氢钠的电离方程式
(4)配制某浓度的稀硫酸,用10mL量筒量取浓硫酸的体积如图Ⅰ所示,A与B,B与C刻度间相差1mL,如果刻度A为8,量筒中浓硫酸的体积是

(5)要用CuSO4·5H2O晶体配制500mL0.01mol/LCuSO4溶液,应该用托盘天平称取CuSO4·5H2O
(6)图Ⅱ所示仪器的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据实验现象书写方程式:
Ⅰ.某同学进行如下实验:
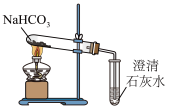
(1)加热NaHCO3的化学方程式:___________ 。
(2)一段时间后可以观察到澄清石灰水变浑浊,原因是___________ (用化学方程式表示,下同),再过一段时间后变澄清,发生的反应是___________ 。
Ⅱ.另一位同学进行如下实验:

(3)开始时,溶液的红色没有明显变化,也没有明显的气泡产生,反应的离子方程式为:___________ 。
(4)继续滴加盐酸,溶液的浅红色褪去,有大量气泡出现,反应的离子方程式为:___________ 。
Ⅲ.书写方程式:
(5)实验室检验Al3+的离子方程式:___________ 、___________ 。
(6)实验室制备Al(OH)3的离子方程式:___________ 、___________ (写出两种方法)
(7)除去Fe2O3中的Al2O3,可以选用的试剂是:___________ ,反应的离子方程式是___________ 。
(8)打磨过的铝条与NaOH反应的离子方程式:___________ 。
Ⅰ.某同学进行如下实验:

(1)加热NaHCO3的化学方程式:
(2)一段时间后可以观察到澄清石灰水变浑浊,原因是
Ⅱ.另一位同学进行如下实验:

(3)开始时,溶液的红色没有明显变化,也没有明显的气泡产生,反应的离子方程式为:
(4)继续滴加盐酸,溶液的浅红色褪去,有大量气泡出现,反应的离子方程式为:
Ⅲ.书写方程式:
(5)实验室检验Al3+的离子方程式:
(6)实验室制备Al(OH)3的离子方程式:
(7)除去Fe2O3中的Al2O3,可以选用的试剂是:
(8)打磨过的铝条与NaOH反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期元素在周期表中的位置如图所示。请按要求回答下列问题。
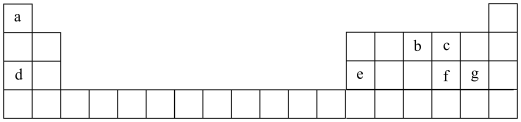
(1)由a、c、d形成的化合物的电子式为___________ ,该物质属于___________ 化合物(填“离子”或“共价”)。可能含有的化学键类型有___________ 。
(2)a与b形成的二元化合物中,所含电子数为10的分子的电子式为___________ ,a与c形成的二元化合物中,所含电子数为18的物质的结构式为___________ 。
(3)在全国抗击“新冠肺炎”的“战疫”中用了大量的“84”来消毒杀菌,84消毒液和洁厕灵混合使用时产生了一种有毒气体,写出两者混合时的化学反应方程式:___________ 。
(4)写出d与e两种元素的最高价氧化物对应的水化物相互反应的离子方程式:___________ 。

(1)由a、c、d形成的化合物的电子式为
(2)a与b形成的二元化合物中,所含电子数为10的分子的电子式为
(3)在全国抗击“新冠肺炎”的“战疫”中用了大量的“84”来消毒杀菌,84消毒液和洁厕灵混合使用时产生了一种有毒气体,写出两者混合时的化学反应方程式:
(4)写出d与e两种元素的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铝及其化合物在生产、生活中用途广泛。
(1)航母升降机可用铝镁合金制造,销镁合金在焊接前应先用氢氧化钠溶液处理表面的氧化膜,发生反应的化学方程式为________ 。
(2)实验室欲以铝屑为起点制备氢氧化铝,如按Al→Al3+→Al(OH)3流程制备,使用最合适的药品是铝屑、稀硫酸、氨水,不用氢氧化钠溶液代替氨水的原因是________ 。写出该制备方案中第二步反应的离子方程式________ 。
(3)氢氧化铝是医用胃酸中和剂的一种,选用其作为胃酸中和剂的两个主要原因是________ ,________ 。
(1)航母升降机可用铝镁合金制造,销镁合金在焊接前应先用氢氧化钠溶液处理表面的氧化膜,发生反应的化学方程式为
(2)实验室欲以铝屑为起点制备氢氧化铝,如按Al→Al3+→Al(OH)3流程制备,使用最合适的药品是铝屑、稀硫酸、氨水,不用氢氧化钠溶液代替氨水的原因是
(3)氢氧化铝是医用胃酸中和剂的一种,选用其作为胃酸中和剂的两个主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有下列七种物质:①CO2 ②过氧化钠 ③氧化铁 ④0.5 mol/LNaOH溶液 ⑤碳酸氢钠 ⑥0.5 mol/LNaHSO4溶液 ⑦次氯酸钠。请根据上述物质回答下列问题:
(1)写出物质对应的用途(填序号)。
②______ ③_______ ⑤________ ⑦________ 。
(2)含有0.4 mol氧原子的①在标准状况下的体积为______ L。
(3)④⑥两种溶液混合可以发生反应,离子方程式为______ 。
(4)废水脱氮工艺有一种方法是在废水中加入过量⑦使 完全转化为N2,此方法可用离子方程式表示为:2
完全转化为N2,此方法可用离子方程式表示为:2 +3ClO-=N2↑+3Cl-+2H++3H2O。该反应中氧化剂与还原剂的物质的量之比为
+3ClO-=N2↑+3Cl-+2H++3H2O。该反应中氧化剂与还原剂的物质的量之比为______ ;用单线桥法在离子方程式上标出电子转移的方向和数目______ ;
(5)某同学帮助水质检测站配制240 mL④溶液以备使用。
①该同学应用托盘天平称取NaOH固体______  。
。
②下列图示对应的操作规范的是______ (填序号)。
A.称量 B.溶解
B.溶解
C.转移 D.定容
D.定容
③定容时加水不慎超过了刻度线,用胶头滴管吸出少量溶液,所配制溶液的浓度会______ (填“偏大”“偏小”或“无影响”)。
(1)写出物质对应的用途(填序号)。
| 物质 用途 ② a.面粉发酵粉 ③ b.84消毒液的有效成分 ⑤ c.呼吸面具中作供氧剂 ⑦ d.红色油漆和涂料 |
②
(2)含有0.4 mol氧原子的①在标准状况下的体积为
(3)④⑥两种溶液混合可以发生反应,离子方程式为
(4)废水脱氮工艺有一种方法是在废水中加入过量⑦使
 完全转化为N2,此方法可用离子方程式表示为:2
完全转化为N2,此方法可用离子方程式表示为:2 +3ClO-=N2↑+3Cl-+2H++3H2O。该反应中氧化剂与还原剂的物质的量之比为
+3ClO-=N2↑+3Cl-+2H++3H2O。该反应中氧化剂与还原剂的物质的量之比为(5)某同学帮助水质检测站配制240 mL④溶液以备使用。
①该同学应用托盘天平称取NaOH固体
 。
。②下列图示对应的操作规范的是
A.称量
 B.溶解
B.溶解
C.转移
 D.定容
D.定容
③定容时加水不慎超过了刻度线,用胶头滴管吸出少量溶液,所配制溶液的浓度会
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下一些氧化物和单质之间可发生如下图所示的反应:其中,氧化物Ⅰ是红棕色固体,氧化物Ⅱ、Ⅲ、Ⅳ在反应条件下都是气体。

(1)氧化物Ⅰ的化学式是________ ,氧化物Ⅱ的化学式是________ 。
(2)反应①的化学方程式是_________ ;反应②的化学方程式_______ ;反应③的化学方程式是_______________ 。

(1)氧化物Ⅰ的化学式是
(2)反应①的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】学习常见物质时,会从“价”和“类”两个方面进行学习。如图表示铁元素的常见化合价与含铁物质类别的关系。
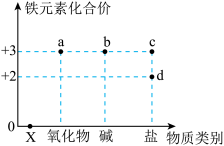
(1)X的物质类别是_______ 。
(2)铁和硫单质反应生成的含铁化合物属于如图中的_______ (填序号)。若不引入杂质,将FeCl3溶液转化FeCl2溶液的离子方程式为:_______ 。
(3)某同学弄清了氨的喷泉实验原理后,探究X与浓硝酸反应生成的气体能否用来做喷泉实验:标准状况下,用一充满该气体的烧瓶来做喷泉实验,实验结果水只能充到烧瓶体积的_______ 处,所得溶液的浓度为_______ mol·L-1。
(4)某同学欲用物质a制取物质b,设计了如图实验步骤:

物质a与稀盐酸反应的离子方程式为_______ 。如果向盛有溶液甲的烧杯中滴加NaOH溶液至过量,下面图象能正确表示烧杯中溶液质量变化的是_______ (填序号)。

(5)c点对应的阳离子用_______ 试剂检验(写出化学名称);现象是_______ ;写出对应的离子方程式_______ 。

(1)X的物质类别是
(2)铁和硫单质反应生成的含铁化合物属于如图中的
(3)某同学弄清了氨的喷泉实验原理后,探究X与浓硝酸反应生成的气体能否用来做喷泉实验:标准状况下,用一充满该气体的烧瓶来做喷泉实验,实验结果水只能充到烧瓶体积的
(4)某同学欲用物质a制取物质b,设计了如图实验步骤:

物质a与稀盐酸反应的离子方程式为

(5)c点对应的阳离子用
您最近一年使用:0次



