在方程式中标出电子转移的方向和数目,________
3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O
氧化剂:_______ ,氧化产物:_______ ,_______ 元素被氧化。
3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O
氧化剂:
更新时间:2023-01-20 23:46:06
|
相似题推荐
【推荐1】I.已知反应 浓
浓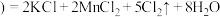 ,若有
,若有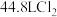 (已换算为标准状况)生成,求:
(已换算为标准状况)生成,求:
(1)被氧化的 为
为_______  ,转移电子数目为
,转移电子数目为_______ 。
(2)用“双线桥”标出上述反应的电子转移方向和数目_______ 。
(3)配平:①_______
_______H2S+_______SO2=_______S↓+_______H2O
②_______
_______Cu+_______NO3-+_______ =_______Cu2++_______NO↑+_______H2O
=_______Cu2++_______NO↑+_______H2O
II.阅读下面科普信息,回答问题:
(4)工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有_______ 性。下列不能实现上述转化的物质是_______ 。
A. B.O2 C.Fe D.
B.O2 C.Fe D.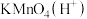
(5)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有_______ 性。
(6)在 稀
稀 的反应中,
的反应中, 参加反应时,被还原的
参加反应时,被还原的 为
为_______  。
。
 浓
浓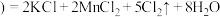 ,若有
,若有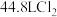 (已换算为标准状况)生成,求:
(已换算为标准状况)生成,求:(1)被氧化的
 为
为 ,转移电子数目为
,转移电子数目为(2)用“双线桥”标出上述反应的电子转移方向和数目
(3)配平:①
_______H2S+_______SO2=_______S↓+_______H2O
②
_______Cu+_______NO3-+_______
 =_______Cu2++_______NO↑+_______H2O
=_______Cu2++_______NO↑+_______H2OII.阅读下面科普信息,回答问题:
(4)工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有A.
 B.O2 C.Fe D.
B.O2 C.Fe D.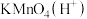
(5)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(6)在
 稀
稀 的反应中,
的反应中, 参加反应时,被还原的
参加反应时,被还原的 为
为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】镁与稀硝酸的反应为:4Mg+10HNO3(稀)=4Mg(NO3)2+NH4NO3+3H2O
(1)该反应中,还原产物是___________ ,HNO3表现了___________ 。(选填“还原性”、“氧化性”、“酸性”、“碱性”)。氧化剂与还原剂的物质的量之比为___________ 。
(2)用“双线桥法”表示该反应中电子转移的方向和数目。___________ ,4Mg+10HNO3(稀)=4Mg(NO3)2+NH4NO3+3H2O
(3)若反应过程中转移的电子数为6.02×1023,则被还原的硝酸物质的量为___________ 。
(1)该反应中,还原产物是
(2)用“双线桥法”表示该反应中电子转移的方向和数目。
(3)若反应过程中转移的电子数为6.02×1023,则被还原的硝酸物质的量为
您最近一年使用:0次
【推荐1】用双线桥法标出电子转移的方向与数目:
_____ K2Cr2O7+_____ HCl=_____ KCl+_____ CrCl3+_____ H2O+___ Cl2↑__________
以上反应中失电子的物质是______ ,还原产物是 ______ ,每生成lmol这种还原产物,将有______ mol电子发生转移氧化剂与还原剂的物质的量之比为______ , 生成标准状况下氯气______ 升。
以上反应中失电子的物质是
您最近一年使用:0次
【推荐2】高锰酸钾(KMnO4)为重要的化合物,具有众多应用。
I.高锰酸钾的制备可以通过氯酸钾(KClO3)、氢氧化钾(KOH)和二氧化锰(MnO2)在加热条件下反应先生成锰酸钾(K2MnO4),再由K2MnO4通过氧化还原化学反应转化成KMnO4。
(1)配平化学反应方程式:_______ 。

Ⅱ.接着向K2MnO4溶液中通入CO2,可使K2MnO4发生歧化反应得到KMnO4和MnO2。具体反应为:3 K2MnO4+2CO2=2 KMnO4+ MnO2+2K2CO3。
(2)用双线桥法标出反应的电子转移:_______ 。
(3)歧化反应中氧化剂和还原剂的物质的量之比为_______ 。
Ⅲ.用流程Ⅱ的方法制备KMnO4,K2MnO4利用率低,仅 转化为KMnO4。为使K2MnO4完全
转化为KMnO4。为使K2MnO4完全转化 为KMnO4,可以通过电解法。离子方程式为 _______。
_______。
(4)通过化合价升降 分析,确定该反应的还原产物为_______ ;补全并配平电解反应的离子反应方程式_______ 。
I.高锰酸钾的制备可以通过氯酸钾(KClO3)、氢氧化钾(KOH)和二氧化锰(MnO2)在加热条件下反应先生成锰酸钾(K2MnO4),再由K2MnO4通过氧化还原化学反应转化成KMnO4。
(1)配平化学反应方程式:

Ⅱ.接着向K2MnO4溶液中通入CO2,可使K2MnO4发生歧化反应得到KMnO4和MnO2。具体反应为:3 K2MnO4+2CO2=2 KMnO4+ MnO2+2K2CO3。
(2)用双线桥法标出反应的电子转移:
(3)歧化反应中氧化剂和还原剂的物质的量之比为
Ⅲ.用流程Ⅱ的方法制备KMnO4,K2MnO4利用率低,仅
 转化为KMnO4。为使K2MnO4完全
转化为KMnO4。为使K2MnO4完全 _______。
_______。(4)通过
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请回答下面的问题
(1)氧化亚铜(Cu2O)是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:
i.Cu2O+H2SO4=CuSO4+Cu+H2O;
ii.3Cu2O+14HNO3(稀)=6Cu(NO3)2+2NO↑+7H2O
①反应i中还原剂为___________ (填化学式,下同),还原产物为___________ 。
②用单线桥标出反应ii中电子转移的方向和数目:___________ 。
③请写出反应ii的离子方程式:___________ 。
(2)高铁酸钠(Na2FeO4)有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。写出并配平湿法制备高铁酸钠的离子方程式:
、Cl-、H2O。写出并配平湿法制备高铁酸钠的离子方程式:___________ 。
(1)氧化亚铜(Cu2O)是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:
i.Cu2O+H2SO4=CuSO4+Cu+H2O;
ii.3Cu2O+14HNO3(稀)=6Cu(NO3)2+2NO↑+7H2O
①反应i中还原剂为
②用单线桥标出反应ii中电子转移的方向和数目:
③请写出反应ii的离子方程式:
(2)高铁酸钠(Na2FeO4)有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。写出并配平湿法制备高铁酸钠的离子方程式:
、Cl-、H2O。写出并配平湿法制备高铁酸钠的离子方程式:
您最近一年使用:0次


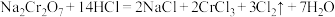
 转移
转移

