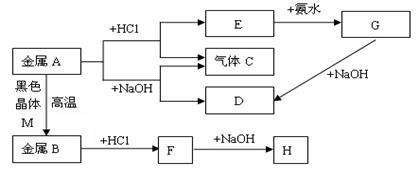
各物质间的转化关系如下图所示,请完成下列空白。
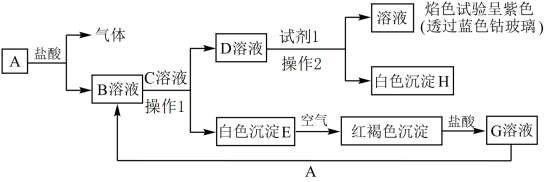
(1)组成A的元素在周期表中的位置是_______ 。
(2)C溶液中溶质的电子式为_______ 。
(3)操作1和操作2操作名称是_______ 。
(4)试剂1的化学式为_______ 。
(5)检验G溶液中阳离子的试剂是_______ 。
(6)写出E转化为红褐色沉淀的化学方程式:_______ 。
(7)写出向G溶液中加入A后的离子方程式:_______ 。

(1)组成A的元素在周期表中的位置是
(2)C溶液中溶质的电子式为
(3)操作1和操作2操作名称是
(4)试剂1的化学式为
(5)检验G溶液中阳离子的试剂是
(6)写出E转化为红褐色沉淀的化学方程式:
(7)写出向G溶液中加入A后的离子方程式:
更新时间:2023-01-21 22:31:12
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
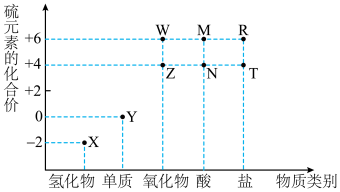
【推荐1】利用元素的化合价物质类别的坐标系,可以对含某元素的各物质性质有整体的认识。如图是硫元素的常见化合价与部分物质类别的对应关系。______ ;检验其阴离子的方法是______ 。
(2)化石燃料的燃烧可产生 ,在上述图表中它是
,在上述图表中它是______ (图中的字母),为避免过多 进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是
进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是 )吸收该物质,成本低廉。其过程如下。
)吸收该物质,成本低廉。其过程如下。 时,发生的主要反应的离子方程式为
时,发生的主要反应的离子方程式为______ 。
②氧化的目的是将硫元素全部转化为 ,该过程中溶液pH
,该过程中溶液pH______ (填“升高”“不变”或“降低”)。
③排放海水与原海水相比,减少的 与增加的
与增加的 的物质的量之比的为
的物质的量之比的为______ 。
(3)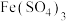 溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为
溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为______ ;每脱除170kg X,消耗标准状况下 的体积为
的体积为______ L。
(2)化石燃料的燃烧可产生
 ,在上述图表中它是
,在上述图表中它是 进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是
进入大气造成酸雨,沿海的火电站可利用天然海水(显弱碱性的微粒主要是 )吸收该物质,成本低廉。其过程如下。
)吸收该物质,成本低廉。其过程如下。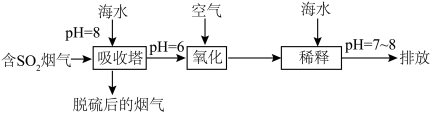
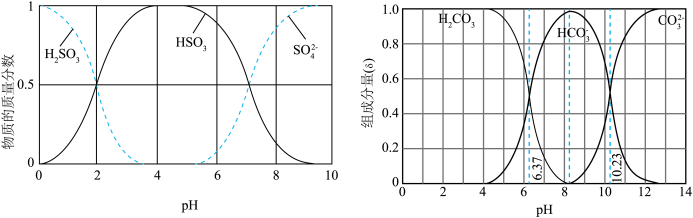
 时,发生的主要反应的离子方程式为
时,发生的主要反应的离子方程式为②氧化的目的是将硫元素全部转化为
 ,该过程中溶液pH
,该过程中溶液pH③排放海水与原海水相比,减少的
 与增加的
与增加的 的物质的量之比的为
的物质的量之比的为(3)
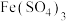 溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为
溶液脱除空气污染物X并再生的原理如图所示。反应I的离子方程式为 的体积为
的体积为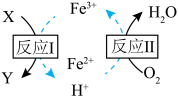
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】如图中A~H都是中学化学中常见的物质,其中,常温下A能使铁或铝钝化,B是固体非金属单质,C为水,D是一种能使品红溶液褪色的无色气体,F是金属单质,G可以用作耐火材料,它们之间有如下转化关系:
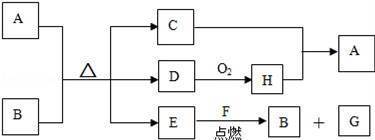
(1)写出下列物质的化学式:E____________ ,H____________ ;
(2)写出A溶液与B反应的化学方程式:____________ ;
试写出E与F的反应方程式:_______________ 。

(1)写出下列物质的化学式:E
(2)写出A溶液与B反应的化学方程式:
试写出E与F的反应方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】制烧碱所用盐水需两次精制。第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、Fe3+、SO42-等离子,过程如下:
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤
Ⅲ.滤液用盐酸调节pH,获得一次精制盐水
(1)过程Ⅰ除去的离子是________________
(2)过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如下表:
①检测Fe3+是否除尽的方法是_____________________ 。
②过程Ⅰ选用BaCl2而不选用CaCl2,运用表中数据解释原因:________________ 。
③除去Mg2+的离子方程式是_______________ 。
④检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测Ba2+ 即可,原因是:_____________ 。
(3)第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如下:

①过程Ⅳ除去的离子是____________________
②盐水b中含有SO42-。Na2S2O3将IO3-还原为I2的离子方程式是:________________ 。
③过程VI中,在电解槽的阴极区生成NaOH,结合化学平衡原理解释:____________ 。
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤
Ⅲ.滤液用盐酸调节pH,获得一次精制盐水
(1)过程Ⅰ除去的离子是
(2)过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如下表:
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
②过程Ⅰ选用BaCl2而不选用CaCl2,运用表中数据解释原因:
③除去Mg2+的离子方程式是
④检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测Ba2+ 即可,原因是:
(3)第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如下:

①过程Ⅳ除去的离子是
②盐水b中含有SO42-。Na2S2O3将IO3-还原为I2的离子方程式是:
③过程VI中,在电解槽的阴极区生成NaOH,结合化学平衡原理解释:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D和甲有以下转化关系。已知甲是短周期元素形成的盐,且是某种消毒液的有效成分,D可溶于酸。

请回答下列问题:
(1)组成A的元素在周期表中位于第_______ 周期第_______ 族。
(2)甲能使B迅速转化为D,甲是(写化学式)_______ ,此时甲溶液表现的性质是_______ 和_______ 。
(3)鉴定C中阳离子(不考虑H+)的试剂_______ ,现象_______ 。
(4)A转化为B时会放出无色气体E,在398 K时1 mol A完全反应放出热量Q kJ,则该反应的热化学方程式为_______
(5)若A转化为C时无气体放出,写出该反应的化学方程式_______ 。
(6)写出溶液C和溶液甲反应的离子方程式_______ 。

请回答下列问题:
(1)组成A的元素在周期表中位于第
(2)甲能使B迅速转化为D,甲是(写化学式)
(3)鉴定C中阳离子(不考虑H+)的试剂
(4)A转化为B时会放出无色气体E,在398 K时1 mol A完全反应放出热量Q kJ,则该反应的热化学方程式为
(5)若A转化为C时无气体放出,写出该反应的化学方程式
(6)写出溶液C和溶液甲反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】工业上常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某课外兴趣小组拟从上述腐蚀废液中(含FeCl3、FeCl2、CuCl2)回收铜,并重新获得FeCl3溶液,设计流程如下:
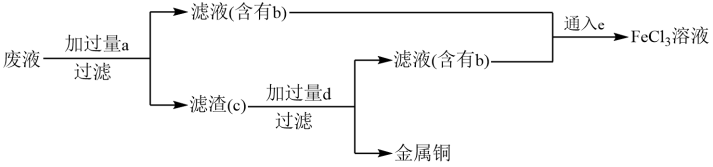
回答下列问题:
(1)写出FeCl3溶液与金属铜发生反应的离子方程式:___________ 。
(2)检验废液中Fe3+存在的试剂是___________ ,证明Fe3+存在的现象是___________ 。
(3)经检验知废液中仍有Fe3+存在。
①废液中加入过量a,发生的化学反应方程式为___________ ;
②过滤操作中需要使用的玻璃仪器有烧杯、___________ ;滤渣c的成分为___________ 。
(4)写出b与e反应的化学方程式:___________ 。

回答下列问题:
(1)写出FeCl3溶液与金属铜发生反应的离子方程式:
(2)检验废液中Fe3+存在的试剂是
(3)经检验知废液中仍有Fe3+存在。
①废液中加入过量a,发生的化学反应方程式为
②过滤操作中需要使用的玻璃仪器有烧杯、
(4)写出b与e反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】根据图中A~I均为中学化学中常见物质.其中A、B、 C、D为单质,通常情况下A为黄绿色气体,B为固体,C、D为无色气体:其余为化合物,其中常温下E是无色气体.其水溶液为强酸,G是具有磁性的物质,常温下I为液体。
(1)写出下列物质的化学式:A________ ;F______ ;G_________ 。
(2)反应①的离子方程式为______________________________________ 。
(3)实验室要除去A气体中少量E,将混和气体通过盛有__________ 的洗气瓶洗气。
(4)F、 H可相互转化,写出一种F转化为H的化学方程式:__________________ 。
(5)请设计一组实验方案检验F中阳离子:_________________________________ 。
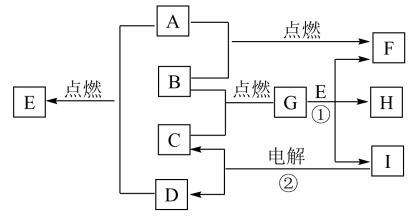
(1)写出下列物质的化学式:A
(2)反应①的离子方程式为
(3)实验室要除去A气体中少量E,将混和气体通过盛有
(4)F、 H可相互转化,写出一种F转化为H的化学方程式:
(5)请设计一组实验方案检验F中阳离子:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】铁是人类较早使用的金属之一,完成下列问题。
(1)下列铁的化合物中,可以由单质直接化合得到的是_______ (用字母代号填)。
A.Fe(OH)2 B.FeCl3 C.Fe(OH)3 D.Fe3O4
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体。
①Fe(OH)3胶体分散质粒子的直径范围是________ 。
②上述反应的离子方程式如下,请将方程式补写完整。
_____  +
+_____ H2O=______ Fe(OH)3(胶体)+_____ O2↑+____ OH-
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
①写出FeCl3溶液与金属铜发生反应的化学方程式______ 。
②某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
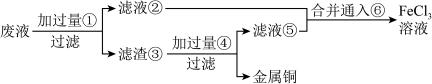
请写出上述过程中滤渣③中所含成分的化学式______ ,物质⑥的化学式______ 。
(1)下列铁的化合物中,可以由单质直接化合得到的是
A.Fe(OH)2 B.FeCl3 C.Fe(OH)3 D.Fe3O4
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体。
①Fe(OH)3胶体分散质粒子的直径范围是
②上述反应的离子方程式如下,请将方程式补写完整。
 +
+(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
①写出FeCl3溶液与金属铜发生反应的化学方程式
②某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

请写出上述过程中滤渣③中所含成分的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下图为前四周期部分元素的单质及其化合物(或其溶液)的转化关系。

已知:常温下,A、B、G、L为单质,A可用于自来水消毒,F为生活中最常见的液体,J的焰色试验呈黄色,K为红褐色沉淀,请回答下列问题:
(1)写出J的电子式___________ ;
(2)写出F和G反应的化学方程式___________ ;该反应中氧化剂化学式为___________ ;
(3)写出H转变为K的化学方程式___________ ;
(4)C溶液中阳离子的检验方法为___________ ;
(5)写出E转变为C的化学方程式,并用双线桥表示出电子转移的方向和数目___________ ;
(6)向E溶液中滴加J溶液的实验现象为___________ 。

已知:常温下,A、B、G、L为单质,A可用于自来水消毒,F为生活中最常见的液体,J的焰色试验呈黄色,K为红褐色沉淀,请回答下列问题:
(1)写出J的电子式
(2)写出F和G反应的化学方程式
(3)写出H转变为K的化学方程式
(4)C溶液中阳离子的检验方法为
(5)写出E转变为C的化学方程式,并用双线桥表示出电子转移的方向和数目
(6)向E溶液中滴加J溶液的实验现象为
您最近一年使用:0次