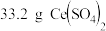在铜锌原电池中,锌板不纯时,少量氢气可以从锌板表面析出。解决方法是用棉花蘸取汞盐后擦拭锌板,在锌的表面形成锌汞齐(锌汞合金)。表面形成锌汞合金的锌板,单独浸泡在稀硫酸中,不再析出氢气,下列说法错误的是
| A.形成原电池后一定会加快氧化还原反应的速率 |
| B.锌板不纯时,析出少量氢气的原因是在锌电极上形成了原电池 |
| C.反应时,电子从Zn电极通过外电路向Cu电极转移 |
| D.负极的电极反应方程式: Zn-2e-=Zn2+ |
更新时间:2023-01-25 19:06:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是化学课外活动小组设计的用化学电源(锌铜硫酸原电池)使LED灯发光的装置示意图。下列有关该装置的说法正确的是()
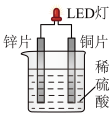

| A.铜片为负极 | B.锌片上发生还原反应 |
| C.其能量转化的形式主要是“化学能→电能→光能” | D.如果将稀硫酸换成盐酸,LED灯将不会发光 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
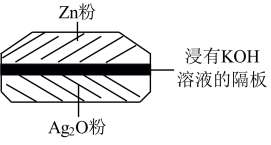
【推荐2】银锌电池是一种微型纽扣电池,总反应式为: ,其电极分别是Zn和
,其电极分别是Zn和 ,下列说法不正确的是
,下列说法不正确的是
 ,其电极分别是Zn和
,其电极分别是Zn和 ,下列说法不正确的是
,下列说法不正确的是 
| A.锌作电源的负极 |
| B.正极发生还原反应 |
C.电池工作时,电子从 经导线流向Zn 经导线流向Zn |
| D.若有0.2mol电子流经导线,则可产生银21.6g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的


| A.H+从左侧经过质子交换膜移向右侧 |
| B.该电池的负极反应式为C2H5OH+3H2O-12e-=2CO2↑+12H+ |
| C.电子经过导线由O2所在的铂电极流入 |
| D.微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的是
| 实验装置与现象 | |||
| 装置 | 甲 | 乙 | 丙 |
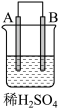 | 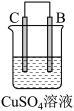 | 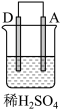 | |
| 现象 | A不断溶解 | C的质量增加 | A上有气体产生 |
| A.装置甲中的B金属是原电池的负极 | B.装置乙中的C金属是原电池的阳极 |
| C.装置丙中的D金属是原电池的正极 | D.四种金属的活泼性顺序是D>A>B>C |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】氮氧化物 会参与形成雾霾,通过NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法不正确的是
会参与形成雾霾,通过NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法不正确的是

 会参与形成雾霾,通过NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法不正确的是
会参与形成雾霾,通过NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法不正确的是
| A.Pt电极发生还原反应 |
B.整个过程的总反应为: |
C.NiO电极的电极反应式为: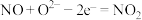 |
| D.装置工作时,电子流动的方向:NiO电极→固体电解质→Pt电极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁电池是一种新型电池,能较长时间保持稳定的放电电压,某高铁电池的工作原理如下图所示(a为离子交换膜)。下列说法正确的是
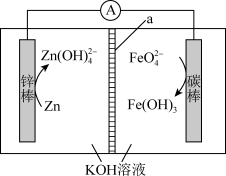

| A.电池工作时,外电路的电流方向:锌棒→碳棒 |
| B.电池工作一段时间后,负极区溶液的pH增大 |
| C.每生成1 mol Fe(OH)3,消耗Zn的质量为65 g |
D.电池正极反应式为 +3e-+4H2O=Fe(OH)3+5OH- +3e-+4H2O=Fe(OH)3+5OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列关于实验现象的描述不正确的是
| A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B.把铜片和铁片紧靠在一起浸入浓硝酸中,铁片表面出现气泡 |
| C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D.把锌粒放入盛有盐酸的试管中,加入氯化铜溶液,气泡放出速率加快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.用含有少量硫酸铜的稀硫酸跟锌粒反应,能加快产生氢气,说明Cu2+具有催化能力 |
| B.增大浓度会加快化学反应速率,是因为增加了反应物单位体积内活化分子的百分数 |
| C.等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA<HB |
| D.碱性锌锰电池是一种常见的二次电池 |
您最近一年使用:0次

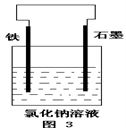
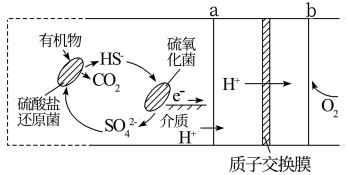
 溶液的装置如下图所示,下列说法不正确的是
溶液的装置如下图所示,下列说法不正确的是 
 电极为正极
电极为正极 由左池向右池迁移
由左池向右池迁移
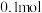 电子通过时,阳极室生成
电子通过时,阳极室生成