1984年我国研制出有效杀灭肝炎病毒的消毒液,命名为“84消毒液”。完成下列问题。
(1)实验室“84 消毒液”可通过将氯气通入冷而稀的氢氧化钠溶液获得,写出该反应的离子方程式_______ 。

(2)“84消毒液”与洁厕灵(主要成分为盐酸)混用,会产生黄绿色有毒气体。反应离子方程式为_______ ,氧化产物与还原产物的物质的量之比为_______ 。
(3)将“84 消毒液”与 同时用于织物漂白,效果不佳,原因
同时用于织物漂白,效果不佳,原因 _______ (用离子方程式表示)。
(4)高铁酸钠 是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
①某兴趣小组欲用 固体配制
固体配制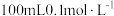 的高铁酸钠溶液,需要高铁酸钠固体的质量为
的高铁酸钠溶液,需要高铁酸钠固体的质量为_______ g 。配制所用的容量瓶上标有
。配制所用的容量瓶上标有_______ 、_______ 、刻度线。
②下列操作导致浓度偏低的是_______ 。
A.容量瓶用蒸馏水洗净之后,直接用于溶液的配制
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切
D.定容时,俯视刻度线
(1)实验室“84 消毒液”可通过将氯气通入冷而稀的氢氧化钠溶液获得,写出该反应的离子方程式

(2)“84消毒液”与洁厕灵(主要成分为盐酸)混用,会产生黄绿色有毒气体。反应离子方程式为
(3)将“84 消毒液”与
 同时用于织物漂白,效果不佳,原因
同时用于织物漂白,效果不佳,原因 (4)高铁酸钠
 是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。①某兴趣小组欲用
 固体配制
固体配制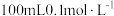 的高铁酸钠溶液,需要高铁酸钠固体的质量为
的高铁酸钠溶液,需要高铁酸钠固体的质量为 。配制所用的容量瓶上标有
。配制所用的容量瓶上标有②下列操作导致浓度偏低的是
A.容量瓶用蒸馏水洗净之后,直接用于溶液的配制
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切
D.定容时,俯视刻度线
更新时间:2023-01-25 11:02:41
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氨催化氧化法是工业生产中制取硝酸的主要途径。
(1)合成氨原料气可由以下方法得到,步骤II在催化剂作用下反应的化学方程式为:_______ 。
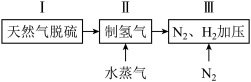
(2)以氨气、氧气为原料,在催化剂存在下生成NO和副产物 的化学方程式如下:
的化学方程式如下:
I:
II:
催化氧化时,有关物质的产率与温度的关系如图
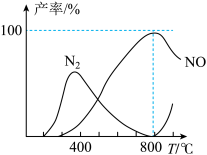
①该催化剂在低温时对反应_______ (填“I”或“II”)的选择性更好。
②温度高于800℃后,副产物 的产率增大的原因可能是
的产率增大的原因可能是_______ 。
(3)氧气与氨气的物质的量之比是影响催化氧化和后续反应的重要因素,催化氧化时加入氧气与氨气的物质的量之比应_______ (填“大于”或“等于”或“小于”)5:4,原因是_______ 。
(4)某合成氨工业废水中含有一定量的氨氮(以 、
、 形式存在),pH约为6时,用NaClO可将废水中的氨氮转化为
形式存在),pH约为6时,用NaClO可将废水中的氨氮转化为 。
。
①NaClO将废水中的 转化为
转化为 的离子方程式为
的离子方程式为_______ 。
②研究发现,当温度高于30℃时,废水中氨氮去除率随着温度升高而降低,其原因是_______ 。
(5)铁触媒(+2价铁和+3价铁组成的氧化物)是工业合成氨的催化剂。某学习小组用下列流程测定铁触媒的含铁量(25.00mL稀释后的溶液不含有 )。根据题意回答相关问题:
)。根据题意回答相关问题:
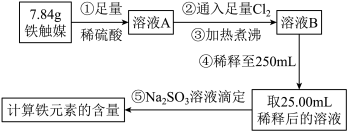
步骤⑤消耗 的
的 溶液25.00mL,则铁触媒中铁元素的质量分数为
溶液25.00mL,则铁触媒中铁元素的质量分数为_______ 。
(1)合成氨原料气可由以下方法得到,步骤II在催化剂作用下反应的化学方程式为:

(2)以氨气、氧气为原料,在催化剂存在下生成NO和副产物
 的化学方程式如下:
的化学方程式如下:I:

II:

催化氧化时,有关物质的产率与温度的关系如图

①该催化剂在低温时对反应
②温度高于800℃后,副产物
 的产率增大的原因可能是
的产率增大的原因可能是(3)氧气与氨气的物质的量之比是影响催化氧化和后续反应的重要因素,催化氧化时加入氧气与氨气的物质的量之比应
(4)某合成氨工业废水中含有一定量的氨氮(以
 、
、 形式存在),pH约为6时,用NaClO可将废水中的氨氮转化为
形式存在),pH约为6时,用NaClO可将废水中的氨氮转化为 。
。①NaClO将废水中的
 转化为
转化为 的离子方程式为
的离子方程式为②研究发现,当温度高于30℃时,废水中氨氮去除率随着温度升高而降低,其原因是
(5)铁触媒(+2价铁和+3价铁组成的氧化物)是工业合成氨的催化剂。某学习小组用下列流程测定铁触媒的含铁量(25.00mL稀释后的溶液不含有
 )。根据题意回答相关问题:
)。根据题意回答相关问题:
步骤⑤消耗
 的
的 溶液25.00mL,则铁触媒中铁元素的质量分数为
溶液25.00mL,则铁触媒中铁元素的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】84消毒液等含氯消毒剂等可有效灭活新型冠状病毒。了解这些消毒剂的制备原理、性质十分重要。
试回答下列问题:
(1)取少量84消毒液于试管中,滴几滴酚酞试液,溶液先变红后褪色,其主要原因是_______ (用离子方程式表示)。
(2)采用如图所示的简易装置可以在家中制备84消毒液。a为电源______ 极,制备84消毒液的总反应的化学方程式为_______ 。
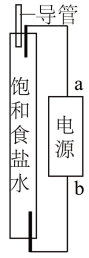
(3)盛装84消毒液宜选择塑料容器,不宜用铁器,其主要原因是________ (答2条即可)。
试回答下列问题:
(1)取少量84消毒液于试管中,滴几滴酚酞试液,溶液先变红后褪色,其主要原因是
(2)采用如图所示的简易装置可以在家中制备84消毒液。a为电源

(3)盛装84消毒液宜选择塑料容器,不宜用铁器,其主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,在疫情期间外出需戴好口罩,返家后立即杀菌消毒。含氯消毒剂在日常生产生活中有着广泛的用途。
(1)实验室除了可以用 和浓盐酸制氯气外,还可以利用如下反应制取氯气:
和浓盐酸制氯气外,还可以利用如下反应制取氯气: 。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为
。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为_______ g,其中被氧化的HCl的物质的量为_______ mol,反应过程中转移的电子数为_______  。
。
(2)“84”消毒液(有效成分为NaClO)在抗击新冠肺炎疫情战役中发挥了重要的作用。常温下,可利用氯气与烧碱溶液反应制得“84”消毒液,在使用前将“84”消毒液的稀释液放置在空气中一段时间,其漂白效果更好,原因为_______ (用离子方程式表示,已知通常情况下,弱酸不能制强酸,酸性: )。
)。
(3)二氧化氯( )是一种黄绿色的气体。可用作饮用水的消毒杀菌处理剂,是国际上公认的安全、低毒的绿色消毒剂。实验室可用
)是一种黄绿色的气体。可用作饮用水的消毒杀菌处理剂,是国际上公认的安全、低毒的绿色消毒剂。实验室可用 和浓盐酸在一定温度下反应制得:
和浓盐酸在一定温度下反应制得: 。
。
①该反应的氧化产物为_______ (填化学式)。
②在该反应中浓盐酸表现出来的性质是_______ (填标号)。
A.还原性 B.氧化性 C.酸性
③ 、
、 、
、 (还原产物为
(还原产物为 )、
)、 等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是
等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是_______ (填标号)。
A. B.
B.  C.
C. D.
D.
(1)实验室除了可以用
 和浓盐酸制氯气外,还可以利用如下反应制取氯气:
和浓盐酸制氯气外,还可以利用如下反应制取氯气: 。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为
。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为 。
。(2)“84”消毒液(有效成分为NaClO)在抗击新冠肺炎疫情战役中发挥了重要的作用。常温下,可利用氯气与烧碱溶液反应制得“84”消毒液,在使用前将“84”消毒液的稀释液放置在空气中一段时间,其漂白效果更好,原因为
 )。
)。(3)二氧化氯(
 )是一种黄绿色的气体。可用作饮用水的消毒杀菌处理剂,是国际上公认的安全、低毒的绿色消毒剂。实验室可用
)是一种黄绿色的气体。可用作饮用水的消毒杀菌处理剂,是国际上公认的安全、低毒的绿色消毒剂。实验室可用 和浓盐酸在一定温度下反应制得:
和浓盐酸在一定温度下反应制得: 。
。①该反应的氧化产物为
②在该反应中浓盐酸表现出来的性质是
A.还原性 B.氧化性 C.酸性
③
 、
、 、
、 (还原产物为
(还原产物为 )、
)、 等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是
等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是A.
 B.
B.  C.
C. D.
D.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】据报道,日常生活中,将洁厕液与84消毒液混合使用会发生中毒的事故。
1.两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是_______ ,写出氯原子最外层电子排布的轨道表示式_____________ 。
2.84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式______ .若将84消毒液长期露置于空气中,溶液中的主要成分将变为________ 。(填化学式)
3.洁厕灵的主要成分是HCl。下列关于卤化氢的性质比较中错误的是____
A. 酸性:HF>HCl>HBr>HI
B. 键能:H—F>H—Cl>H—Br>H—I
C. 熔点:HF<HCl<HBr<HI
D. 还原性:HF<HCl<HBr<HI
4.洁厕液与84消毒液混合后会发生氧化还原反应,生成有毒的氯气。写出该反应的离子方程式____ 。
5.下列氧化还原反应中,与上述反应类型不同的是____
A. Na2S2O3+ H2SO4 → Na2SO4+ S + SO2+ H2O
B. 2FeCl3+ Fe → 2FeCl2
C. S + 2H2SO4(浓) 3SO2+ 2H2O
3SO2+ 2H2O
D. KClO3+ 5KCl + 3H2SO4 → 3K2SO4 + 3Cl2 + 3H2O
6.若以物质单位质量得到的电子数衡量物质的消毒效率,则下列常用的消毒剂中,消毒效率最高的是____
A. NaClO B. ClO2 C. Cl2 D. Ca(ClO)2
1.两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是
2.84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式
3.洁厕灵的主要成分是HCl。下列关于卤化氢的性质比较中错误的是
A. 酸性:HF>HCl>HBr>HI
B. 键能:H—F>H—Cl>H—Br>H—I
C. 熔点:HF<HCl<HBr<HI
D. 还原性:HF<HCl<HBr<HI
4.洁厕液与84消毒液混合后会发生氧化还原反应,生成有毒的氯气。写出该反应的离子方程式
5.下列氧化还原反应中,与上述反应类型不同的是
A. Na2S2O3+ H2SO4 → Na2SO4+ S + SO2+ H2O
B. 2FeCl3+ Fe → 2FeCl2
C. S + 2H2SO4(浓)
 3SO2+ 2H2O
3SO2+ 2H2OD. KClO3+ 5KCl + 3H2SO4 → 3K2SO4 + 3Cl2 + 3H2O
6.若以物质单位质量得到的电子数衡量物质的消毒效率,则下列常用的消毒剂中,消毒效率最高的是
A. NaClO B. ClO2 C. Cl2 D. Ca(ClO)2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求书写下列反应的离子方程式。
(1)通常用饱和NaHCO3溶液除去混在CO2中少量的HCl气体,其反应的离子方程式为_______ ;
(2)用氢氧化钠溶液和氯气反应制备84消毒液,反应的离子方程式是_______ 。
(3)若将84消毒液与洁厕灵(通常含盐酸)混合使用,则会产生黄绿色的有毒气体,该反应的离子方程式是_______ 。
(4)锌粒投入稀H2SO4中,溶液里氢离子的量减少,锌离子的量增加,反应的离子方程式是_______ 。
(5)过氧化钠与水反应会产生氧气,写出该反应的离子方程式_______ 。
(1)通常用饱和NaHCO3溶液除去混在CO2中少量的HCl气体,其反应的离子方程式为
(2)用氢氧化钠溶液和氯气反应制备84消毒液,反应的离子方程式是
(3)若将84消毒液与洁厕灵(通常含盐酸)混合使用,则会产生黄绿色的有毒气体,该反应的离子方程式是
(4)锌粒投入稀H2SO4中,溶液里氢离子的量减少,锌离子的量增加,反应的离子方程式是
(5)过氧化钠与水反应会产生氧气,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氯元素的单质及其化合物在生产、生活中均有重要用途。请结合相关知识回答下列问题:
(1)84消毒液能有效杀灭新冠病毒,其主要成分为NaClO,在常温下,将氯气通入烧碱中可以得到NaClO,写出该反应的离子方程式___________ ,使用说明中特别提醒84消毒液不可与洁厕灵(主要成分盐酸)混合使用,否则会产生 ,请用离子方程式表示其原因
,请用离子方程式表示其原因___________ 。
(2)世界卫生组织(WHO)和中国卫健委公认二氧化氯( )为新时代绿色消毒剂。工业上可采用
)为新时代绿色消毒剂。工业上可采用 与氯酸钠在硫酸存在的条件下反应制取
与氯酸钠在硫酸存在的条件下反应制取 ,并生成
,并生成 ,写出工业上制取
,写出工业上制取 反应的化学方程式
反应的化学方程式___________ ,该反应中氧化剂与还原剂物质的量之比为___________ 。
(3)现测定二氧化氯漂白液的浓度。步骤如下:量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再加入硫酸和10%碘化钾10mL,此时溶液出现棕色(发生反应: ,然后再逐滴滴入0.12
,然后再逐滴滴入0.12 硫代硫酸钠溶液15mL,恰好完全反应(发生反应:
硫代硫酸钠溶液15mL,恰好完全反应(发生反应: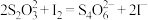 ,计算该漂白液中二氧化氯的物质的量浓度:
,计算该漂白液中二氧化氯的物质的量浓度:___________ 。
(4)实验室要配制1L 0.2 的NaClO溶液。配制过程如下:
的NaClO溶液。配制过程如下:
①将已恢复至室温的溶液沿玻璃棒注入1L容量瓶中。
②盖好容量瓶瓶塞,反复上下颠倒,摇匀。
③用天平准确称取14.9g的NaClO固体并放入烧杯中,加入约30mL的蒸馏水充分搅拌、溶解。
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡。
⑤定容。
⑥将配置好的溶液倒入试剂瓶中,贴好标签。
实验操作顺序依次为___________ (填序号),定容的具体操作是___________ 。
(1)84消毒液能有效杀灭新冠病毒,其主要成分为NaClO,在常温下,将氯气通入烧碱中可以得到NaClO,写出该反应的离子方程式
 ,请用离子方程式表示其原因
,请用离子方程式表示其原因(2)世界卫生组织(WHO)和中国卫健委公认二氧化氯(
 )为新时代绿色消毒剂。工业上可采用
)为新时代绿色消毒剂。工业上可采用 与氯酸钠在硫酸存在的条件下反应制取
与氯酸钠在硫酸存在的条件下反应制取 ,并生成
,并生成 ,写出工业上制取
,写出工业上制取 反应的化学方程式
反应的化学方程式(3)现测定二氧化氯漂白液的浓度。步骤如下:量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再加入硫酸和10%碘化钾10mL,此时溶液出现棕色(发生反应:
 ,然后再逐滴滴入0.12
,然后再逐滴滴入0.12 硫代硫酸钠溶液15mL,恰好完全反应(发生反应:
硫代硫酸钠溶液15mL,恰好完全反应(发生反应: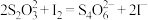 ,计算该漂白液中二氧化氯的物质的量浓度:
,计算该漂白液中二氧化氯的物质的量浓度:(4)实验室要配制1L 0.2
 的NaClO溶液。配制过程如下:
的NaClO溶液。配制过程如下:①将已恢复至室温的溶液沿玻璃棒注入1L容量瓶中。
②盖好容量瓶瓶塞,反复上下颠倒,摇匀。
③用天平准确称取14.9g的NaClO固体并放入烧杯中,加入约30mL的蒸馏水充分搅拌、溶解。
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡。
⑤定容。
⑥将配置好的溶液倒入试剂瓶中,贴好标签。
实验操作顺序依次为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】欲配制1mol/L的氢氧化钠溶液250mL,完成下列步骤:
(1)用天平称取氢氧化钠固体_______ g。
(2)将称好的氢氧化钠固体放入_______ 中,加蒸馏水将其溶解,待冷却后将溶液沿_______ 移入_______ 中。
(3)用少量蒸馏水冲洗玻璃棒和烧杯2~3次,将冲洗液移入_______ 中,在操作过程中不损失点滴液体,否则会使溶液的浓度偏_______ (高或低)。
(4)向容量瓶内加水至刻度线_______ 时,改用_______ 小心地加水至溶液凹液面与刻度线相切,若加水超过刻度线,会造成溶液浓度_______ ,应该_______ 。
(1)用天平称取氢氧化钠固体
(2)将称好的氢氧化钠固体放入
(3)用少量蒸馏水冲洗玻璃棒和烧杯2~3次,将冲洗液移入
(4)向容量瓶内加水至刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某化学兴趣小组进行硫酸性质的实验探究时,需要 的稀
的稀 。请回答下列问题:
。请回答下列问题:
(1)实验室欲用98%的浓 (密度为
(密度为 )来配制,经计算需要
)来配制,经计算需要___________ mL(保留一位小数)浓硫酸,在量取时宜选用下列量筒中的___________ 。
A.5mL B.10mL C.25mL D.50mL
(2)实验中所用的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还有___________ 。
(3)在量取浓硫酸后,进行了下列操作:
①等稀释的硫酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③将量取的浓硫酸稀释。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)___________ 。第③步中稀释浓硫酸的操作是___________ 。
(4)下列哪些操作会引起所配溶液浓度偏大___________ (填写字母)。
A.容量瓶底部有蒸馏水未干燥即用来配制溶液
B.硫酸在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
C.往容量瓶转移时,有少量液体溅出
D.在容量瓶中定容时俯视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
 的稀
的稀 。请回答下列问题:
。请回答下列问题:(1)实验室欲用98%的浓
 (密度为
(密度为 )来配制,经计算需要
)来配制,经计算需要A.5mL B.10mL C.25mL D.50mL
(2)实验中所用的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还有
(3)在量取浓硫酸后,进行了下列操作:
①等稀释的硫酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③将量取的浓硫酸稀释。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)
(4)下列哪些操作会引起所配溶液浓度偏大
A.容量瓶底部有蒸馏水未干燥即用来配制溶液
B.硫酸在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
C.往容量瓶转移时,有少量液体溅出
D.在容量瓶中定容时俯视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】分类是认识和研究物质及其变化的一种常用的科学方法。依据物质类别和元素价态可以对物质的性质进行解释和预测。
(1) 与NaOH溶液反应的离子方程式为
与NaOH溶液反应的离子方程式为_______ 。
(2)某同学购买了一瓶“威露士”牌“84"消毒液,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如图信息:
①该“84”消毒液的物质的量浓度约为_______ 。
②某同学取100mL该“84”消毒液,稀释后100倍用于消毒,稀释后的溶液中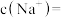
_______  。
。
③“84”消毒液与稀硫酸混合使用可增强消毒能力,其发生的化学反应符合规律:_______ +_______ =_______ + _______ (填物质类别)。某消毒小组人员用98%的浓硫酸配制250mL 的稀硫酸用于增强“84”消毒液的消毒能力。在下列配制过程示意图中,错误的是
的稀硫酸用于增强“84”消毒液的消毒能力。在下列配制过程示意图中,错误的是_______ (填选项字母)。
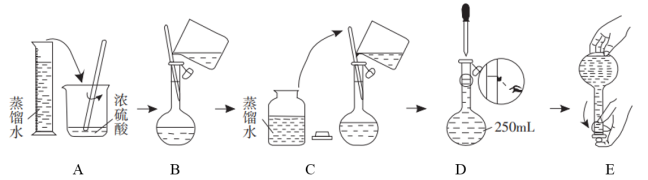
对所配制的稀硫酸进行标定,发现其浓度小于 ,引起误差的原因可能为
,引起误差的原因可能为_______ (填选项字母)。
A.定容时,俯视刻度线
B.转移溶液后,未洗涤烧杯和玻璃棒
C.容量瓶在使用前未干燥,里面有少量蒸馏水
D.定容摇匀后,发现液面低于容量瓶的刻度线,再加水至刻度线
(3)“84”消毒液不能与洁厕灵(含盐酸)混用,混用会发生如下反应:
 。
。
①该反应中起氧化作用的微粒是_______ 。
②若反应中生成了0.01 mol ,转移电子的物质的量为
,转移电子的物质的量为_______ mol。
(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO将 氧化,产生的
氧化,产生的 促进藻类快速生长,该反应说明氧化性:NaClO
促进藻类快速生长,该反应说明氧化性:NaClO_______  (填“>”或“<”)。
(填“>”或“<”)。
资料:人们常用“84”消毒液进行消毒。“84”消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。“84”消毒液呈无色或淡黄色,可由 与NaOH溶液反应制得,其主要成分为NaClO、NaCl。 与NaOH溶液反应制得,其主要成分为NaClO、NaCl。 |
 与NaOH溶液反应的离子方程式为
与NaOH溶液反应的离子方程式为(2)某同学购买了一瓶“威露士”牌“84"消毒液,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如图信息:
| “84”消毒液 有效成分:NaClO 规格:1000mL 质量分数:25% 密度:  |
②某同学取100mL该“84”消毒液,稀释后100倍用于消毒,稀释后的溶液中
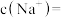
 。
。③“84”消毒液与稀硫酸混合使用可增强消毒能力,其发生的化学反应符合规律:
 的稀硫酸用于增强“84”消毒液的消毒能力。在下列配制过程示意图中,错误的是
的稀硫酸用于增强“84”消毒液的消毒能力。在下列配制过程示意图中,错误的是
对所配制的稀硫酸进行标定,发现其浓度小于
 ,引起误差的原因可能为
,引起误差的原因可能为A.定容时,俯视刻度线
B.转移溶液后,未洗涤烧杯和玻璃棒
C.容量瓶在使用前未干燥,里面有少量蒸馏水
D.定容摇匀后,发现液面低于容量瓶的刻度线,再加水至刻度线
(3)“84”消毒液不能与洁厕灵(含盐酸)混用,混用会发生如下反应:

 。
。①该反应中起氧化作用的微粒是
②若反应中生成了0.01 mol
 ,转移电子的物质的量为
,转移电子的物质的量为(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO将
 氧化,产生的
氧化,产生的 促进藻类快速生长,该反应说明氧化性:NaClO
促进藻类快速生长,该反应说明氧化性:NaClO (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次



