根据要求回答下列问题。
(1)在标准状况下,①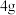
 ②
②
 ③
③
 中,含原子数最多的是
中,含原子数最多的是_______ (填序号),体积最小的是_______ (填序号)。
(2)现有由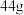
 和
和
 组成的混合气体,该混合气体中的
组成的混合气体,该混合气体中的 和
和 物质的量之比为
物质的量之比为_______ ,该混合气体的平均摩尔质量为_______ (保留一位小数)。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打受热分解的化学方程式:_______ 。
(4)84消毒液(主要成分是 )和洁厕灵(主要成分是
)和洁厕灵(主要成分是 )同时使用时生成有毒气体,用离子方程式表示该反应
)同时使用时生成有毒气体,用离子方程式表示该反应_______ 。
(5)某溶液中有 、
、 、
、 、
、 等离子,向其中加入足量的
等离子,向其中加入足量的 后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。
后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。
(1)在标准状况下,①
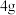
 ②
②
 ③
③
 中,含原子数最多的是
中,含原子数最多的是(2)现有由
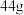
 和
和
 组成的混合气体,该混合气体中的
组成的混合气体,该混合气体中的 和
和 物质的量之比为
物质的量之比为(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打受热分解的化学方程式:
(4)84消毒液(主要成分是
 )和洁厕灵(主要成分是
)和洁厕灵(主要成分是 )同时使用时生成有毒气体,用离子方程式表示该反应
)同时使用时生成有毒气体,用离子方程式表示该反应(5)某溶液中有
 、
、 、
、 、
、 等离子,向其中加入足量的
等离子,向其中加入足量的 后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。
后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。A. | B. | C. 和 和 | D. |
更新时间:2023-02-02 14:44:22
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)在标准状况下,1.7gNH3所占的体积约为___ L,它与标准状况__ LH2S含有相同数目的氢原子。
(2)质量之比为8∶7∶6的三种气体SO2、CO、NO,其分子数之比为__ ;氧原子数之比为__ ;相同条件下的体积之比为__ 。
(3)已知由CH4和O2组成的混合气体质量为12g,在标准状况下为11.2L,该混合气体的平均摩尔质量是__ ,混合气体中CH4和O2的物质的量之比为__ 。
(2)质量之比为8∶7∶6的三种气体SO2、CO、NO,其分子数之比为
(3)已知由CH4和O2组成的混合气体质量为12g,在标准状况下为11.2L,该混合气体的平均摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】混合气体由 和
和 组成,测得混合气体在标准状况下的密度为
组成,测得混合气体在标准状况下的密度为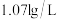 ,则混合气体中
,则混合气体中 和
和 的体积比为
的体积比为__________ 。
 和
和 组成,测得混合气体在标准状况下的密度为
组成,测得混合气体在标准状况下的密度为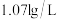 ,则混合气体中
,则混合气体中 和
和 的体积比为
的体积比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】氯化亚铜(CuCl)广泛用于有机合成、气体吸收、冶金、医药化工等行业。
(1)工业上氯化亚铜可由下列反应制备:
2CuSO4+ Na2SO3 + 2NaCl + Na2CO3® 2CuCl ↓+ 3Na2SO4 + CO2↑。制备过程中需要20% 的CuSO4溶液,配制100g 该CuSO4溶液需要胆矾__________ g,需要水_________ g。
(2)实验室可用如下方法制备少量CuCl:取10mL 0.2mol/L CuCl2溶液,加入0.128g铜屑和36.5%的浓盐酸(密度为1.2g/mL)3mL,在密闭容器中加热,充分反应后,得到无色溶液A;将溶液A全部倾入水中,可得到白色的氯化亚铜沉淀。已知溶液A中只含氢离子和两种阴离子(不考虑水的电离),其中,n(H+)=0.036mol、n(Cl–)=0.032mol。请通过分析和计算,确定溶液A中另一阴离子的化学式和物质的量_____________ 。
(3)由CO2、O2、CO、N2组成的混合气体1.008L,测得其密度为1.429g/L,将该气体依次通过足量的30%KOH溶液、氯化亚铜氨溶液(可完全吸收O2和CO) (假定每一步反应都能进行完全),使上述液体分别增加0.44g、0.44g(体积和密度均在标准状况下测定)。
①该混合气体的摩尔质量是_______ g/mol;混合气体中n(CO2): n(CO和N2) =_______ 。
列式计算:
②混合气体中CO的质量是____________ 。
③最后剩余气体的体积是______________ 。
(1)工业上氯化亚铜可由下列反应制备:
2CuSO4+ Na2SO3 + 2NaCl + Na2CO3® 2CuCl ↓+ 3Na2SO4 + CO2↑。制备过程中需要20% 的CuSO4溶液,配制100g 该CuSO4溶液需要胆矾
(2)实验室可用如下方法制备少量CuCl:取10mL 0.2mol/L CuCl2溶液,加入0.128g铜屑和36.5%的浓盐酸(密度为1.2g/mL)3mL,在密闭容器中加热,充分反应后,得到无色溶液A;将溶液A全部倾入水中,可得到白色的氯化亚铜沉淀。已知溶液A中只含氢离子和两种阴离子(不考虑水的电离),其中,n(H+)=0.036mol、n(Cl–)=0.032mol。请通过分析和计算,确定溶液A中另一阴离子的化学式和物质的量
(3)由CO2、O2、CO、N2组成的混合气体1.008L,测得其密度为1.429g/L,将该气体依次通过足量的30%KOH溶液、氯化亚铜氨溶液(可完全吸收O2和CO) (假定每一步反应都能进行完全),使上述液体分别增加0.44g、0.44g(体积和密度均在标准状况下测定)。
①该混合气体的摩尔质量是
列式计算:
②混合气体中CO的质量是
③最后剩余气体的体积是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】实验室用8.7 gMnO2与100 mL 12mol/L的浓盐酸(足量)反应制氯气,试计算:
(1)在标准状况下,生成氯气的体积__________ 。(不考虑氯气在溶液中的溶解)
(2)将反应后的溶液加水稀释到500 mL,向从其中取出的50 mL溶液中加入足量AgNO3溶液,生成沉淀的物质的量__________ 。(要求写出计算过程)
(1)在标准状况下,生成氯气的体积
(2)将反应后的溶液加水稀释到500 mL,向从其中取出的50 mL溶液中加入足量AgNO3溶液,生成沉淀的物质的量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】实验室可用如下反应制取氯气,反应原理如下: 2KMnO4 + 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O
(1)用单线桥表示出上述反应中电子转移的方向和数目_________
(2)上述反应中氧化剂与还原剂的物质的量比_________
(3)15.8g KMnO4能使_________ 克HCl被氧化?
(4)产生的Cl2在标准状况下的体积为_________ ?
(1)用单线桥表示出上述反应中电子转移的方向和数目
(2)上述反应中氧化剂与还原剂的物质的量比
(3)15.8g KMnO4能使
(4)产生的Cl2在标准状况下的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】将可能混有NaOH的16.80gNaHCO3固体,在200℃条件下充分加热,排出反应产生的气体,得到固体的质量为bg。
(1)b的最小值为___________ 。
(2)当b=____________ 时,产物中水的质量最多。
(1)b的最小值为
(2)当b=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】取一定量碳酸钠和碳酸氢钠的固体混合物样品,分成两等份,取其中一份加热到质量不再改变,冷却后称其质量减少6.2g,另一份样品溶于水,向所得溶液中逐滴加入200mL稀盐酸时产生CO22.24L,过量时产生CO211.2L(气体体积均为标准状况)
(1)每份样品中碳酸氢钠的物质的量为:_______ 。
(2)盐酸物质的量浓度为:_______ mol/L
(1)每份样品中碳酸氢钠的物质的量为:
(2)盐酸物质的量浓度为:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】为测定某补血剂样品[主要成分是硫酸亚铁晶体(FeSO4·7HO,M=278gmol-1)]中铁元素的含量,某化学兴趣小组设计了如下实验方案。取10片补血剂,加入一定量稀硫酸溶解后,配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.00500mol·L-1酸性KMnO4溶液滴定,重复实验平均消耗酸性KMnO4溶液10.00mL。已知滴定过程反应的离子方程式为:MnO +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O
(1)若实验无损耗,则每片补血剂含FeSO4·7H2O含量为____ mg(列式计算)。
(2)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天最少需服用含FeSO4·7H2O的片剂____ 片。
 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O(1)若实验无损耗,则每片补血剂含FeSO4·7H2O含量为
(2)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天最少需服用含FeSO4·7H2O的片剂
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】计算:
(1)将铁的某种氧化物投入到 的盐酸中,在一定条件下恰好完全溶解,所得溶液再通入0.56 L标准状况下的氯气时,刚好使溶液中
的盐酸中,在一定条件下恰好完全溶解,所得溶液再通入0.56 L标准状况下的氯气时,刚好使溶液中 完全转化为
完全转化为 ,则该氧化物的化学式为
,则该氧化物的化学式为_______ 。
(2)向含4 mol 的稀溶液中,逐渐加入铁粉至过量。假设生成的气体只有一种,得到的
的稀溶液中,逐渐加入铁粉至过量。假设生成的气体只有一种,得到的 的物质的量与所加铁粉的物质的量的关系如图所示。则B点消耗铁的物质的量为
的物质的量与所加铁粉的物质的量的关系如图所示。则B点消耗铁的物质的量为_______ mol,C点生成 的物质的量为
的物质的量为_______ mol。

(1)将铁的某种氧化物投入到
 的盐酸中,在一定条件下恰好完全溶解,所得溶液再通入0.56 L标准状况下的氯气时,刚好使溶液中
的盐酸中,在一定条件下恰好完全溶解,所得溶液再通入0.56 L标准状况下的氯气时,刚好使溶液中 完全转化为
完全转化为 ,则该氧化物的化学式为
,则该氧化物的化学式为(2)向含4 mol
 的稀溶液中,逐渐加入铁粉至过量。假设生成的气体只有一种,得到的
的稀溶液中,逐渐加入铁粉至过量。假设生成的气体只有一种,得到的 的物质的量与所加铁粉的物质的量的关系如图所示。则B点消耗铁的物质的量为
的物质的量与所加铁粉的物质的量的关系如图所示。则B点消耗铁的物质的量为 的物质的量为
的物质的量为
您最近一年使用:0次



