根据①~⑩元素的编号所在周期表中的位置,用相应的元素符号回答有关问题:
(1)其单质与氧气反应生成淡黄色固体化合物,该化合物的化学式是_______ ,该化合物与二氧化碳反应的化学方程式是_______ 。
(2)通常显+1价的非金属元素是_______ (填化学式,下同)。
(3)最难形成简单离子的元素是_______ 。
(4)其中一种金属单质能和冷水剧烈反应的反应方程式:_______ 。
(5)其中气态氢化物稳定性最强的是_______ (填氢化物化学式)。
(6)气态氢化物可与其最高价含氧酸反应,该元素是_______ (填化学式)。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 3 | ⑧ | ⑨ | ⑩ |
(2)通常显+1价的非金属元素是
(3)最难形成简单离子的元素是
(4)其中一种金属单质能和冷水剧烈反应的反应方程式:
(5)其中气态氢化物稳定性最强的是
(6)气态氢化物可与其最高价含氧酸反应,该元素是
更新时间:2023-02-07 10:51:03
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】元素周期表部分结构如下,根据表中给出的6种元素,按要求作答:
(1)元素Z的原子结构示意图为___________ 。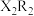 的电子式为
的电子式为___________ 。
(2)R、Y、T所形成的简单离子半径由大到小顺序为___________ (用离子符号表示)。
(3)R、T的简单气态氢化物中,较稳定的是___________ (填化学式,下同),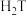 溶液在空气中变质的化学方程式为
溶液在空气中变质的化学方程式为___________ 。
(4)最高价氧化物对应水化物中,酸性最强的是___________ (填化学式)。
(5)Y与Q形成的化合物类型为___________ (填“离子化合物”或“共价化合物”)。
(6)Z的氧化物与Y的最高价氧化物对应水化物反应的离子方程式为_______ 。
(7)不能说明非金属性R强于T的事实是_______ 。
A.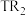 中T元素显正价
中T元素显正价
B. 的沸点比
的沸点比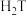 的沸点高
的沸点高
C.R、T的单质与 反应分别生成
反应分别生成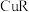 与
与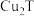
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | X | |||||||
| 2 | R | |||||||
| 3 | Y | Z | T | Q | ||||
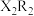 的电子式为
的电子式为(2)R、Y、T所形成的简单离子半径由大到小顺序为
(3)R、T的简单气态氢化物中,较稳定的是
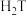 溶液在空气中变质的化学方程式为
溶液在空气中变质的化学方程式为(4)最高价氧化物对应水化物中,酸性最强的是
(5)Y与Q形成的化合物类型为
(6)Z的氧化物与Y的最高价氧化物对应水化物反应的离子方程式为
(7)不能说明非金属性R强于T的事实是
A.
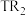 中T元素显正价
中T元素显正价B.
 的沸点比
的沸点比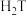 的沸点高
的沸点高C.R、T的单质与
 反应分别生成
反应分别生成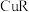 与
与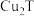
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】联合国大会将2019年定为“化学元素周期表国际年”,表明了元素周期律的重要性。以下短周期主族元素中,含元素a的化合物被广泛用于制作手机电池,古迪纳夫因在该领域做出了杰出贡献荣获2019年诺贝尔化学奖。
(1)a原子结构示意图为___________ 。
(2)b、c、d三种元素的气态氢化物中,其中最稳定的是___________ (写化学式)。
(3)元素e与c能形成一种淡黄色物质,该物质与二氧化碳反应方程式为___________ 。
(4)元素g的单质与NaOH溶液反应的离子方程式为___________ 。
(5)上表所标元素的最高价氧化物对应水化物酸性最强的是___________ (写化学式,下同),碱性最强的是 ___________ 。
(6)科学家在研究元素周期表时,预言了在元素h的下一周期存在一种“类h”元素,该元素多年后被德国化学家文克勒发现,命名为锗(Ge),锗在周期表的位置为___________ 。预测h、Ge与氢气较难反应的是___________ (填元素名称)
(7)关于a原子结构和性质的判断如下:
①与H2O反应比Na剧烈;
②它的原子半径比Na小;
③它的氧化物暴露在空气中易吸收CO2;
④它的阳离子最外层电子数和钠离子的最外层电子数相同;
⑤它是还原剂;
⑥a单质应保存在煤油中,以隔绝空气;
⑦a单质在空气中燃烧生成过氧化物。
其中上述说法错误的是_____
| a | … | b | c | d | |||
| e | … | g | h | j |
(2)b、c、d三种元素的气态氢化物中,其中最稳定的是
(3)元素e与c能形成一种淡黄色物质,该物质与二氧化碳反应方程式为
(4)元素g的单质与NaOH溶液反应的离子方程式为
(5)上表所标元素的最高价氧化物对应水化物酸性最强的是
(6)科学家在研究元素周期表时,预言了在元素h的下一周期存在一种“类h”元素,该元素多年后被德国化学家文克勒发现,命名为锗(Ge),锗在周期表的位置为
(7)关于a原子结构和性质的判断如下:
①与H2O反应比Na剧烈;
②它的原子半径比Na小;
③它的氧化物暴露在空气中易吸收CO2;
④它的阳离子最外层电子数和钠离子的最外层电子数相同;
⑤它是还原剂;
⑥a单质应保存在煤油中,以隔绝空气;
⑦a单质在空气中燃烧生成过氧化物。
其中上述说法错误的是
| A.①④⑥⑦ | B.①②③ | C.③⑤⑥ | D.①②⑦ |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知A、B、C、D、E是短周期的5种元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出B、D元素的名称:B______________ ,D______________ 。
(2)画出C元素的离子结构示意图_____________________________ 。
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式_________ 。
(4)A、B、C三种元素形成的化合物为_____________________ , 所含的化学键类型为_______________________ 。
(5)B、C、D三种元素的离子半径由大到小的排列顺序为__________________ (用离子符号表示)。
(1)请写出B、D元素的名称:B
(2)画出C元素的离子结构示意图
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式
(4)A、B、C三种元素形成的化合物为
(5)B、C、D三种元素的离子半径由大到小的排列顺序为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】现有部分短周期元素的性质或原子结构如下表:
根据上述信息进行判断,并回答下列问题:
(1)元素W在元素周期表中的位置是___________ 。
(2)元素X的一种同位素可测定文物的年代,这种同位素的符号是___________ 。
(3)元素Y与氢元素形成一种离子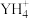 ,如何检验某溶液中含该离子:
,如何检验某溶液中含该离子:___________ 。
(4)元素Z与元素W相比,金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ (填字母)。
a.Z单质的熔点比W单质的低
b.Z的化合价比W的低
c.常温下Z单质与水反应的程度很剧烈,而W单质在加热条件下才能与水反应
d.Z的最高价氧化物对应的水化物的碱性比W的强
(5)由上述元素中的X、Y、Z组成的某剧毒化合物ZXY不慎泄漏时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,该反应的化学方程式为___________ 。
| T | 地壳中含量最多的元素 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下,单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | M层比K层少1个电子 |
| W | 其离子是第三周期金属元素的离子中半径最小的 |
(1)元素W在元素周期表中的位置是
(2)元素X的一种同位素可测定文物的年代,这种同位素的符号是
(3)元素Y与氢元素形成一种离子
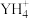 ,如何检验某溶液中含该离子:
,如何检验某溶液中含该离子:(4)元素Z与元素W相比,金属性较强的是
a.Z单质的熔点比W单质的低
b.Z的化合价比W的低
c.常温下Z单质与水反应的程度很剧烈,而W单质在加热条件下才能与水反应
d.Z的最高价氧化物对应的水化物的碱性比W的强
(5)由上述元素中的X、Y、Z组成的某剧毒化合物ZXY不慎泄漏时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】2021年10月16日,神舟十三号载人飞船与“天和”核心舱成功径向交会对接。化学助力我国航天事业发展,借助元素周期表可以认识各种材料的组成、结构和性质。a~h8种元素在元素周期表中的位置如下:
(1)液态a单质和液态d单质可用作火箭推进剂,二者反应的化学方程式为___________ 。常温下,与a单质更容易反应的是___________ (填“c”或“d”或“e”)单质。
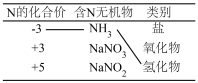
(2)空间站再生式生活保障系统能将尿液处理得到再生水,再生水后处理需除去残留的有机物和含N无机物。按示例,在答题卡相应位置补齐连线。_________
(3)我国科学家自主研发了用于航空航天的f合金材料。f原子的核外电子排布为___________ ;h最高价氧化物对应的水化物的稀溶液,与f的最高价氧化物反应的离子方程式为___________ 。
(4)g单质在太阳能电池和芯片制造等领域有着重要应用。g最高价氧化物的化学式为___________ ;b和g组成的化合物可作为新型陶瓷材料,其化学式为___________ 。上述g的两种化合物含有的化学键类型均为___________ 。
| 周期 | ⅠA | 0 | |||||||
| 1 | a | ⅡA | … | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | b | c | d | e | |||||
| 3 | f | g | h | ||||||
(2)空间站再生式生活保障系统能将尿液处理得到再生水,再生水后处理需除去残留的有机物和含N无机物。按示例,在答题卡相应位置补齐连线。

(3)我国科学家自主研发了用于航空航天的f合金材料。f原子的核外电子排布为
(4)g单质在太阳能电池和芯片制造等领域有着重要应用。g最高价氧化物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】如图为元素周期表的一部分,请参照元素①~②在图中的位置,回答下列问题。
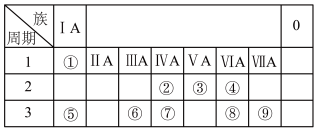
(1)第三周期元素中非金属性最强的元素的原子结构示意图是______ 。
(2)②③⑦最高价氧化物对应水化物的酸性由强到弱的顺序是______ (填化学式)。
(3)下列可以判断⑤和⑥金属性强弱的是______ (填序号)。
a.单质的熔点:⑤<⑥
b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥
d.最高价氧化物对应水化物的碱性:⑤>⑥
(4)为验证第Ⅵ 族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
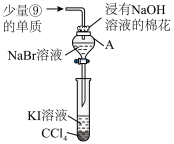
①仪器 的名称是
的名称是______ , 中发生反应的离子方程式是
中发生反应的离子方程式是__________________ 。
②棉花中浸有 溶液的作用是
溶液的作用是__________________ (用离子方程式表示)。
③验证溴与碘的非金属性强弱:通入少量⑨的单质,充分反应后,将 中液体滴入试管内,取下试管,充分振荡、静置,可观察到
中液体滴入试管内,取下试管,充分振荡、静置,可观察到______ 。该实验必须控制②单质的加入量,否则得不出溴的非金属性比碘强的结论,理由是__________________ 。
④第Ⅵ 族元素非金属性随元素核电荷数的增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐
族元素非金属性随元素核电荷数的增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐______ (填“增大”或“减小”),得电子能力逐渐减弱。

(1)第三周期元素中非金属性最强的元素的原子结构示意图是
(2)②③⑦最高价氧化物对应水化物的酸性由强到弱的顺序是
(3)下列可以判断⑤和⑥金属性强弱的是
a.单质的熔点:⑤<⑥
b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥
d.最高价氧化物对应水化物的碱性:⑤>⑥
(4)为验证第Ⅵ
 族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
①仪器
 的名称是
的名称是 中发生反应的离子方程式是
中发生反应的离子方程式是②棉花中浸有
 溶液的作用是
溶液的作用是③验证溴与碘的非金属性强弱:通入少量⑨的单质,充分反应后,将
 中液体滴入试管内,取下试管,充分振荡、静置,可观察到
中液体滴入试管内,取下试管,充分振荡、静置,可观察到④第Ⅵ
 族元素非金属性随元素核电荷数的增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐
族元素非金属性随元素核电荷数的增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】J、L、M、R、T 是原子序数依次增大的短周期主族元素,J、R 在周期表中的相对位置如表; J 原子最外层电子数是其内层电子数的 2 倍;L 的最简单气态氢化物甲的水溶液显碱性;M 是地壳中含量最多的金属元素。
(1)M 的离子结构示意图为_______ ;元素 T 在周期表中位于第________ 周期第_______ 族。
(2)J 元素是_________ (用元素符号表示);J 和氢组成的 10 电子化合物的化学式为_________ 。
(3)M 和 T 形成的化合物属于_______ (填“离子化合物”、或“共价化合物”),其中所有原 子都满足最外层 8 电子结构的分子是_______ (填化学式),电子式为_______ 。
(4)元素 M 形成的简单离子的水溶液与甲的水溶液反应的离子方程式_______ 。
J | ||||
R |
(2)J 元素是
(3)M 和 T 形成的化合物属于
(4)元素 M 形成的简单离子的水溶液与甲的水溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
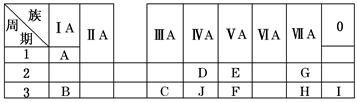
(1)表中元素,化学性质最不活泼的是________ ,只有负价而无正价的元素是________ 。
(2)C元素在元素周期表中的位置是第三周期第________ 族。
(3)最高价氧化物的水化物酸性最强的是________ ,呈两性的是________ 。
(4)A分别与E、G、H形成的化合物中,最稳定的是________ 。
(5)在B、C、E、F中,原子半径最大的是________ 。
(6)B、H两种元素所形成的化合物所含的化学键类型为________________ 。
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:__________________________ 。
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:________________________________________________________________________ 。

(1)表中元素,化学性质最不活泼的是
(2)C元素在元素周期表中的位置是第三周期第
(3)最高价氧化物的水化物酸性最强的是
(4)A分别与E、G、H形成的化合物中,最稳定的是
(5)在B、C、E、F中,原子半径最大的是
(6)B、H两种元素所形成的化合物所含的化学键类型为
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】A、B、C、D、E均为短周期元素,原子序数依次增大,请根据表中信息回答下列问题:
(1)G在元素周期表中的位置________ 。
(2)B最简单气态氢化物的结构式____ ,属于____ 化合物(填“离子”或“共价”);E的最高价氧化物的水化物电子式____ ,所含化学键类型________ 。
(3)C、D、E、F、G简单离子半径由大到小顺序为:____ (填离子符号)。
(4)用电子式表示G的氢化物的形成过程______ 。
(5)A元素的某氧化物与E元素的某含氧化合物反应生成单质的化学方程式是_______ 。
(6)E、F两元素最高价氧化物对应水化物相互反应的离子方程式:____ 。
| 元素 | 元素性质或结构 |
| A | 最外层电子数是其内层电子数的2倍 |
| B | B元素的单质在空气中含量最多 |
| C | C元素在地壳中含量最多 |
| D | D是同周期中原子半径最小的元素 |
| E | E元素在同周期中金属性最强 |
| F | F元素的最外层电子数等于周期序数 |
| G | G元素原子M层上电子数比L上少2个电子。 |
(2)B最简单气态氢化物的结构式
(3)C、D、E、F、G简单离子半径由大到小顺序为:
(4)用电子式表示G的氢化物的形成过程
(5)A元素的某氧化物与E元素的某含氧化合物反应生成单质的化学方程式是
(6)E、F两元素最高价氧化物对应水化物相互反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题。
(1)②表示的元素是_______ (填元素符号);
(2)①、⑤两种元素的原子半径大小为:①___ ⑤(填“<”或“>”);
(3)③、④两种元素的金属性强弱顺序为:③___ ④(填“<”或“>”);
(4)写出③与⑥两种元素所形成化合物的化学式__________ 。
| 族 周期 | ⅠA | 0 | |||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | F | Ne | |||||
| 3 | ③ | Mg | ④ | Si | ⑤ | ⑥ | |||
(1)②表示的元素是
(2)①、⑤两种元素的原子半径大小为:①
(3)③、④两种元素的金属性强弱顺序为:③
(4)写出③与⑥两种元素所形成化合物的化学式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】A、B、C、D、E、F、G 是短周期元素,周期表中 B 与 C 相邻,C 与 E 同主族; A 中 L 层是 K 层的 2 倍,B 的电子数比 C 的电子数少 1 个;F 元素的原子在周期表中半径最小;常见化合物 D2C2 与水反应生成 C 的气体单质,且完全反应后的溶液能使酚酞溶液变红。G 是第三周期原子半径最小的主族元素。
(1)A 在元素周期表中的位置_________________ 。
(2) D2C2 的电子式为________ , 属于________________ 化合物(填“离子”或“共价”)。
(3)C 与 F 元素可形成 18 电子分子的电子式为 。
(4)A、B、C 的氢化物稳定性顺序为____________________ (用分子式表示); G 的阴离子的还原性比 E 的阴离子的还原性 ___________________________ (填“强”或“弱”)。
(5)F2C 和 F2E 中,沸点较高的是________ (填化学式),其主要原因是 _____________ 。
(6)锡(Sn)与 A 同主族,常温下能和浓硫酸反应,生成 Sn(SO4)2 和刺激性气味气体, 反应的化学方程式为__________________________________ 。
(1)A 在元素周期表中的位置
(2) D2C2 的电子式为
(3)C 与 F 元素可形成 18 电子分子的电子式为 。
(4)A、B、C 的氢化物稳定性顺序为
(5)F2C 和 F2E 中,沸点较高的是
(6)锡(Sn)与 A 同主族,常温下能和浓硫酸反应,生成 Sn(SO4)2 和刺激性气味气体, 反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】下表是五种主族元素的结构特点及其元素、单质、化合物的性质.
(1)写出X元素的原子核外电子排布__ ;其单质的化学性质__ (填“稳定”或“活泼”),该元素的非金属性__ (填“强”或“弱”),证明其强弱的理由是__ .
(2)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式__ ;已知w的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为__ .
(3)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反 应的离子方程式:__ ,__ .
(4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱.Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为__ .
A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3.
| 元素 | 结构特点及元素、单质、化合物的性质 |
| X | 气态氢化物与最高价氧化物对应水化物可以化合成盐 |
| Y | 原子中s电子数与p电子数相同,且p电子的能量最高 |
| Z | 单质在空气中燃烧产生黄色火焰,生成黄色粉末 |
| W | 最外层电子排布(n+1)sn(n+1)pn﹣1 |
| T | 单质升华可以产生紫色的烟 |
(1)写出X元素的原子核外电子排布
(2)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式
(3)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反 应的离子方程式:
(4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱.Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为
A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3.
您最近一年使用:0次



