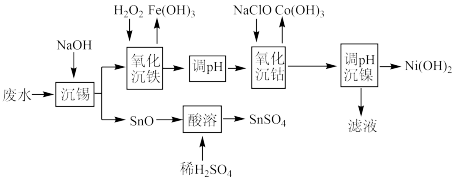
某电镀厂废水的pH为0.45,主要含有Sn2+、Ni2+和SO ,还含有少量的Fe2+和Co2+,处理该废水的一种工艺流程如图所示:
,还含有少量的Fe2+和Co2+,处理该废水的一种工艺流程如图所示:
下列叙述中错误的是
 ,还含有少量的Fe2+和Co2+,处理该废水的一种工艺流程如图所示:
,还含有少量的Fe2+和Co2+,处理该废水的一种工艺流程如图所示:
下列叙述中错误的是
| A.“氧化沉铁”时,可适当升高温度加快反应速率 |
| B.调节pH至6.5,进行“氧化沉钴”的离子方程式为ClO-+2Co2++H2O+4OH-=2Co(OH)3↓+Cl- |
| C.“滤液”中溶质主要为Na2SO4,可回收利用 |
| D.“酸溶”所得SnSO4经电解可回收得到金属Sn |
22-23高三下·山东·开学考试 查看更多[2]
更新时间:2023-02-10 13:56:24
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列方程式书写不正确 的是
| A.常温下,氯气和氢氧化钠溶液反应的离子方程式:Cl2+2OH-=ClO-+Cl-+H2O |
| B.向氯化铝溶液中滴加氨水的离子方程式:Al3++3OH-=Al(OH)3↓ |
| C.过氧化钠与水反应的化学方程式:2Na2O2+2H2O=4NaOH+O2↑ |
D.铁与水蒸气反应的化学方程式:3Fe+4H2O(g) Fe3O4+4H2 Fe3O4+4H2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列物质在水溶液中的电离方程式中,不正确的是
A.CH3COOH CH3COO-+H+ CH3COO-+H+ | B.NH3·H2O NH4 ++OH- NH4 ++OH- |
| C.Ba(OH)2=Ba2++2OH- | D.NaHSO4=Na+ +HSO4- |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列离子方程式符合题意的是
A.等物质的量浓度的盐酸与Na2CO3溶液等体积混合:2H++CO =CO2↑+H2O =CO2↑+H2O |
| B.加入Na2S除去废水中的Cu2+:S2-+Cu2+=CuS↓ |
| C.将NaClO碱性溶液与含Fe2+的溶液混合: ClO-+2Fe2++H2O=Cl-+2Fe3++2OH- |
D.用铜电极电解硫酸铜溶液:2Cu2+ + 2H2O 2Cu + O2↑ + 4H+ 2Cu + O2↑ + 4H+ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】为分析某铜合金的成分,用足量酸将其完全溶解后,用 溶液调节
溶液调节 ,当
,当 时开始出现沉淀,分别在
时开始出现沉淀,分别在 为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有
为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有

 溶液调节
溶液调节 ,当
,当 时开始出现沉淀,分别在
时开始出现沉淀,分别在 为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有
为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有
A. 、 、 | B. 、 、 | C. 、 、 | D. 、 、 、 、 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】常温下,已知CaSO4的Ksp=4.8×10-5,CaCO3的Ksp=3.6×10-9,下列说法正确的是
| A.该温度下,将5×10-2mol/L氯化钙溶液与2×10-3mol/L硫酸钠溶液等体积混合(忽略体积变化),混合后有沉淀生成 |
B.向CaSO4悬浊液中加入稀硫酸,c(SO )增大,Ksp增大 )增大,Ksp增大 |
C.向只含CaCO3的悬浊液中加入Na2SO4固体至开始有CaSO4沉淀时,溶液中c(SO ):c(CO ):c(CO )=7.5×10-5 )=7.5×10-5 |
| D.向只含CaCO3的悬浊液中加入少量的水,c(Ca2+)减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列气体去除少量杂质(括号中物质为杂质)的方法中,不能实现目的的是( )
| A.CO2(SO2),酸性KMnO4溶液 |
| B.Cl2(HCl),通过饱和的食盐水 |
| C.N2(O2),通过灼热的铜丝网 |
| D.CO2(HCl),通过饱和碳酸钠溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】人造光卤石(KCl·MgCl2·6H2O)是盐化工生产的中间产物。以光卤石为原料制得金属镁,可有下列步骤:①过滤 ②溶解 ③加入适量 Ca (OH)2 ④蒸发 ⑤用盐酸溶解 ⑥电解熔融MgCl2⑦在HCl气流中强热MgCl2·6H2O晶体正确的顺序是
| A.⑤③①②④⑥⑦ | B.②③①⑤④⑦⑥ |
| C.②④①③⑦⑤⑥ | D.⑤③①④②⑦⑥ |
您最近一年使用:0次

 2+
2+ +
+
 2
2 2O
2O

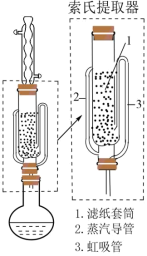
 代替乙醇进行实验
代替乙醇进行实验

