电子云轮廓图形和电子运动状态的判断。
(1)[2018·全国卷Ⅱ,35(1)节选]基态S原子电子占据最高能级的电子云轮廓图为_______ 形。
(2)[2017·全国卷Ⅰ,35(2)基态K原子中,核外电子占据的最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(3)[2021·山东,16(1)]基态F原子核外电子的运动状态,有_______ 种。
(1)[2018·全国卷Ⅱ,35(1)节选]基态S原子电子占据最高能级的电子云轮廓图为
(2)[2017·全国卷Ⅰ,35(2)基态K原子中,核外电子占据的最高能层的符号是
(3)[2021·山东,16(1)]基态F原子核外电子的运动状态,有
2023高三·全国·专题练习 查看更多[1]
(已下线)第五章 物质结构与性质 元素周期律 第26讲 原子结构核 外电子排布原理
更新时间:2023-03-09 21:42:24
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E是原子序数逐渐增大的前四周期元素,其中A元素原子核外电子有6种不同的运动状态,s轨道电子数是p轨道的两倍;C元素原子L层上有两对成对电子;D的3p轨道上得到一个电子后不容纳外来电子;E元素原子的最外层只有一个电子,其次外层的所有轨道的电子均成对。试回答:
(1)基态E原子的价层电子排布式为______ ,属于周期表的______ 区。
(2)基态B原子的轨道表示式为______ ,其核外电子占据的最高能级的电子云轮廓图为______ 形。
(3)A、B、C三种元素形成的简单氢化物的键角从大到小为______ (用氢化物分子式表示)。
(4)E与Zn相比,第二电离能与第一电离能差值更大的是______ (填“Zn”或“E”的元素符号),原因是______ 。
(1)基态E原子的价层电子排布式为
(2)基态B原子的轨道表示式为
(3)A、B、C三种元素形成的简单氢化物的键角从大到小为
(4)E与Zn相比,第二电离能与第一电离能差值更大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】新工艺采用金属氧化物 催化尿素与甲醇合成碳酸二甲酯
催化尿素与甲醇合成碳酸二甲酯 ,副产物氨气回收重新生成尿素,有关的方程式如下:
,副产物氨气回收重新生成尿素,有关的方程式如下:
反应①: +2CH3OH(g)
+2CH3OH(g)
 +2NH3(g)
+2NH3(g)
反应②:2NH3(g)+CO2(g)
 +H2O(l)
+H2O(l)
完成下列填空:
(1)C原子核外能量最高的电子有______ 个,比较 、N、O简单离子的半径大小
、N、O简单离子的半径大小__________ 。
(2)下列事实能说明氮的非金属性比碳强的是______ (选填编号)。
a.酸性: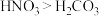 b.最高正价:氮>碳
b.最高正价:氮>碳
c.沸点: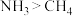 d.吸引电子能力强弱:氮>碳
d.吸引电子能力强弱:氮>碳
(3)达到平衡时,反应①碳酸二甲酯的产率 随温度T的变化关系如图所示,则反应是
随温度T的变化关系如图所示,则反应是__________ 反应(选填“放热”或“吸热”),
______  (选填“>”或“<”)。
(选填“>”或“<”)。

(4)某一恒温恒容 装置内,
装置内, 与
与 发生反应②,
发生反应②,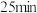 后,气体的密度减少
后,气体的密度减少 ,则
,则 内氨气的平均反应速率为
内氨气的平均反应速率为__________ 。
(5)传统合成DMC的方法是以光气( ,有剧毒)和甲醇为原料,请写出相应的化学方程式
,有剧毒)和甲醇为原料,请写出相应的化学方程式__________ 。
(6)新工艺合成DMC的方法和传统方法相比,优点有__________ (任写两点)。
 催化尿素与甲醇合成碳酸二甲酯
催化尿素与甲醇合成碳酸二甲酯 ,副产物氨气回收重新生成尿素,有关的方程式如下:
,副产物氨气回收重新生成尿素,有关的方程式如下:反应①:
 +2CH3OH(g)
+2CH3OH(g)
 +2NH3(g)
+2NH3(g)反应②:2NH3(g)+CO2(g)

 +H2O(l)
+H2O(l)完成下列填空:
(1)C原子核外能量最高的电子有
 、N、O简单离子的半径大小
、N、O简单离子的半径大小(2)下列事实能说明氮的非金属性比碳强的是
a.酸性:
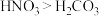 b.最高正价:氮>碳
b.最高正价:氮>碳c.沸点:
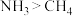 d.吸引电子能力强弱:氮>碳
d.吸引电子能力强弱:氮>碳(3)达到平衡时,反应①碳酸二甲酯的产率
 随温度T的变化关系如图所示,则反应是
随温度T的变化关系如图所示,则反应是
 (选填“>”或“<”)。
(选填“>”或“<”)。
(4)某一恒温恒容
 装置内,
装置内, 与
与 发生反应②,
发生反应②,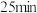 后,气体的密度减少
后,气体的密度减少 ,则
,则 内氨气的平均反应速率为
内氨气的平均反应速率为(5)传统合成DMC的方法是以光气(
 ,有剧毒)和甲醇为原料,请写出相应的化学方程式
,有剧毒)和甲醇为原料,请写出相应的化学方程式(6)新工艺合成DMC的方法和传统方法相比,优点有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)铁在元素周期表中的位置为_____ ,基态铁原子有个未成对电子_____ ,三价铁离子的电子排布式为_____ 。
(2)基态Si原子中,电子占据的最高能层符号_____ ,该能层具有的原子轨道数为_____ ;铝元素的原子核外共有_____ 种不同运动状态的电子、_____ 种不同能级的电子。
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_____ 形象化描述。在基态14C原子中,核外存在_____ 对自旋相反的电子。
(2)基态Si原子中,电子占据的最高能层符号
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表列出了①~④四种元素在周期表中的位置.
回答下列问题:
(1)①的元素符号为_____________ 。
(2)②的基态原子电子排布式为__________________________ 。
(3)③和④中原子半径较大的是_____________ (填元素符号)。
(4)如图是③原子中s电子和p电子的电子云轮廓图。s电子的电子云形状为_____________ 形;每个p能级都有_____________ 个相互垂直的电子云。

| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | |||||||
| 3 | ② | ③ | ||||||
| 4 | ④ |
回答下列问题:
(1)①的元素符号为
(2)②的基态原子电子排布式为
(3)③和④中原子半径较大的是
(4)如图是③原子中s电子和p电子的电子云轮廓图。s电子的电子云形状为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图是s能级和p能级的原子轨道示意图,试回答下列问题:
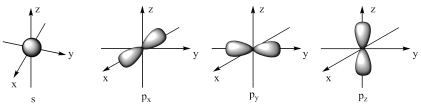
(1)若元素X的原子最外层电子排布式为 ,原子中能量最高的是
,原子中能量最高的是 ____________ 电子,其电子云在空间内有 ____________ 个互相垂直的伸展方向;元素X的名称是 ____________ ,它的简单氢化物的电子式是 ____________ 。
(2)若元素X的原子最外层电子排布式为 ,那么X的元素符号为
,那么X的元素符号为 ____________ ,原子的轨道表示式为 ____________ 。

(1)若元素X的原子最外层电子排布式为
 ,原子中能量最高的是
,原子中能量最高的是 (2)若元素X的原子最外层电子排布式为
 ,那么X的元素符号为
,那么X的元素符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请根据所学知识点,完成以下填空。
(1)基态P原子的价电子轨道表示式_______ 。
(2)基态K原子的简化电子排布式为_______ ,其能量最高的电子所在的能级是_______ ,该能级的原子轨道呈_______ 形。
(3)基态Ni原子核外电子的运动状态有_______ 种,基态 中未成对的电子数与成对电子数之比为
中未成对的电子数与成对电子数之比为_______ 。
(4) 的VSEPR模型和空间构型分别为
的VSEPR模型和空间构型分别为_______ 、_______ 。
(5)一氯乙烷( )和四氟乙烯(
)和四氟乙烯( )分子中C的杂化轨道类型分别为
)分子中C的杂化轨道类型分别为_______ 和_______ 。
(6) 分子中各原子都满足最外层8电子结构,分子中σ键与π键数目之比为
分子中各原子都满足最外层8电子结构,分子中σ键与π键数目之比为_______ , 分子为
分子为_______ (填“极性分子”或“非极性分子”)。
(1)基态P原子的价电子轨道表示式
(2)基态K原子的简化电子排布式为
(3)基态Ni原子核外电子的运动状态有
 中未成对的电子数与成对电子数之比为
中未成对的电子数与成对电子数之比为(4)
 的VSEPR模型和空间构型分别为
的VSEPR模型和空间构型分别为(5)一氯乙烷(
 )和四氟乙烯(
)和四氟乙烯( )分子中C的杂化轨道类型分别为
)分子中C的杂化轨道类型分别为(6)
 分子中各原子都满足最外层8电子结构,分子中σ键与π键数目之比为
分子中各原子都满足最外层8电子结构,分子中σ键与π键数目之比为 分子为
分子为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)基态氟原子核外有9个电子,这些电子的电子云形状有_______ 种;氟原子有_______ 种不同能量的电子,价电子排布图为_______ 。
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:_______ ;Cl-中有_______ 种运动状态不同的电子。
(3)基态硼原子的核外电子排布图为_______ 。
(1)基态氟原子核外有9个电子,这些电子的电子云形状有
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:
(3)基态硼原子的核外电子排布图为
您最近一年使用:0次
【推荐3】如图是元素周期表中的前四周期,回答下列问题:

(1)a元素的基态原子的电子排布图是图①、②中的一个。
① ②
② 
另一个电子排布图错误的原因是:它不符合___________ (填标号)。
A.构造原理 B.泡利原理 C.洪特规则
a的简单氢化物的VSEPR模型为___________
(2)b元素的正二价离子的核外价电子轨道表示式是___________
(3)b、e两种元素的第四电离能大小关系为 ___________>
___________> ___________,
___________,___________ (填元素符号),原因是___________
(4)已知元素c、f的最简单的化合物中共用电子对偏向f,元素c、g的最简单的化合物中共用电子对偏向c,则元素c、f、g的电负性由大到小的顺序为___________ (填元素符号)
(5)某元素的原子价电子排布式为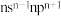 ,该基态原子核外自旋方向相同的电子最多有
,该基态原子核外自旋方向相同的电子最多有___________ 个。
(6)下列现象与原子核外电子跃迁有关的是___________ (填标号)
a.激光 b.LED灯光 c.金属导电 d.核辐射

(1)a元素的基态原子的电子排布图是图①、②中的一个。
①
 ②
② 
另一个电子排布图错误的原因是:它不符合
A.构造原理 B.泡利原理 C.洪特规则
a的简单氢化物的VSEPR模型为
(2)b元素的正二价离子的核外价电子轨道表示式是
(3)b、e两种元素的第四电离能大小关系为
 ___________>
___________> ___________,
___________,(4)已知元素c、f的最简单的化合物中共用电子对偏向f,元素c、g的最简单的化合物中共用电子对偏向c,则元素c、f、g的电负性由大到小的顺序为
(5)某元素的原子价电子排布式为
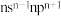 ,该基态原子核外自旋方向相同的电子最多有
,该基态原子核外自旋方向相同的电子最多有(6)下列现象与原子核外电子跃迁有关的是
a.激光 b.LED灯光 c.金属导电 d.核辐射
您最近一年使用:0次

 )氧化法常用于测定钢中锰的含量,H2S2O8的结构式如图所示,S的轨道杂化方式为
)氧化法常用于测定钢中锰的含量,H2S2O8的结构式如图所示,S的轨道杂化方式为


