物质的类别和核心元素的化合价是研究物质性质的两个重要维度。如图是硫及其部分化合物的“价一类”二维图。
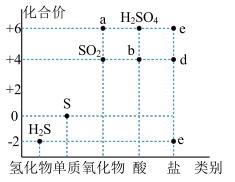
(1)据图中信息,物质a和b的化学式:a_____ ;b_____ 。
(2)Na2S2O5和Na2S2O3在化工生产中应用广泛,若将Na2S2O5归入图中,应置于图中的_____ (填“c”、“d”或“e”)点。已知:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,氢化物单质氧化物酸盐类别此反应中的物质没有涉及的类别是_____ (填序号)。
A.单质 B.酸性氧化物 C.酸 D.碱 E.盐
(3)将SO2通入以下溶液,均会发生颜色变化,其中体现SO2还原性的是_____ (填序号)。
(4)硫元素的部分转化如图所示。过程①可利用克劳斯法实现,该法先将部分H2S通过燃烧转化为SO2,再将SO2与剩余的H2S混合。为实现硫的最大回收,燃烧的H2S和剩余的H2S物质的量之比应为_____ 。过程②宜在土壤的_____ 区实现(填“富氧”或“缺氧”)。


(1)据图中信息,物质a和b的化学式:a
(2)Na2S2O5和Na2S2O3在化工生产中应用广泛,若将Na2S2O5归入图中,应置于图中的
A.单质 B.酸性氧化物 C.酸 D.碱 E.盐
(3)将SO2通入以下溶液,均会发生颜色变化,其中体现SO2还原性的是
| A.使溴水褪色 |
| B.使品红溶液褪色有机硫 |
| C.使滴有酚酞的氢氧化钠溶液褪色 |
| D.使氢硫酸溶液中出现淡黄色浑浊 |

更新时间:2023-02-15 14:12:33
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某小组同学设计实验实现几种价态硫元素的转化。
任务I:从以下试剂中选择合适的试剂实现S(+6)→S(+4)的转化。
试剂清单:①浓H2SO4②稀H2SO4③酸性KMnO4溶液④Na2SO3溶液⑤Cu⑥品红溶液
(1)写出实现转化的化学方程式:___________ 。
(2)设计实验,证明实现了该转化(写出操作和现象):___________ 。
任务II:实现硫元素在0、+2、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
 产生淡黄色沉淀和刺激性气体
产生淡黄色沉淀和刺激性气体
(3)过程i中加入的物质是___________ (填化学式),该转化利用的是SO2的___________ 性质。
(4)过程ii中试剂X为___________ (填“氧化剂”或“还原剂”)
(5)写出过程iii反应的离子 方程式:___________ 。
任务I:从以下试剂中选择合适的试剂实现S(+6)→S(+4)的转化。
试剂清单:①浓H2SO4②稀H2SO4③酸性KMnO4溶液④Na2SO3溶液⑤Cu⑥品红溶液
(1)写出实现转化的化学方程式:
(2)设计实验,证明实现了该转化(写出操作和现象):
任务II:实现硫元素在0、+2、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
 产生淡黄色沉淀和刺激性气体
产生淡黄色沉淀和刺激性气体(3)过程i中加入的物质是
(4)过程ii中试剂X为
(5)写出过程iii反应的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】盐酸、硫酸、硝酸是工业生产中常用的三种强酸。回答下列问题:
(1)盐酸既有酸性,又能表现氧化性和还原性。若用浓盐酸制取氯气,需要与具有___________ (酸性、氧化性、还原性)的物质发生反应;若用0.6mol  与100 mL
与100 mL 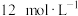 的浓盐酸加热反应,生成Cl2的物质的量
的浓盐酸加热反应,生成Cl2的物质的量___________ (填标号)。
A.等于0.6 mol B.大于0.3 mol C.等于0.3 mol D.小于0.3 mol
(2)以下为用硫酸制取硫酸铜的两种方法。①实验室常利用铜与浓硫酸加热反应制得硫酸铜;②工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制备硫酸铜。方法②反应的离子方程式为___________ 。上述两种方法中,制取硫酸铜的最佳方法是___________ (填“①”或“②”)。
(3)将3.84 g铜与一定量的浓硝酸反应,当铜消耗完毕时产生NO和NO2气体的体积为2.24 L(标况),则参加反应的硝酸的物质的量为___________ mol。生成的NO在标况下的体积是___________ L,氧化剂与还原剂的物质的量之比是___________ 。
(4)Q为单质,X、Y、Z、E、M五种物质含有同一元素,一定条件下有以下的转化关系。
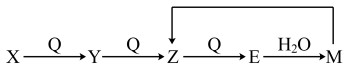
若M为酸。则M的化学式可能为___________ 。
(1)盐酸既有酸性,又能表现氧化性和还原性。若用浓盐酸制取氯气,需要与具有
 与100 mL
与100 mL 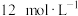 的浓盐酸加热反应,生成Cl2的物质的量
的浓盐酸加热反应,生成Cl2的物质的量A.等于0.6 mol B.大于0.3 mol C.等于0.3 mol D.小于0.3 mol
(2)以下为用硫酸制取硫酸铜的两种方法。①实验室常利用铜与浓硫酸加热反应制得硫酸铜;②工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制备硫酸铜。方法②反应的离子方程式为
(3)将3.84 g铜与一定量的浓硝酸反应,当铜消耗完毕时产生NO和NO2气体的体积为2.24 L(标况),则参加反应的硝酸的物质的量为
(4)Q为单质,X、Y、Z、E、M五种物质含有同一元素,一定条件下有以下的转化关系。

若M为酸。则M的化学式可能为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:

注:氢化物指的是由氢元素和另一种元素组成的化合物, CH4就是碳元素的一种氢化物。
(1)X的化学式为_______ 。
(2)已知SO3是一种酸性氧化物,请写出SO3与NaOH溶液反应的离子方程式为_______ 。
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是_______ (填序号)。
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4 d.SO2 + Na2SO4
(4)将X与Y混合,可生成硫单质。该反应的氧化剂与还原剂的个数之比为_______ 。

注:氢化物指的是由氢元素和另一种元素组成的化合物, CH4就是碳元素的一种氢化物。
(1)X的化学式为
(2)已知SO3是一种酸性氧化物,请写出SO3与NaOH溶液反应的离子方程式为
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4 d.SO2 + Na2SO4
(4)将X与Y混合,可生成硫单质。该反应的氧化剂与还原剂的个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求完成下列内容
(1)请写出下列反应的化学方程式。
①Na2SO3和较浓H2SO4制取SO2气体:_______
②足量氨水中通入SO2气体:_______
③Cu与浓H2SO4加热条件下反应:_______
(2)一定条件下, 和氟气可发生如下反应:
和氟气可发生如下反应: ,从而可知在
,从而可知在 中,元素R的化合价是
中,元素R的化合价是_______ 。
(3)实验室用氯酸钾和浓盐酸制取氯气,配平下列方程式_______ _______KClO3+_______HCl=_______Cl2↑+_______KCl+_______H2O
(4)①配平该反应的化学方程式:_______ ______FeSO4+_______KNO3+_______H2SO4=_______K2SO4+_______Fe2(SO4)3+_______NO↑+_______H2O。
②该反应中氧化产物是_______ (填化学式);当15.2 g FeSO4恰好完全反应时,转移电子的物质的量为_______ 。
(1)请写出下列反应的化学方程式。
①Na2SO3和较浓H2SO4制取SO2气体:
②足量氨水中通入SO2气体:
③Cu与浓H2SO4加热条件下反应:
(2)一定条件下,
 和氟气可发生如下反应:
和氟气可发生如下反应: ,从而可知在
,从而可知在 中,元素R的化合价是
中,元素R的化合价是(3)实验室用氯酸钾和浓盐酸制取氯气,配平下列方程式
(4)①配平该反应的化学方程式:
②该反应中氧化产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,在循环过程中价态变化在-2价至+6价之间,以不同的状态(或形态)发生一系列的变化,请分析此图并回答有关问题。
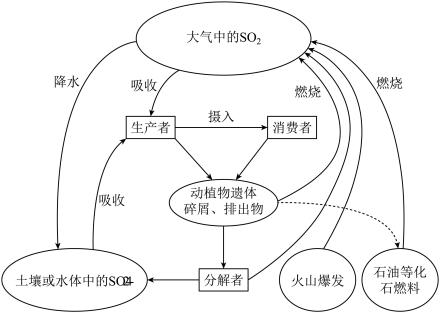
(1)分解者可将含硫有机物分解为硫化氢,硫黄细菌和硫化细菌可将硫化氢进一步转变为元素硫或硫酸盐,下列关于硫化氢说法正确的是_______
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢是一种无色臭鸡蛋气味的有毒气体
(2)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在较小,其原因可能是_______ 。(用化学方程式表示)
(3)研究发现,空气其中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2→SO3+NO
②SO3+H2O→H2SO4
③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不同的是_______ 。
A.潮湿的氯气通过盛有浓H2SO4的洗气瓶
B.硫化氢通入浓H2SO4中
C.向盐酸中加入浓硫酸产生白雾
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是_______ 。
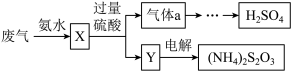
(5)若采用如图所示的流程处理则气体a是_______ ,Y一定含有_______ 。(填化学式)

(1)分解者可将含硫有机物分解为硫化氢,硫黄细菌和硫化细菌可将硫化氢进一步转变为元素硫或硫酸盐,下列关于硫化氢说法正确的是
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢是一种无色臭鸡蛋气味的有毒气体
(2)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在较小,其原因可能是
(3)研究发现,空气其中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2→SO3+NO
②SO3+H2O→H2SO4
③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不同的是
A.潮湿的氯气通过盛有浓H2SO4的洗气瓶
B.硫化氢通入浓H2SO4中
C.向盐酸中加入浓硫酸产生白雾
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是
(5)若采用如图所示的流程处理则气体a是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)红热木炭与浓H2SO4反应的化学方程式是C+2H2SO4 CO2↑+2SO2↑+2H2O,该反应中浓硫酸的作用是作
CO2↑+2SO2↑+2H2O,该反应中浓硫酸的作用是作___________ (填“氧化剂”或“还原剂”)。
(2)SO2能够使品红溶液褪色,体现了二氧化硫具有___________ 性。
(3)为了探究HClO的漂白性,某同学设计了如下的实验。
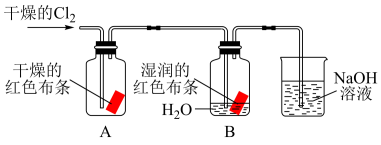
通入Cl2后,集气瓶A中的现象是___________ ,集气瓶B中湿润的红色布条的现象可得出的结论是___________ ,最后的NaOH装置中发生的主要化学方程式是___________ 。
(1)红热木炭与浓H2SO4反应的化学方程式是C+2H2SO4
 CO2↑+2SO2↑+2H2O,该反应中浓硫酸的作用是作
CO2↑+2SO2↑+2H2O,该反应中浓硫酸的作用是作(2)SO2能够使品红溶液褪色,体现了二氧化硫具有
(3)为了探究HClO的漂白性,某同学设计了如下的实验。

通入Cl2后,集气瓶A中的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】为消除燃煤烟气中的SO2、NOx,研究者提出了烟气“脱硫”、“脱硝”的方法。
(1)将烟气与空气按一定比例通入含Fe2+的溶液中,可实现“脱硫”,其过程表示如下:
i:2Fe2++O2+SO2=2Fe3++
ii:2H2O+2Fe3++SO2=2Fe2++ +4H+
+4H+
“脱硫”过程的总反应方程式为_______ 。
(2)在催化剂作用下,用NH3将烟气中NO还原,进行无害化处理,可实现“脱硝”,反应方程式为_______ 。
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”,将烟气中的SO2、NO转化为 、
、 。当烟气中SO2和NO的体积比为4:1时,得到的吸收液中烟气转化生成的
。当烟气中SO2和NO的体积比为4:1时,得到的吸收液中烟气转化生成的 和Cl-的物质的量之比为
和Cl-的物质的量之比为_______ 。
(1)将烟气与空气按一定比例通入含Fe2+的溶液中,可实现“脱硫”,其过程表示如下:
i:2Fe2++O2+SO2=2Fe3++

ii:2H2O+2Fe3++SO2=2Fe2++
 +4H+
+4H+“脱硫”过程的总反应方程式为
(2)在催化剂作用下,用NH3将烟气中NO还原,进行无害化处理,可实现“脱硝”,反应方程式为
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”,将烟气中的SO2、NO转化为
 、
、 。当烟气中SO2和NO的体积比为4:1时,得到的吸收液中烟气转化生成的
。当烟气中SO2和NO的体积比为4:1时,得到的吸收液中烟气转化生成的 和Cl-的物质的量之比为
和Cl-的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】分别向盛有①紫色石蕊溶液、②NaOH溶液、③品红溶液、④酸性高锰酸钾溶液的试管中通入 气体。
气体。
(1)试管①中的现象:___________ ,发生反应的化学方程式是___________ 。
(2)试管②中发生反应的化学方程式是___________ ,如果通入过量的 ,则发生反应的化学方程式为
,则发生反应的化学方程式为___________ 。
(3)试管③中的现象:___________ ,如将吸收 后的该溶液加热,现象:
后的该溶液加热,现象:___________ 。
(4)试管④中的现象:___________ 。
(5)上述实验中, 表现出酸性氧化物性质的是
表现出酸性氧化物性质的是___________ (填试管标号,下同), 表现出漂白性的是
表现出漂白性的是___________ 。
 气体。
气体。(1)试管①中的现象:
(2)试管②中发生反应的化学方程式是
 ,则发生反应的化学方程式为
,则发生反应的化学方程式为(3)试管③中的现象:
 后的该溶液加热,现象:
后的该溶液加热,现象:(4)试管④中的现象:
(5)上述实验中,
 表现出酸性氧化物性质的是
表现出酸性氧化物性质的是 表现出漂白性的是
表现出漂白性的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮、硫的氧化物可以带来酸雨、空气污染等危害。
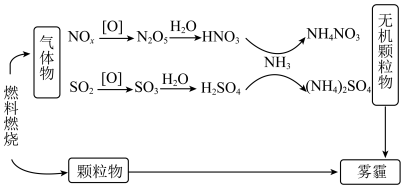
Ⅰ.科学家发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:
(1)实验室利用两种固体加热的方式制备氨气,反应的化学方程式为________________ 。
(2)下列关于雾霾的叙述不正确的是___________ (填标号)。
A.雾霾中含有硝酸铵和硫酸铵
B. 是形成无机颗粒物的催化剂
是形成无机颗粒物的催化剂
C.雾霾的形成与过度施用氮肥有关
(3) 是典型的铵盐,请写出检验其稀溶液中
是典型的铵盐,请写出检验其稀溶液中 的方法:
的方法:________________________ 。
(4)实验室模拟用浓硫酸脱除氮氧化物,装置如图所示,实验开始后装置C中发生反应: 。
。_____________ ,装置B的作用是________________ 。
②理论上应控制相同时间内a、b处通入气体的物质的量之比为___________ 。
(5)可用双碱法(氢氧化钙为悬浊液)脱硫处理工业废气中的 ,原理如图所示,其中可循环使用的物质是
,原理如图所示,其中可循环使用的物质是_______________ ,双碱法脱硫的总反应方程式为________________ 。
Ⅰ.科学家发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:
(1)实验室利用两种固体加热的方式制备氨气,反应的化学方程式为
(2)下列关于雾霾的叙述不正确的是
A.雾霾中含有硝酸铵和硫酸铵
B.
 是形成无机颗粒物的催化剂
是形成无机颗粒物的催化剂C.雾霾的形成与过度施用氮肥有关
(3)
 是典型的铵盐,请写出检验其稀溶液中
是典型的铵盐,请写出检验其稀溶液中 的方法:
的方法:(4)实验室模拟用浓硫酸脱除氮氧化物,装置如图所示,实验开始后装置C中发生反应:
 。
。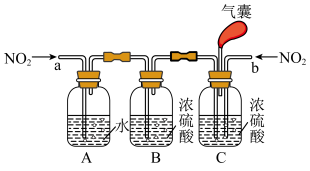
②理论上应控制相同时间内a、b处通入气体的物质的量之比为
(5)可用双碱法(氢氧化钙为悬浊液)脱硫处理工业废气中的
 ,原理如图所示,其中可循环使用的物质是
,原理如图所示,其中可循环使用的物质是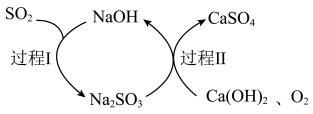
您最近一年使用:0次



