电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的 在5.0~6.0之间,通过电解生成
在5.0~6.0之间,通过电解生成 沉淀。
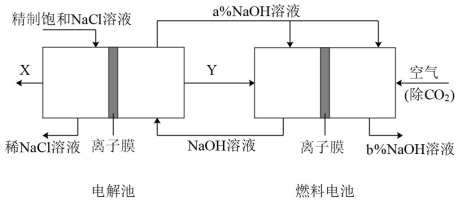
沉淀。 有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
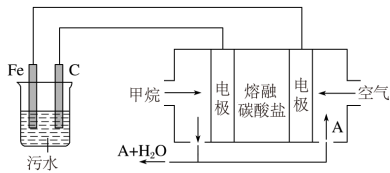
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的___________ (填字母)。
a. b.
b. c.
c. d.
d.
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应分别是___________ ;___________ 。
(3)该熔融盐燃料电池是以熔融碳酸盐为电解质,以 为燃料,空气为氧化剂,稀土金属材料为电极。
为燃料,空气为氧化剂,稀土金属材料为电极。
①正极的电极反应为___________ 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环,A物质的化学式是___________ 。
(4)实验过程中,若在阴极产生了67.2L(标准状况)气体,则熔融盐燃料电池消耗 (标准状况)
(标准状况)___________ L。
 在5.0~6.0之间,通过电解生成
在5.0~6.0之间,通过电解生成 沉淀。
沉淀。 有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的
a.
 b.
b. c.
c. d.
d.
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应分别是
(3)该熔融盐燃料电池是以熔融碳酸盐为电解质,以
 为燃料,空气为氧化剂,稀土金属材料为电极。
为燃料,空气为氧化剂,稀土金属材料为电极。①正极的电极反应为
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环,A物质的化学式是
(4)实验过程中,若在阴极产生了67.2L(标准状况)气体,则熔融盐燃料电池消耗
 (标准状况)
(标准状况)
更新时间:2023-03-12 10:45:38
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】能源是影响全球经济和生活的重要因素。目前人类已开发和利用的能源中,电能是和人类生产生活联系最为密切的能源,原电池是可以将化学能转化为电能的装置。
(1)下列装置能构成原电池的是___________(填标号);
(2)电池负极的现象是___________ ;
(3)请写出该电池正极反应方程式___________ ;
(4)该反应的电子流向为:___________ 电极流向___________ 电极(请填写电极名称);
(5)将正极材料替换成下列物质,该电极发生的电极反应不变的是___________ (填标号)。
A.Fe B.Al C.石墨
(1)下列装置能构成原电池的是___________(填标号);
A. | B. | C. | D. |
(3)请写出该电池正极反应方程式
(4)该反应的电子流向为:
(5)将正极材料替换成下列物质,该电极发生的电极反应不变的是
A.Fe B.Al C.石墨
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)已知1mol葡萄糖完全燃烧放热2800kJ。写出葡萄糖燃烧的化学反应方程式:_______ 。现有72g葡萄糖(C6H12O6)与足量的氧气充分反应,共放热_______ kJ。
(2)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示(电解质溶液为酸性),试写出该电池的两极反应式:_______ 质子在交换膜上向_______ (填正或负)极区迁移。72g葡萄糖在该电池中可转移电子_______ mol。

(2)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示(电解质溶液为酸性),试写出该电池的两极反应式:

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】某化学兴趣小组探究不同条件下化学能转化为电能的装置如图所示。

(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为___________ 。
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为___________ ,负极的电极反应式为___________ ,当反应中收集到标准状况下448mL气体时,电极消耗的质量为___________ g。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的能量直接转化为电能。现设计一种燃料电池,以电极a为正极,电极b为负极,乙醇(C2H5OH)为燃料,氢氧化钠溶液为电解质溶液,则乙醇应通入___________ (填“a”或“b”,下同)极,溶液中OH-向___________ 极移动。

(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的能量直接转化为电能。现设计一种燃料电池,以电极a为正极,电极b为负极,乙醇(C2H5OH)为燃料,氢氧化钠溶液为电解质溶液,则乙醇应通入
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。

请回答下列问题:
(1)甲池为_________ (填“原电池”、“电解池”或“电镀池”),A电极为_________ (填“正极”、“负极”、“阴极”或“阳极”),其电极反应式为__________ 。
(2)乙池中C极为_________ (填“正极”、“负极”、“阴极”或“阳极”),其电极反应式为__________ 。当池中D极质量增重21.6g时,甲池中B电极理论上消耗O2的体积为_________ L(标准状况)。
(3)丙池中F电极为_______ (填“正极”“负极”、“阴极”或“阳极”),该池的总反应的化学方程式为__________ 。
(4)已知丙池中的溶液为400 mL,合上开关K,一段时间后,丙池中,F极增重1.28 g,若不考虑溶液体积变化,则此时溶液的pH为_______ 。

请回答下列问题:
(1)甲池为
(2)乙池中C极为
(3)丙池中F电极为
(4)已知丙池中的溶液为400 mL,合上开关K,一段时间后,丙池中,F极增重1.28 g,若不考虑溶液体积变化,则此时溶液的pH为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】乙醇是一种比较理想的可用于燃料电池的有机物。乙醇来源丰富,可以通过含糖有机物的发酵进行大规模的生产。下图是以乙醇燃料电池为电源,电解含NO的废气制备HNO3示意图(c、d均为石墨电极)。
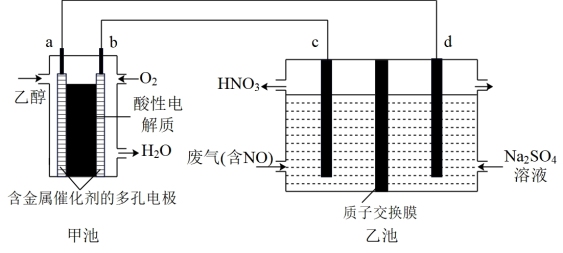
(1)请写出甲池中a极上的电极反应式:___________ 。
(2)导线中电子转移的方向为___________→___________、___________ →___________ (用a、b、c、d表示)。___________
(3)请写出乙池中c极上的电极反应式:___________ 。
(4)假设电解前,乙池两侧溶液体积均为100ml,左侧溶液中c (HNO3)为0.1 mol/L。电解结束后,左侧溶液中c (HNO3)变为0.3 mol/L,则处理NO的体积为___________ (标准状况);若忽略溶液体积变化,乙池右侧溶液的pH与电解前相比___________ (填“增大”、“减小”或“不变”)。

(1)请写出甲池中a极上的电极反应式:
(2)导线中电子转移的方向为___________→___________、___________ →___________ (用a、b、c、d表示)。
(3)请写出乙池中c极上的电极反应式:
(4)假设电解前,乙池两侧溶液体积均为100ml,左侧溶液中c (HNO3)为0.1 mol/L。电解结束后,左侧溶液中c (HNO3)变为0.3 mol/L,则处理NO的体积为
您最近一年使用:0次
【推荐1】如图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题。

(1)打开K2,合并K1,B为_______ 极,A的电极反应式为:_______ ,
(2)打开K1,合并K2,E为_______ 极,F极的电极反应式为:_______ ;检验F极产生气体的方法是_______ 。

(1)打开K2,合并K1,B为
(2)打开K1,合并K2,E为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】电解原理常用于某些物质的制备。回答下列问题:
(1) 可以通过石墨为电板,
可以通过石墨为电板, 和
和 的混合溶液为电解液电解制取。阳极发生的电极反应式为
的混合溶液为电解液电解制取。阳极发生的电极反应式为_______ ,阴极上观察到的现象是_______ ;若电解液中不加入 ,阴极发生的电极反应式为
,阴极发生的电极反应式为_______ 。
(2) 可采用“电解法”制备,装置如图所示。
可采用“电解法”制备,装置如图所示。

①写出电解时阴极的电极反应式_______ 。
②电解过程中通过阳离子交换膜的离子主要为_______ ,其迁移方向是_______ 。
(1)
 可以通过石墨为电板,
可以通过石墨为电板, 和
和 的混合溶液为电解液电解制取。阳极发生的电极反应式为
的混合溶液为电解液电解制取。阳极发生的电极反应式为 ,阴极发生的电极反应式为
,阴极发生的电极反应式为(2)
 可采用“电解法”制备,装置如图所示。
可采用“电解法”制备,装置如图所示。
①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)依据反应: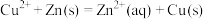 设计的原电池如图所示。
设计的原电池如图所示。
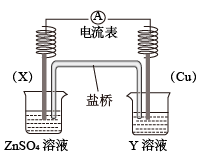
①电极X的材料是________ ;Y溶液可以是________ 溶液。
②电池放电过程中,盛有饱和 琼脂溶胶的盐桥中,向
琼脂溶胶的盐桥中,向 溶液扩散的离子是
溶液扩散的离子是________ (填离子符号)。
(2)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防护。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:_________ 。
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图所示的方案:
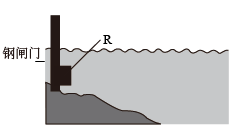
其中连接在铁闸门上的固体材料R可以采用________ (填写字母序号)。
a.铜 b.钠 c.锌 d.石墨
(3)电解原理在工业上有着广泛的用途,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
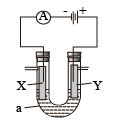
①若X、Y都是惰性电极,a是饱和 溶液,则电解的总反应式为
溶液,则电解的总反应式为________________ 。
②当电路中流通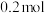 电子时,整个装置共放出气体
电子时,整个装置共放出气体________ L(标准状况下)。
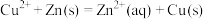 设计的原电池如图所示。
设计的原电池如图所示。
①电极X的材料是
②电池放电过程中,盛有饱和
 琼脂溶胶的盐桥中,向
琼脂溶胶的盐桥中,向 溶液扩散的离子是
溶液扩散的离子是(2)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防护。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图所示的方案:

其中连接在铁闸门上的固体材料R可以采用
a.铜 b.钠 c.锌 d.石墨
(3)电解原理在工业上有着广泛的用途,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。

①若X、Y都是惰性电极,a是饱和
 溶液,则电解的总反应式为
溶液,则电解的总反应式为②当电路中流通
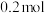 电子时,整个装置共放出气体
电子时,整个装置共放出气体
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】甲烷是非常重要的能源和化工原料,请回答下列问题.
(1)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为H2SO4溶液),通过装置Ⅱ实现铁棒镀铜。
①a处应通入______ (填“CH4”或“O2”),b处电极上发生的电极反应式是___________ ;
②电镀结束后,装置Ⅰ中溶液的pH______ (填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度_______ ;
③若实验过程中Ⅱ中的铜片质量减少了2.56g,则Ⅰ中理论上消耗CH4的体积(标准状况)______ L。
(2)若将装置Ⅱ中的两电极均改为石墨惰性电极 :
①写出装置Ⅱ中发生的总化学反应方式________________________________ 。
②若用Ⅱ电解200 mL 0.05 mol·L-1的CuSO4溶液,一段时间后溶液中的Cu2+恰好完全析出,恢复至室温,溶液pH=__________ (忽略电解过程中溶液体积变化);若想将上述电解后的溶液恢复为与电解前的溶液相同,可以加入一定质量的__________ (填序号);
a.Cu b.CuO c.Cu(OH)2 d.CuSO4
(1)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为H2SO4溶液),通过装置Ⅱ实现铁棒镀铜。

①a处应通入
②电镀结束后,装置Ⅰ中溶液的pH
③若实验过程中Ⅱ中的铜片质量减少了2.56g,则Ⅰ中理论上消耗CH4的体积(标准状况)
(2)若将装置Ⅱ中的两电极均改为石墨
①写出装置Ⅱ中发生的总化学反应方式
②若用Ⅱ电解200 mL 0.05 mol·L-1的CuSO4溶液,一段时间后溶液中的Cu2+恰好完全析出,恢复至室温,溶液pH=
a.Cu b.CuO c.Cu(OH)2 d.CuSO4
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】如图,C、D、E、F、X、Y都是惰性电极,A、B为电源。接通电源一段时间后,X极液体颜色变深。

(1)若用甲醇碱性燃料电池作电源,则A为___________ 极,总反应式为___________ 。
(2)若甲中装有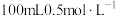 硫酸铜溶液,工作一段时间后,当硫酸铜恰好完全被消耗时,停止通电,此时测得溶液pH=
硫酸铜溶液,工作一段时间后,当硫酸铜恰好完全被消耗时,停止通电,此时测得溶液pH=___________ (假设溶液体积不变)。
(3)通电后,检验乙中F极产物的方法是___________ 。
(4)欲用丙装置给铁件镀铜,反应一段时间后(用甲醇碱性燃料电池作电源)铁制品质量增加9.6g,理论上消耗甲醇的质量为___________ g。

(1)若用甲醇碱性燃料电池作电源,则A为
(2)若甲中装有
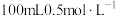 硫酸铜溶液,工作一段时间后,当硫酸铜恰好完全被消耗时,停止通电,此时测得溶液pH=
硫酸铜溶液,工作一段时间后,当硫酸铜恰好完全被消耗时,停止通电,此时测得溶液pH=(3)通电后,检验乙中F极产物的方法是
(4)欲用丙装置给铁件镀铜,反应一段时间后(用甲醇碱性燃料电池作电源)铁制品质量增加9.6g,理论上消耗甲醇的质量为
您最近一年使用:0次