钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。请回答下列问题:
(1)钢铁的电化学腐蚀原理:在酸性环境中发生析氢腐蚀,在中性或碱性环境中发生吸氧腐蚀。

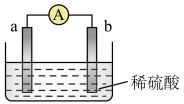
①分别写出图1中铁电极和石墨电极的电极反应式:_______ ,_______ 。
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图1虚线框内所示位置做出修改,并用箭头标出导线中电子流动方向_____ 。
③写出修改后石墨电极的电极反应式:_______ 。
(2)工业上常用盐酸除去铁锈。现将一生锈的铁片放入盐酸中,溶液中可能发生反应的化学方程式有__________ 。
(3)在实际生产中,可在铁制品的表面镀铜防止铁被腐蚀。装置如图2所示:
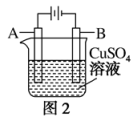
①A电极对应的金属是_______ (填元素名称),B电极的电极反应式为_______ 。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为_______ mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因:_______ 。
(1)钢铁的电化学腐蚀原理:在酸性环境中发生析氢腐蚀,在中性或碱性环境中发生吸氧腐蚀。

①分别写出图1中铁电极和石墨电极的电极反应式:
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图1虚线框内所示位置做出修改,并用箭头标出导线中电子流动方向
③写出修改后石墨电极的电极反应式:
(2)工业上常用盐酸除去铁锈。现将一生锈的铁片放入盐酸中,溶液中可能发生反应的化学方程式有
(3)在实际生产中,可在铁制品的表面镀铜防止铁被腐蚀。装置如图2所示:

①A电极对应的金属是
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因:
2023高三·全国·专题练习 查看更多[1]
(已下线)专题六 金属的化学腐蚀与防护(练习)
更新时间:2023-03-18 22:00:59
|
相似题推荐
【推荐1】(1)紫薯营养丰富,具有特殊的保健功能。下表是100 g紫薯粉的营养成分含量表:
①以上营养成分中,______ 是人体中含有的微量元素。
②紫薯粉中的脂肪在人体内会水解成高级脂肪酸和______ 。
③蛋白质在人体内水解的最终产物是氨基酸,其结构可表示为R—CH(NH2)—X,则“—X”的名称为___ 。
④在酶的作用下,淀粉水解为葡萄糖,葡萄糖再转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式______ 。
(2)合理饮食、正确使用药物对人体健康至关重要。
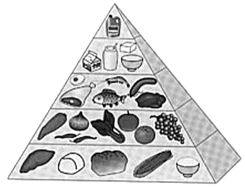
①“中国居民平衡膳食宝塔”如图所示,位于最上层且每天不超过25g的能量物质是______ 。
②某品牌饼干的配料标签如图所示,其中苯甲酸钠的作用是______ 。
③三硅酸镁(Mg2Si3O8·nH2O)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2·H2O等物质的化学方程式______ 。
(3)材料的生产与使用是人类文明和生活进步的一个重要标志。
①我国C919大型客机的机身蒙皮使用的是第三代铝锂合金材料,选用铝锂合金的优点是______ (任答一点)。
②铁路建设中如何防止铁轨的腐蚀是工程技术人员攻克的难题之一。钢铁在潮湿的空气中易发生吸氧腐蚀如图所示,则正极的电极反应式为______ 。

③玻璃中加入适量的溴化银(AgBr)和氧化铜的微小晶粒,经过适当的热处理,可以制成变色玻璃,请写出强光照射变色玻璃时发生反应的化学方程式______ 。
| 营养成分 | 含量(每100 g) | 营养成分 | 含量(每100 g) |
| 水分 | 9.9 g | 钙元素 | 23.00 mg |
| 脂肪 | 0.2 g | 铁元素 | 1.10 mg |
| 蛋白质 | 4.8 g | 硒元素 | 0.02 mg |
| 淀粉 | 82.5 g | 花青素 | 0.10 g |
| 纤维素 | 2.7 g | 其他 | …… |
②紫薯粉中的脂肪在人体内会水解成高级脂肪酸和
③蛋白质在人体内水解的最终产物是氨基酸,其结构可表示为R—CH(NH2)—X,则“—X”的名称为
④在酶的作用下,淀粉水解为葡萄糖,葡萄糖再转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式
(2)合理饮食、正确使用药物对人体健康至关重要。
①“中国居民平衡膳食宝塔”如图所示,位于最上层且每天不超过25g的能量物质是

②某品牌饼干的配料标签如图所示,其中苯甲酸钠的作用是
| 配料: 小麦粉 食用植物油 葡萄糖浆 食用油 苯甲酸钠 …… |
③三硅酸镁(Mg2Si3O8·nH2O)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2·H2O等物质的化学方程式
(3)材料的生产与使用是人类文明和生活进步的一个重要标志。
①我国C919大型客机的机身蒙皮使用的是第三代铝锂合金材料,选用铝锂合金的优点是
②铁路建设中如何防止铁轨的腐蚀是工程技术人员攻克的难题之一。钢铁在潮湿的空气中易发生吸氧腐蚀如图所示,则正极的电极反应式为

③玻璃中加入适量的溴化银(AgBr)和氧化铜的微小晶粒,经过适当的热处理,可以制成变色玻璃,请写出强光照射变色玻璃时发生反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题:
(1)下列四种化合物中含铜量最高的是________ (填字母)
A.Cu5FeS4 B.CuFeS2 C.Cu2S D.Cu2(OH)2CO3
(2)2014年我国精炼铜产量796万吨,若全部由含Cu2S质量分数为32%的铜矿石冶炼得到,则需要铜矿石质量为__________ 万吨.(保留一位小数)
(3)可溶性铜盐常用于生产其它含铜化合物.在KOH溶液中加入一定量的CuSO4溶液,再加入一定量的还原剂﹣﹣肼(N2H4),加热并保持温度在90℃,生成一种对环境无污染的气体,反应完全后,分离,洗涤,真空干燥得到纳米氧化亚铜固体(Cu2O).
①该制备过程的反应方程式为_________________ .
②工业上常用的固液分离设备有_______ (填字母)
A.离心机 B.分馏塔 C.框式压滤机 D.反应釜
(4)我国出土的青铜器工艺精湛,具有很高的艺术价值和历史价值.但出土的青铜器大多受到环境腐蚀.如图是青铜器在潮湿环境中发生电化学腐蚀的原理示意图:
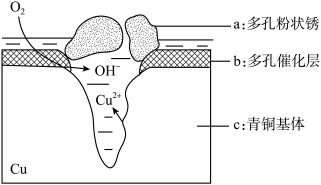
①腐蚀过程中,负极是_________ (填“a”“b”或“c”),正极反应方程式为_______________ .
②环境中的Cl﹣扩散到孔口,并与正极产物和负极产物生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为___________________ .
(1)下列四种化合物中含铜量最高的是
A.Cu5FeS4 B.CuFeS2 C.Cu2S D.Cu2(OH)2CO3
(2)2014年我国精炼铜产量796万吨,若全部由含Cu2S质量分数为32%的铜矿石冶炼得到,则需要铜矿石质量为
(3)可溶性铜盐常用于生产其它含铜化合物.在KOH溶液中加入一定量的CuSO4溶液,再加入一定量的还原剂﹣﹣肼(N2H4),加热并保持温度在90℃,生成一种对环境无污染的气体,反应完全后,分离,洗涤,真空干燥得到纳米氧化亚铜固体(Cu2O).
①该制备过程的反应方程式为
②工业上常用的固液分离设备有
A.离心机 B.分馏塔 C.框式压滤机 D.反应釜
(4)我国出土的青铜器工艺精湛,具有很高的艺术价值和历史价值.但出土的青铜器大多受到环境腐蚀.如图是青铜器在潮湿环境中发生电化学腐蚀的原理示意图:

①腐蚀过程中,负极是
②环境中的Cl﹣扩散到孔口,并与正极产物和负极产物生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.Ti、Na、Mg、C、N、O、Fe等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)已知C、CO的燃烧热分别为393.5kJ/mol和283.0kJ/mol,写出碳不完全燃烧生成CO的热化学方程式___________ 。
(2)Na、Mg、C、N、O的第一电离能由大到小的顺序为___________ 。
(3)基态 原子最高能层的原子轨道形状为
原子最高能层的原子轨道形状为___________ ,其价电子轨道表示式为___________ 。
(4)钢铁发生吸氧腐蚀时正极的电极反应式为:___________ 。为防止钢铁输水管的腐蚀,可用导线将其与镁块连接,这种防护方法为___________ 。(电化学保护法中的一种)
(5)用琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是___________ 。
II.制备硫酸四氨合铜晶体
①取20mL配制好的硫酸铜溶液于试管中,向其中滴加1mol/L氨水,有蓝色沉淀生成。
②继续慢慢加入氨水并振荡试管,沉淀逐渐消失,生成深蓝色溶液。
(6) 中,形成配位键提供孤电子对的原子是
中,形成配位键提供孤电子对的原子是___________ (填元素符号),1mol该微粒中,含有σ键的数目为___________  (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(7)步骤②中蓝色沉淀溶解的离子方程式为___________ 。
(8)步骤③中加入无水乙醇的目的是___________ 。
(1)已知C、CO的燃烧热分别为393.5kJ/mol和283.0kJ/mol,写出碳不完全燃烧生成CO的热化学方程式
(2)Na、Mg、C、N、O的第一电离能由大到小的顺序为
(3)基态
 原子最高能层的原子轨道形状为
原子最高能层的原子轨道形状为(4)钢铁发生吸氧腐蚀时正极的电极反应式为:
(5)用琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是II.制备硫酸四氨合铜晶体
①取20mL配制好的硫酸铜溶液于试管中,向其中滴加1mol/L氨水,有蓝色沉淀生成。
②继续慢慢加入氨水并振荡试管,沉淀逐渐消失,生成深蓝色溶液。
③再向试管中加入15mL无水乙醇,混合后静置30分钟,有深蓝色晶体析出
(6)
 中,形成配位键提供孤电子对的原子是
中,形成配位键提供孤电子对的原子是 (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(7)步骤②中蓝色沉淀溶解的离子方程式为
(8)步骤③中加入无水乙醇的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题。
(1)将下列物质进行分类:①CH3CH2CH2CH3和(CH3)2CHCH3;②红磷与白磷、③乙醇(CH3CH2OH)与二甲醚(CH3OCH3)、④金刚石与石墨、⑤冰与水、⑥16O与18O、⑦CH2=CH2和CH3CH=CH2;⑧CH3CH2CH2CH(C2H5)CH3和CH3CH2CH2CH(CH3)C2H5,用数字序号回答下列问题:
A.互为同分异构体的是___________ 。
B.属于同一种化合物的是___________ 。
C.互为同系物的是___________ 。
(2)分析下列烃分子,完成填空。
①CH3—CH2—CH2—CH2—CH3 ②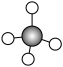
i.写出①有3个—CH3的同分异构体的结构简式:___________ 。
ii.②为甲烷的___________ 模型。
(3)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
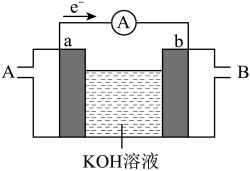
假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为___________ 。如果消耗甲醇160 g,假设化学能完全转化为电能,则转移电子的数目为___________ 。
(1)将下列物质进行分类:①CH3CH2CH2CH3和(CH3)2CHCH3;②红磷与白磷、③乙醇(CH3CH2OH)与二甲醚(CH3OCH3)、④金刚石与石墨、⑤冰与水、⑥16O与18O、⑦CH2=CH2和CH3CH=CH2;⑧CH3CH2CH2CH(C2H5)CH3和CH3CH2CH2CH(CH3)C2H5,用数字序号回答下列问题:
A.互为同分异构体的是
B.属于同一种化合物的是
C.互为同系物的是
(2)分析下列烃分子,完成填空。
①CH3—CH2—CH2—CH2—CH3 ②

i.写出①有3个—CH3的同分异构体的结构简式:
ii.②为甲烷的
(3)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】随着科学技术的进步,硫及其化合物的研究越来越深入。
(1)共生工程可以促进化学工业的发展,并改善环境。
①下列有关环境问题的说法错误的是________ (填序号字母)。
a.空气中SO2浓度过高会加重呼吸系统和心脑血管疾病
b.SO2、NOx、CO2的大量排放都会造成酸雨
c.氮的氧化物和碳氢化合物大量排放可能引发光化学烟雾
d.“静电除尘”、“燃煤固硫”、“低碳经济”都能改善空气质量
②发电厂产生的SO2尾气中的可直接用氨水吸收,变废为宝。若用15L 2.0 mol 氨水充分吸收4480L含10%的SO2硫酸尾气(气体体积已折算成标准状况)。充分反应后吸收液中的溶质为
氨水充分吸收4480L含10%的SO2硫酸尾气(气体体积已折算成标准状况)。充分反应后吸收液中的溶质为________ 。
③利用发电厂产生的SO2制成以水为电解质的SO2质子交换膜燃料电池,该电池电动势为1. 06V。电池工作时负极反应式为________ 。
(2)将发电厂产生的SO2通入含有Na2S、Na2CO3的废液中可制得Na2S2O3·5H2O,通入SO2过程中的现象是:通了一段时间后,产生气体并析出沉淀,沉淀量逐渐增多;沉淀量逐渐减少并形成清液;停止通SO2,过滤后母液经蒸发浓缩,冷却得Na2S2O3·5H2O晶体(提示:)。上述过程中析出沉淀时发生的氧化还原反应的化学方程式为:________ 。调节废液中Na2S和Na2CO3的物质的量之比为________ ,时可以恰好完全反应生成Na2S2O3·5H2O。
(1)共生工程可以促进化学工业的发展,并改善环境。
①下列有关环境问题的说法错误的是
a.空气中SO2浓度过高会加重呼吸系统和心脑血管疾病
b.SO2、NOx、CO2的大量排放都会造成酸雨
c.氮的氧化物和碳氢化合物大量排放可能引发光化学烟雾
d.“静电除尘”、“燃煤固硫”、“低碳经济”都能改善空气质量
②发电厂产生的SO2尾气中的可直接用氨水吸收,变废为宝。若用15L 2.0 mol
 氨水充分吸收4480L含10%的SO2硫酸尾气(气体体积已折算成标准状况)。充分反应后吸收液中的溶质为
氨水充分吸收4480L含10%的SO2硫酸尾气(气体体积已折算成标准状况)。充分反应后吸收液中的溶质为③利用发电厂产生的SO2制成以水为电解质的SO2质子交换膜燃料电池,该电池电动势为1. 06V。电池工作时负极反应式为
(2)将发电厂产生的SO2通入含有Na2S、Na2CO3的废液中可制得Na2S2O3·5H2O,通入SO2过程中的现象是:通了一段时间后,产生气体并析出沉淀,沉淀量逐渐增多;沉淀量逐渐减少并形成清液;停止通SO2,过滤后母液经蒸发浓缩,冷却得Na2S2O3·5H2O晶体(提示:)。上述过程中析出沉淀时发生的氧化还原反应的化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:正极_________ , 负极_________ 。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用如图所示的方案,其中焊接在闸门上的固体材料R可以采用_________。
(3)如图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的_________ 极。
①若溶液的pH=7,则该溶液中c( )
)_________ c(Cl-)。
②若溶液的pH>7,则该溶液中c( )
)_________ c(Cl-)。
③若c( )<c (Cl-),则溶液的pH
)<c (Cl-),则溶液的pH_________ 7。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:正极
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用如图所示的方案,其中焊接在闸门上的固体材料R可以采用_________。
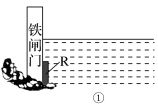
| A.铜 | B.钠 | C.锌 | D.石墨 |
(3)如图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的

①若溶液的pH=7,则该溶液中c(
 )
)②若溶液的pH>7,则该溶液中c(
 )
)③若c(
 )<c (Cl-),则溶液的pH
)<c (Cl-),则溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有同学设计了一个实验,以研究钢铁腐蚀的情况,实验装置如图所示,操作过程是:在水槽中的试管内置一枚铁钉,放置数天观察,请你把有关可能的实验现象的原因及解释补充完全:
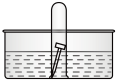
(1)若试管内液面上升,则溶液呈______ 性,发生______ 腐蚀,电极反应式:负极______ ,正极______ 。
(2)若试管内液面下降,则溶液呈______ 性,发生______ 腐蚀,电极反应式:负极______ ,正极______ 。

(1)若试管内液面上升,则溶液呈
(2)若试管内液面下降,则溶液呈
您最近一年使用:0次
【推荐3】电化学在化工、冶金、机械、电子、航空、航天、轻工、仪表、医学、材料、能源、金属腐蚀与防护、环境科学等科技领域获得了广泛的应用。
Ⅰ.电解精炼镓的装置如图所示,粗镓含 、
、 、
、 杂质,已知镓(
杂质,已知镓( )的化学性质与铝(
)的化学性质与铝( )相似,金属活动性顺序为
)相似,金属活动性顺序为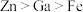 ,镓(
,镓( )的熔点为29.8℃。
)的熔点为29.8℃。
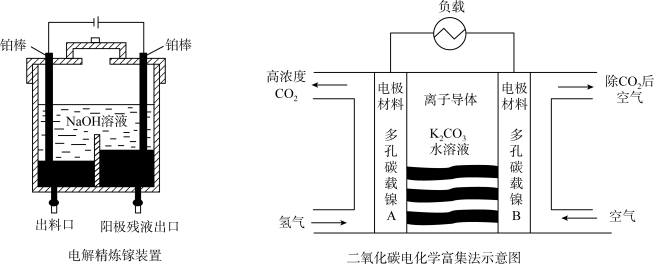
(1)电解后,电解槽底部阳极泥中所含的金属有_____ 。
(2)电解过程中阴极的电极反应式是_____ 。
Ⅱ.载人航天器中的物质和能源资源十分宝贵,二氧化碳的富集与转化是氧气再生的核心问题,电化学富集二氧化碳的方法如图所示。回答下列问题:
(3)离子导体中, 向多孔碳载镍
向多孔碳载镍_____ (填“A”或“B”)电极移动。
(4)负极的电极反应式是_____ 。
(5)在多孔碳载镍A电极上消耗1
 ,理论上多孔碳载镍B电极转化的
,理论上多孔碳载镍B电极转化的 在标准状况下的体积是
在标准状况下的体积是_____ L。
Ⅲ.日常生活中使用的金属往往含有杂质,当这样的金属与潮湿的空气或者电解质溶液接触时,会在其表面的杂志附近形成许多微小的原电池而被腐蚀。钢铁吸氧腐蚀的原理如图所示。
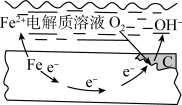
(6)钢铁吸氧腐蚀的正极反应式是_____ 。
(7)下列关于金属腐蚀的防护说法正确的是_____ 。
①用电镀的方法,在钢铁制品表面镀上一层不易被腐蚀的金属,能够减缓金属的腐蚀。
②镀铜铁制品镀层受损后,铁制品比受损前更易生锈。
③改变金属内部组成、结构可以防止金属腐蚀。
④牺牲阳极保护法是将被保护的金属作正极,以一种活动性较强的金属作负极。
⑤外加电流阴极保护法是将被保护的金属作阴极,惰性电极作辅助阳极,连接直流电源。
Ⅰ.电解精炼镓的装置如图所示,粗镓含
 、
、 、
、 杂质,已知镓(
杂质,已知镓( )的化学性质与铝(
)的化学性质与铝( )相似,金属活动性顺序为
)相似,金属活动性顺序为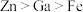 ,镓(
,镓( )的熔点为29.8℃。
)的熔点为29.8℃。
(1)电解后,电解槽底部阳极泥中所含的金属有
(2)电解过程中阴极的电极反应式是
Ⅱ.载人航天器中的物质和能源资源十分宝贵,二氧化碳的富集与转化是氧气再生的核心问题,电化学富集二氧化碳的方法如图所示。回答下列问题:
(3)离子导体中,
 向多孔碳载镍
向多孔碳载镍(4)负极的电极反应式是
(5)在多孔碳载镍A电极上消耗1

 ,理论上多孔碳载镍B电极转化的
,理论上多孔碳载镍B电极转化的 在标准状况下的体积是
在标准状况下的体积是Ⅲ.日常生活中使用的金属往往含有杂质,当这样的金属与潮湿的空气或者电解质溶液接触时,会在其表面的杂志附近形成许多微小的原电池而被腐蚀。钢铁吸氧腐蚀的原理如图所示。

(6)钢铁吸氧腐蚀的正极反应式是
(7)下列关于金属腐蚀的防护说法正确的是
①用电镀的方法,在钢铁制品表面镀上一层不易被腐蚀的金属,能够减缓金属的腐蚀。
②镀铜铁制品镀层受损后,铁制品比受损前更易生锈。
③改变金属内部组成、结构可以防止金属腐蚀。
④牺牲阳极保护法是将被保护的金属作正极,以一种活动性较强的金属作负极。
⑤外加电流阴极保护法是将被保护的金属作阴极,惰性电极作辅助阳极,连接直流电源。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电化学是化学研究重要分支,在生产生活中发挥着非常重要的作用。请回答下列问题:
铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为 。
。
(1)放电时,正极的电极反应式:______ ,电解质溶液中硫酸的浓度______ (填“增大”“减小”或“不变”),当外电路通过1mol 时,理论上负极板的质量增加
时,理论上负极板的质量增加______ g。
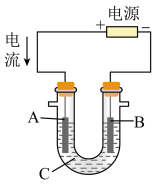
(2)用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。
如下图所示,电解液c选用______ 溶液,A电极的材料是______ ,B电极反应式是______ 。
铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为
 。
。(1)放电时,正极的电极反应式:
 时,理论上负极板的质量增加
时,理论上负极板的质量增加(2)用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。
如下图所示,电解液c选用

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则电子由_____ (填“a”或“b”,下同) 极流向_____ 极,电解质溶液中 移向
移向_____ 极,a极上的电极反应式为___________________ 。
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。其正极反应方程式为___________ ,若将燃料改为CH4,写出其负极反应方程式_________ 。

(3)图为青铜器在潮湿环境中因发生电化学反应而被腐蚀的原理示意图。

①腐蚀过程中,负极是_________ (填图中字母“a”或“b”或“c”);
②环境中的Cl- 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为_______________________ ;
③若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为_______ L(标况)。
 移向
移向
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。其正极反应方程式为

(3)图为青铜器在潮湿环境中因发生电化学反应而被腐蚀的原理示意图。

①腐蚀过程中,负极是
②环境中的Cl- 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为
③若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷(或氢气、一氧化碳等可燃性气体)和氧气构成燃料电池,则通入甲烷气体的一极是原电池的____ 极,该极的电极反应式是____ ,电池工作时的总反应的离子方程式是_____ 。
(2)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极气体,空气与CO2的混合气体为正极气体,制得650 ℃下工作的燃料电池,完成下列反应式:
正极:_______ ,
负极:2CO+2CO32--4e-=4CO2。
总反应:______ 。
(3)铅蓄电池放电时,总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O,由此可以判断:
①原电池的电极材料:负极:__ 。
②电极反应式:正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,负极反应式为_______ 。
③工作后,铅蓄电池里电解质溶液的pH____ (填“变大”“变小”或“不变”),理由是_____ 。
(2)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极气体,空气与CO2的混合气体为正极气体,制得650 ℃下工作的燃料电池,完成下列反应式:
正极:
负极:2CO+2CO32--4e-=4CO2。
总反应:
(3)铅蓄电池放电时,总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O,由此可以判断:
①原电池的电极材料:负极:
②电极反应式:正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,负极反应式为
③工作后,铅蓄电池里电解质溶液的pH
您最近一年使用:0次



