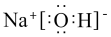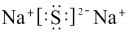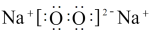下列变化过程中,所需克服的作用力均相同的是
| A.干冰熔化,氢氧化钠由固态变为熔融态 |
| B.氯化氢溶于水,氯化钠溶于水 |
| C.过氧化氢受热分解,碘化氢气体受热分解 |
| D.大理石高温生成二氧化碳,碘晶体升华为碘蒸气 |
22-23高一上·甘肃天水·期末 查看更多[3]
甘肃省天水市第一中学2022-2023学年高一上学期期末考试化学试题福建省莆田华侨中学2022-2023学年高一下学期5月月考化学试题(已下线)寒假作业11 化学键-【寒假分层作业】2024年高一化学寒假培优练(人教版2019必修第一册)
更新时间:2023-03-18 19:26:25
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
| A.CH3CH3的熔、沸点低于CH3(CH2)2CH3,是由于CH3(CH2)2CH3中氢键数目更多 |
| B.液态氟化氢中氟化氢分子之间形成氢键,可写为(HF)n,则NO2分子间也是因氢键而聚合形成N2O4 |
| C.邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点高 |
| D.H2O的沸点比HF高,是由于单位物质的量的水分子形成的氢键数目多 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列含氧酸中酸性最强是
| A.HClO2 | B.H2SeO3 | C.HBO2 | D.HMnO4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法不正确的是
| A.化学反应的实质是旧键的断裂,新键的形成 |
| B.石墨转化为金刚石的反应是吸热反应,说明金刚石比石墨稳定 |
| C.原电池反应的实质是自发进行的氧化还原反应 |
| D.元素周期律的实质是元素原子核外电子排布呈周期性变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列变化中,需要克服分子间作用力是的( )
| A.NaCl溶于水 | B.干冰升华 |
| C.加热碘化氢使之分解 | D.加热硅晶体使之熔化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】将金属钠投入足量水中,关于此过程说法错误的是
| A.破坏了金属键 | B.破坏了极性共价键 |
| C.生成了离子键 | D.生成了非极性共价键 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】黑火药爆炸的主要反应为 。下列表示相关微粒的化学用语错误的是
。下列表示相关微粒的化学用语错误的是
 。下列表示相关微粒的化学用语错误的是
。下列表示相关微粒的化学用语错误的是| A.硫原子核外电子有16种运动状态 |
B. 的结构示意图: 的结构示意图: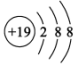 |
C.基态 原子价电子的轨道表达式: 原子价电子的轨道表达式: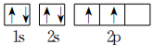 |
D. 和 和 形成离子键的过程: 形成离子键的过程: |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】甲、乙、丙、丁都是短周期元素,其中甲、丁在周期表中的相对位置如下表所示,甲原子最外层电子数是其内层电子数的2倍,乙单质在空气中燃烧发出黄色火焰,丙是地壳中含量最高的金属元素,下列判断正确的是
| 甲 | |||
| 丁 |
| A.原子半径:丙>乙 |
| B.乙和丁的最高价氧化物的水化物均可和丙单质反应 |
| C.基态甲原子有5种不同的运动状态 |
| D.甲、乙的最高价氧化物均是共价化合物 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列反应中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是
A.NH4Cl NH3↑+HCl↑ NH3↑+HCl↑ | B.CaO+3C CaC2+CO↑ CaC2+CO↑ |
| C.2Na2O2+2CO2=2Na2CO3+O2 | D.2NaOH+Cl2=NaCl+NaClO+H2O |
您最近一年使用:0次
【推荐3】离子液体是指由体积较大的阴、阳离子组成,并且在室温或接近室温下呈液态的盐,也称为低温熔融盐。有许多优点,例如难挥发,有良好的导电性,可作溶剂、电解质、催化剂等。1-正丁基-3-甲基咪唑六氟磷酸盐是一种离子液体,结构简式如图,下列关于它的叙述正确的是
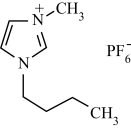 或
或
A.该新型化合物含有的C、N、P元素均为 杂化 杂化 |
| B.1-正丁基-3-甲基咪唑六氟磷酸盐属于含共价键的离子化合物 |
| C.电负性:F>N>H>C |
| D.该新型化合物的组成元素全部位于元素周期表p区 |
您最近一年使用:0次