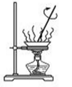
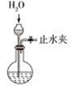
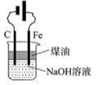
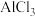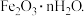下列有关实验说法正确的是
| A.对于含重金属(如铅、汞或镉等)离子的废液,可用Na2S或NaOH进行沉淀处理 |
| B.在给粗糙铁质镀件电镀时,用砂纸将镀件打磨干净后即可直接与直流电源负极相连 |
| C.在润洗洁净的碱式滴定管时,先从滴定管上口加入3~5 mL待盛装碱液,然后轻挤压滴定管中的玻璃珠,将液体从滴定管下端放入预置的烧杯中 |
| D.中和热测定实验中,玻璃搅拌棒应左右匀速搅拌,以减少热量散失 |
23-24高二上·浙江·期末 查看更多[2]
更新时间:2023/04/06 15:55:56
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
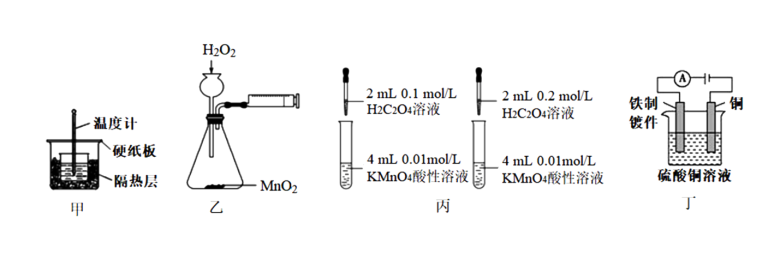
【推荐1】某实验小组学生用50 mL0.50 mol·L-1的盐酸与50 mL0.55 mol·L-1的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和反应的反应热ΔH = -52 kJ·mol-1,下列说法不正确 的是


| A.图中实验装置缺少环形玻璃搅拌棒 |
| B.烧杯间填满碎纸条的作用是减少实验过程中的热量损失,减小实验误差 |
| C.若用铜丝做成环形搅拌棒,求得的反应热ΔH > -52 kJ·mol-1 |
| D.把盐酸体积改为60 mL,求得中和反应的反应热ΔH < -52 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】中和热测定实验,用50 mL 0.50 mol/L盐酸和50 mL0.55 mol/LNaOH溶液进行实验,下列说法正确的是
| A.在测定中和热实验中必不可少的仪器有:分液漏斗、量筒、烧杯、玻璃棒 |
| B.使用环形玻璃搅拌棒是为了使反应物混合均匀,减小误差 |
| C.改用60 mL 0.5 mol/L盐酸跟50 mL0.50 mol/LNaOH溶液进行反应,求出的中和热数值和原来不相同 |
| D.测量酸溶液的温度后,未冲洗温度计就测碱溶液的温度,会使求得的中和热的数值偏大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】如图是常温下向10mL某浓度的盐酸(滴有酚酞)中逐滴加入0.10mol·L−1NaOH溶液时,溶液的pH随NaOH溶液的体积V变化的曲线,下列相关判断错误的是


| A.原盐酸的浓度为0.10mol·L−1 |
| B.滴定过程中,眼睛应注视锥形瓶中溶液颜色的变化 |
| C.达到滴定终点时不慎多加了1滴NaOH溶液(约0.04mL),继续加水至40mL,所得溶液的pH为10 |
| D.滴定后仰视读数,则最终测得的待测盐酸浓度偏小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用标准NaOH滴定未知浓度的醋酸溶液,下列说法中,正确的是
| A.滴定管、锥形瓶均用待测醋酸溶液润洗后进行滴定 |
| B.滴定时,眼睛要注视滴定管的读数 |
| C.滴定前平视滴定管刻度线,滴定终点俯视刻度线,滴定结果偏低 |
| D.用酚酞试液作指示剂,当溶液由红色变为无色,且半分钟内不恢复红色为滴定终点 |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
【推荐1】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.利用电镀在铁上镀铜,当阳极消耗1 mol Cu时电路中转移的电子数大于 |
B.64g 的中心原子价电子对数为 的中心原子价电子对数为 |
C.100mL 的醋酸铵溶液中 的醋酸铵溶液中 的数目为 的数目为 |
D.1mol基态铬原子中含有的未成对电子数为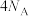 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】关于下列装置说法正确的是
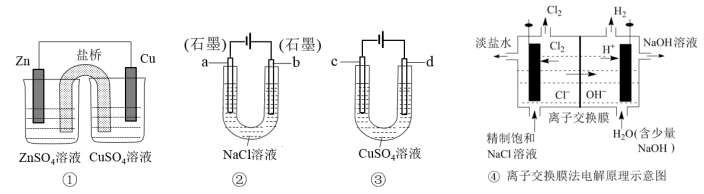

| A.装置①中,盐桥中的Cl-移向ZnSO4溶液 |
| B.装置②工作一段时间后,b极附近溶液的pH增大 |
| C.用装置③精炼铜时,c极为粗铜 |
| D.④装置的离子交换膜允许阳离子、阴离子、水分子自由通过 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列仪器的有关说法,错误的是


| A.①和⑤实验前需检漏 | B.②④⑥可直接用酒精灯加热 |
| C.②和④可用于物质提纯 | D.③和⑤可用于量取液体的体积 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.可用pH试纸检测新制氯水的pH |
| B.用高锰酸钾溶液可以除去甲烷中混有的乙烯 |
| C.强氧化物如KMnO4、KClO3、Na2O2等固体不能随意丢弃,可放回原试剂瓶 |
D.如果不慎将酸沾到皮肤上,应立即用大量水冲洗,然后用3%~5% 溶液冲洗 溶液冲洗 |
您最近一年使用:0次




 镀锌的铁
镀锌的铁 比马口铁
比马口铁