下列处理方法对应的反应方程式一定错误的是
A.利用沉淀剂NaHS除去废水中的 |
B.加碘食盐中碘元素的检验: |
C.用生物质热解气CO将 还原为 还原为 |
D.用双氧水擦拭变黑的白色油画: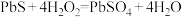 |
2023·福建福州·模拟预测 查看更多[3]
更新时间:2023-04-08 21:20:29
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】在水溶液中,下列离子方程式书写错误的是( )
| A.用醋酸除水垢:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O + CO2↑ |
| B.硫酸铜溶液与氢氧化钡溶液混合:Cu2++20H-=Cu(OH)2↓ |
| C.向稀盐酸中加入适量铁粉:Fe+2H+=Fe2++H2↑ |
| D.石灰乳与稀盐酸混合:Ca(OH)2+2H+= Ca2++2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列指定反应的离子方程式正确的是
A.电解熔融NaCl:2Cl-+2H2O 2OH-+Cl2↑+H2↑ 2OH-+Cl2↑+H2↑ |
| B.用氨水溶解AgCl沉淀:Ag++2NH3·H2O=[Ag(NH3)2]++2H2O |
C.Na2CO3溶液吸收溴蒸气:3CO +Br2=Br-+BrO +Br2=Br-+BrO +3CO2 +3CO2 |
| D.金属钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知溴水(Br2)显橙黄色,碘水(I2)显棕黄色; 还原性:Br-<Fe2+<I-<SO32-。有一无色未知溶液可能含有K+、Fe2+、SO42-、I-、SO32-中的一种或者几种,现做以下实验:
①取部分溶液加入少量溴水,振荡,溶液呈无色;
②向①的溶液中加入过量氯化钡溶液,产生白色沉淀,再加过量稀硝酸沉淀不溶解;
③取少量②的溶液滴入足量AgNO3溶液,有白色沉淀生成。
下列关于无色溶液组成的判断正确的是
①取部分溶液加入少量溴水,振荡,溶液呈无色;
②向①的溶液中加入过量氯化钡溶液,产生白色沉淀,再加过量稀硝酸沉淀不溶解;
③取少量②的溶液滴入足量AgNO3溶液,有白色沉淀生成。
下列关于无色溶液组成的判断正确的是
| A.肯定含有SO32-,肯定不含Fe2+、I-,可能含有K+、SO42- |
| B.肯定含有SO42-,肯定不含Fe2+、I-,可能含有K+、SO32- |
| C.肯定含有K+、SO32-,肯定不含Fe2+,可能含有SO42-、I- |
| D.肯定含有SO42-、SO32-,肯定不含Fe2+、I-,可能含有K+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】将3.75g镁铝合金投入一定量热的浓硝酸中,合金完全溶解,共产生0.05molNO与0.2molNO2,向反应后的溶液中加入过量的NaOH溶液,最终得到一定量的白色沉淀。关于此过程说法错误的是
| A.有0.25molHNO3被还原 | B.有0.60molHNO3参加了反应 |
| C.转移电子物质的量为0.35mol | D.白色沉淀质量为9.7g |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】已知:还原性HSO3¯>I¯,氧化性IO3¯> I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法不正确的是


| A.0--b :3HSO3-+ IO3-= 3SO42-+ I-+ 3H+ |
| B.a点时消耗NaHSO3的物质的量为1.2 mol |
| C.b点时的还原产物可能是KI或NaI,b~c间的还原产物是I2 |
| D.当溶液中I¯与I2的物质的量之比为5∶2时,加入的KIO3为1.8mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列说法正确的是 )
| A.用湿润的pH试纸测得0.01mol/L的HCl水溶液的pH为2 |
| B.常温下,0.1mol/LCH3COONa溶液的pH>7,说明CH3COOH是弱酸 |
| C.用碱式滴定管量取20.00mL酸性KMnO4溶液 |
| D.Mg(OH)2固体能溶于饱和NH4Cl溶液,其主要原因是NH4Cl在溶液中水解显酸性,中和Mg(OH)2电离出的OH—,从而促进了Mg(OH)2的溶解平衡 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】某实验小组以粗镍(含少量 和
和 杂质)为原料制备
杂质)为原料制备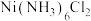 ,并测定相关组分的含量,制备流程示意图如下:
,并测定相关组分的含量,制备流程示意图如下: 为绿色难溶物;
为绿色难溶物;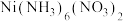 、
、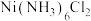 均为可溶于水的蓝紫色晶体,碱性条件下稳定存在,下列说法不正确的是
均为可溶于水的蓝紫色晶体,碱性条件下稳定存在,下列说法不正确的是
 和
和 杂质)为原料制备
杂质)为原料制备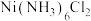 ,并测定相关组分的含量,制备流程示意图如下:
,并测定相关组分的含量,制备流程示意图如下:
 为绿色难溶物;
为绿色难溶物;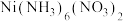 、
、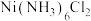 均为可溶于水的蓝紫色晶体,碱性条件下稳定存在,下列说法不正确的是
均为可溶于水的蓝紫色晶体,碱性条件下稳定存在,下列说法不正确的是A.试剂X的作用是调节 除去 除去 和 和 杂质,则试剂X可为 杂质,则试剂X可为 |
B.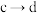 过程的转化离子方程式为 过程的转化离子方程式为 |
C.实验配制3.0 稀硝酸250 稀硝酸250 需要的玻璃仪器有烧杯、量筒、玻璃棒、250 需要的玻璃仪器有烧杯、量筒、玻璃棒、250 容量瓶 容量瓶 |
| D.步骤c、d中为防止氨水分解及降低固体溶解度需0~10℃冷水浴控温,则温度计应在水浴中 |
您最近一年使用:0次

 +OH-=NH3·H2O
+OH-=NH3·H2O +3Cl-+4H++H2O
+3Cl-+4H++H2O ,
, 。在含大量
。在含大量 和
和 的浊液中滴加
的浊液中滴加 溶液,浊液中pX[
溶液,浊液中pX[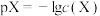 ,
, 、
、 、
、 ]与pH的关系如图。平衡常数K大于或等于
]与pH的关系如图。平衡常数K大于或等于 时认为反应不可逆(即完全反应)。下列叙述正确的是
时认为反应不可逆(即完全反应)。下列叙述正确的是
 直线代表pN和pH的关系
直线代表pN和pH的关系



