现有下列10种物质:①Al ②熔融KCl ③ ④
④ ⑤
⑤ ⑥NaOH溶液 ⑦酒精 ⑧
⑥NaOH溶液 ⑦酒精 ⑧ ⑨盐酸 ⑩稀硫酸
⑨盐酸 ⑩稀硫酸
(1)上述物质中属于电解质的有_______ ,能导电的有_______ 。(填序号)
(2)⑧在水溶液中电离方程式为_______ 。
(3)⑤的俗名是_______ ,其用途之一是做发酵剂,请用化学方程式解释这一用途:_______ 。
(4)向 溶液中逐滴加入
溶液中逐滴加入 溶液至
溶液至 恰好完全沉淀,发生反应的离子方程式为
恰好完全沉淀,发生反应的离子方程式为_______ 。
 ④
④ ⑤
⑤ ⑥NaOH溶液 ⑦酒精 ⑧
⑥NaOH溶液 ⑦酒精 ⑧ ⑨盐酸 ⑩稀硫酸
⑨盐酸 ⑩稀硫酸(1)上述物质中属于电解质的有
(2)⑧在水溶液中电离方程式为
(3)⑤的俗名是
(4)向
 溶液中逐滴加入
溶液中逐滴加入 溶液至
溶液至 恰好完全沉淀,发生反应的离子方程式为
恰好完全沉淀,发生反应的离子方程式为
更新时间:2023-04-13 22:22:09
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有以下物质:①NaCl晶体 ②液态SO3 ③铁(Fe) ④BaSO4固体 ⑤纯蔗糖(C12H22O11) ⑥熔化的KNO3。
请回答下列问题(用序号)
(1)以上物质中能导电的是________ 。
(2)以上物质中属于电解质的是________ 。
(3)以上物质中属于非电解质的是________ 。
(4)以上物质中溶于水后形成的水溶液能导电的是________ 。
请回答下列问题(用序号)
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
(4)以上物质中溶于水后形成的水溶液能导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有下列7种物质:
① ②NH4Cl ③
②NH4Cl ③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
请回答下列问题:
(1)属于电解质的有_______ (填序号),②物质的电子式为_______ 。
(2)准确配制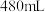 一定浓度的①溶液需要用到的玻璃仪器有烧杯、量筒、玻璃棒、
一定浓度的①溶液需要用到的玻璃仪器有烧杯、量筒、玻璃棒、_______ 。
(3)①溶液中加入少量的④反应的离子方程式为_______ 。
(4)将足量的⑧通入BaCl2溶液中,下列说法正确的是_______ 。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入Cl2或NH3,则溶液中均会出现白色沉淀
(5)用含⑧的烟气处理含Cr2O (被还原为Cr3+)的酸性废水时,所发生的离子反应为:
(被还原为Cr3+)的酸性废水时,所发生的离子反应为:_______ 。
(6)关于以上7种物质的说法不正确的有_______。
①
 ②NH4Cl ③
②NH4Cl ③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
请回答下列问题:
(1)属于电解质的有
(2)准确配制
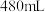 一定浓度的①溶液需要用到的玻璃仪器有烧杯、量筒、玻璃棒、
一定浓度的①溶液需要用到的玻璃仪器有烧杯、量筒、玻璃棒、(3)①溶液中加入少量的④反应的离子方程式为
(4)将足量的⑧通入BaCl2溶液中,下列说法正确的是
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入Cl2或NH3,则溶液中均会出现白色沉淀
(5)用含⑧的烟气处理含Cr2O
 (被还原为Cr3+)的酸性废水时,所发生的离子反应为:
(被还原为Cr3+)的酸性废水时,所发生的离子反应为:(6)关于以上7种物质的说法不正确的有_______。
| A.加碘食盐中的“碘”指的是⑥ | B.液态③可做制冷剂 |
| C.⑤和⑧都有漂白性 | D.⑦性质稳定,在自然界中以游离态存在 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有如下各物质:①酒精②固态苛性钾③硫化氢④氨水⑤硫酸⑥金属镁⑦石墨⑧二氧化碳⑨氢氧化钡⑩胆矾,请用物质序号填空:
(1)属于电解质的有___________ 。
(2)属于非电解质的有___________ 。
(3)属于强电解质的有___________ 。
(4)既不是电解质,又不是非电解质的是___________ ;
(5)能导电的是___________ 。
(1)属于电解质的有
(2)属于非电解质的有
(3)属于强电解质的有
(4)既不是电解质,又不是非电解质的是
(5)能导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有下列物质:
①氢氧化钡 ②KHSO4 ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铜 ⑦碳酸钠 ⑧蔗糖 ⑨熔融氯化钠 ⑩胆矾
请回答下列问题:
(1)可以导电的有_______ (填序号)
(2)属于电解质的有_______ (填序号)
(3)属于非电解质的有_______ (填序号)
(4)②在熔融状态时的电离方程式为_______
(5)写出“向②溶液中滴加①溶液”至中性的离子反应方程式:_______ ,继续向上述溶液中滴加氢氧化钡溶液反应的离子方程式:_______
(6)写出“向①溶液中通入少量⑤气体”反应的离子方程式:_______
(7)写出①溶液与⑦溶液反应的化学方程式:_______
①氢氧化钡 ②KHSO4 ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铜 ⑦碳酸钠 ⑧蔗糖 ⑨熔融氯化钠 ⑩胆矾
请回答下列问题:
(1)可以导电的有
(2)属于电解质的有
(3)属于非电解质的有
(4)②在熔融状态时的电离方程式为
(5)写出“向②溶液中滴加①溶液”至中性的离子反应方程式:
(6)写出“向①溶液中通入少量⑤气体”反应的离子方程式:
(7)写出①溶液与⑦溶液反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】运用分类的方法研究物质及其变化的规律是化学学习的有效途径。回答下列问题:
(1)将①Fe ②CO ③硫酸铜溶液 ④液态氯化氢 ⑤熔融氯化钠 ⑥固态烧碱 ⑦ 固体 ⑧CuO固体 ⑨氨气 ⑩
固体 ⑧CuO固体 ⑨氨气 ⑩ 晶体
晶体
按不同的分类标准填空:
a.碱性氧化物:_______ (填序号,下同);
b.电解质:_______ ;
c.上述状态下能导电的是_______ 。
(2)用上述物质,按要求填空。
a.⑩在熔融状态下的电离方程式为_______ ;
b.④和⑥在溶液中反应的离子方程式为_______ ;
c.将少量⑦投入③中的现象为_______ ;
d.用②还原⑧的化学方程式为_______ 。
(1)将①Fe ②CO ③硫酸铜溶液 ④液态氯化氢 ⑤熔融氯化钠 ⑥固态烧碱 ⑦
 固体 ⑧CuO固体 ⑨氨气 ⑩
固体 ⑧CuO固体 ⑨氨气 ⑩ 晶体
晶体按不同的分类标准填空:
a.碱性氧化物:
b.电解质:
c.上述状态下能导电的是
(2)用上述物质,按要求填空。
a.⑩在熔融状态下的电离方程式为
b.④和⑥在溶液中反应的离子方程式为
c.将少量⑦投入③中的现象为
d.用②还原⑧的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】以 为原料合成甲醇可以减少
为原料合成甲醇可以减少 的排放,实现碳的循环利用。一种
的排放,实现碳的循环利用。一种 催化剂对该反应有良好的催化效果。
催化剂对该反应有良好的催化效果。
Ⅰ.催化剂的合成
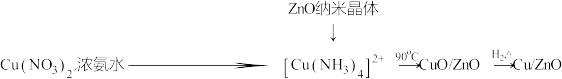
(1)氨水与 的反应
的反应___________ (填“属于”或“不属于”)氧化还原反应。
(2)补全上述过程中生成 的离子方程式:
的离子方程式:
Ⅱ.催化剂的性能测试
一定条件下使 、
、 混合气体通过反应器,检测反应器出口气体的成分及其含量,计算
混合气体通过反应器,检测反应器出口气体的成分及其含量,计算 的转化率和
的转化率和 的选择性以评价催化剂的性能。
的选择性以评价催化剂的性能。
已知:ⅰ。反应器内发生的反应有:
a.
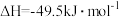
b.
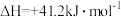
ⅱ. 选择性
选择性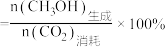
(3)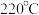 时,测得反应器出口气体中全部含碳物质的物质的量之比
时,测得反应器出口气体中全部含碳物质的物质的量之比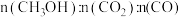
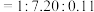 ,则该温度下
,则该温度下 转化率=
转化率=___________ 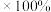 (列出计算式)。
(列出计算式)。
(4)其他条件相同时,反应温度对 的转化率和
的转化率和 的选择性的影响如下图所示:
的选择性的影响如下图所示:

①由图1可知实验中反应均未达到化学平衡状态的依据是___________ 。
②温度高于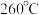 时,
时, 平衡转化率变化的原因是
平衡转化率变化的原因是___________ 。
③温度相同时, 选择性的实验值略高于平衡值(见图2),从化学反应速率的角度解释原因:
选择性的实验值略高于平衡值(见图2),从化学反应速率的角度解释原因:___________ 。
 为原料合成甲醇可以减少
为原料合成甲醇可以减少 的排放,实现碳的循环利用。一种
的排放,实现碳的循环利用。一种 催化剂对该反应有良好的催化效果。
催化剂对该反应有良好的催化效果。Ⅰ.催化剂的合成
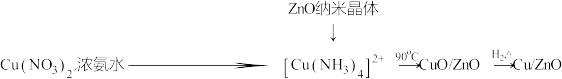
(1)氨水与
 的反应
的反应(2)补全上述过程中生成
 的离子方程式:
的离子方程式:

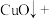
Ⅱ.催化剂的性能测试
一定条件下使
 、
、 混合气体通过反应器,检测反应器出口气体的成分及其含量,计算
混合气体通过反应器,检测反应器出口气体的成分及其含量,计算 的转化率和
的转化率和 的选择性以评价催化剂的性能。
的选择性以评价催化剂的性能。已知:ⅰ。反应器内发生的反应有:
a.

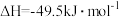
b.

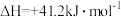
ⅱ.
 选择性
选择性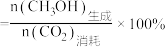
(3)
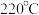 时,测得反应器出口气体中全部含碳物质的物质的量之比
时,测得反应器出口气体中全部含碳物质的物质的量之比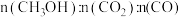
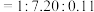 ,则该温度下
,则该温度下 转化率=
转化率=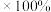 (列出计算式)。
(列出计算式)。(4)其他条件相同时,反应温度对
 的转化率和
的转化率和 的选择性的影响如下图所示:
的选择性的影响如下图所示:
①由图1可知实验中反应均未达到化学平衡状态的依据是
②温度高于
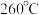 时,
时, 平衡转化率变化的原因是
平衡转化率变化的原因是③温度相同时,
 选择性的实验值略高于平衡值(见图2),从化学反应速率的角度解释原因:
选择性的实验值略高于平衡值(见图2),从化学反应速率的角度解释原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
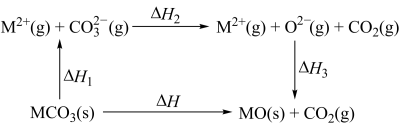
【推荐2】在煤炭中加入碳酸钙可减少酸雨的形成。在研究碳酸盐分解时发现MgCO3和CaCO3的能量关系如图所示(M=Ca、Mg),ΔH表达式为___________ ;已知CaCO3(s)=CaO(s)+CO2(g)ΔH>0,则该反应能自发进行的条件是___________ 。___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在 中加入蒸馏水,微热,
中加入蒸馏水,微热, 完全水解,产物之一是亚磷酸
完全水解,产物之一是亚磷酸 。
。
 易溶于水,它的结构式表示为
易溶于水,它的结构式表示为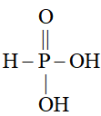 。
。 和
和 反应只生成
反应只生成 和
和 两种盐,其正盐溶液呈碱性。常温下,
两种盐,其正盐溶液呈碱性。常温下,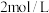 的亚磷酸溶液pH约为1。在
的亚磷酸溶液pH约为1。在 溶液中加入碘水振荡后,碘水的棕黄色褪去,再滴加溶液有黄
溶液中加入碘水振荡后,碘水的棕黄色褪去,再滴加溶液有黄 色沉淀析出。若在装有
色沉淀析出。若在装有 溶液的试管中加入
溶液的试管中加入 溶液,则析出黑色金属银沉淀,溶液中有无色气泡产生,在试管口变为红棕色。回答下列问题:
溶液,则析出黑色金属银沉淀,溶液中有无色气泡产生,在试管口变为红棕色。回答下列问题:
(1) 为
为__________ 盐(填“酸式”、“碱式”或“正”)。
(2)用化学方程式表示 和碘水的反应:
和碘水的反应:_______________ 。
 水溶液呈碱性的原因(用离子方程式表示):
水溶液呈碱性的原因(用离子方程式表示):_____________ 。
(3)根据上述事实,可以得知 是
是______ (填序号)。
A.强酸 B.弱酸 C.二元酸 D.三元酸 E.具有强氧化性 F.具有强还原性
 中加入蒸馏水,微热,
中加入蒸馏水,微热, 完全水解,产物之一是亚磷酸
完全水解,产物之一是亚磷酸 。
。 易溶于水,它的结构式表示为
易溶于水,它的结构式表示为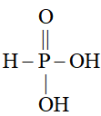 。
。 和
和 反应只生成
反应只生成 和
和 两种盐,其正盐溶液呈碱性。常温下,
两种盐,其正盐溶液呈碱性。常温下,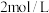 的亚磷酸溶液pH约为1。在
的亚磷酸溶液pH约为1。在 溶液中加入碘水振荡后,碘水的棕黄色褪去,再滴加溶液有黄
溶液中加入碘水振荡后,碘水的棕黄色褪去,再滴加溶液有黄 色沉淀析出。若在装有
色沉淀析出。若在装有 溶液的试管中加入
溶液的试管中加入 溶液,则析出黑色金属银沉淀,溶液中有无色气泡产生,在试管口变为红棕色。回答下列问题:
溶液,则析出黑色金属银沉淀,溶液中有无色气泡产生,在试管口变为红棕色。回答下列问题:(1)
 为
为(2)用化学方程式表示
 和碘水的反应:
和碘水的反应: 水溶液呈碱性的原因(用离子方程式表示):
水溶液呈碱性的原因(用离子方程式表示):(3)根据上述事实,可以得知
 是
是A.强酸 B.弱酸 C.二元酸 D.三元酸 E.具有强氧化性 F.具有强还原性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2021年是国际化学年十周年,中国的宣传口号是“化学一我们的生活,我们的未来”。下列为生产生活中一些常见的化学反应。
(1)反应2Al+Fe2O3 2Fe+Al2O3可用于野外焊接钢轨。
2Fe+Al2O3可用于野外焊接钢轨。
①该反应属于四种基本反应类型中的_____ 。
②该反应中,发生氧化反应的是_____ (填化学式,下同),还原产物是_____ 。
(2)ClO2是世卫组织确认的A级新型高效消毒剂,其安全性远高于氯气。一种制备方法为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,其中氧化剂与还原剂的物质的量之比为_____ 。ClO2在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为Cl-除去。下列试剂中可将
),需将其转化为Cl-除去。下列试剂中可将 ,转化为Cl-的是
,转化为Cl-的是_____ (填序号)。
A.FeSO4 B.O2 C.KMnO4 D.SO2
(3)小苏打(NaHCO3)可作为食品制作过程中的膨松剂。
①往饱和Na2CO3溶液中通入_____ (填化学式),过滤、干燥可得到NaHCO3。
②小苏打受热发生分解,产生的气体使面包松软,该反应的化学方程式为_____ 。
(1)反应2Al+Fe2O3
 2Fe+Al2O3可用于野外焊接钢轨。
2Fe+Al2O3可用于野外焊接钢轨。①该反应属于四种基本反应类型中的
②该反应中,发生氧化反应的是
(2)ClO2是世卫组织确认的A级新型高效消毒剂,其安全性远高于氯气。一种制备方法为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,其中氧化剂与还原剂的物质的量之比为
 ),需将其转化为Cl-除去。下列试剂中可将
),需将其转化为Cl-除去。下列试剂中可将 ,转化为Cl-的是
,转化为Cl-的是A.FeSO4 B.O2 C.KMnO4 D.SO2
(3)小苏打(NaHCO3)可作为食品制作过程中的膨松剂。
①往饱和Na2CO3溶液中通入
②小苏打受热发生分解,产生的气体使面包松软,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请用下列物质的序号填空:
A.Na2O2 B.Na2CO3 C.NaHCO3 D.K- Na合金E.Na F.Ca(ClO)2 G.CaCO3 H.NaCl
(1)可用于潜艇中供氧剂的是______________________________ ;
(2)可用于消毒饮用水的是_____________________________ ;
(3)可用作原子反应堆的导热剂是_______________________ ;
(4)可用作制取发酵粉或用于治疗胃酸过多的药物的是_____________________ ;
(5)广泛用于玻璃、制皂、造纸、纺织工业上的是____________________________ 。
A.Na2O2 B.Na2CO3 C.NaHCO3 D.K- Na合金E.Na F.Ca(ClO)2 G.CaCO3 H.NaCl
(1)可用于潜艇中供氧剂的是
(2)可用于消毒饮用水的是
(3)可用作原子反应堆的导热剂是
(4)可用作制取发酵粉或用于治疗胃酸过多的药物的是
(5)广泛用于玻璃、制皂、造纸、纺织工业上的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Na2CO3、NaHCO3是生活中常见的盐,某实验小组通过以下实验探究这两种物质的性质。
(1)称取两种固体各1g分别放入两支试管中,再各加入5mL水,充分振荡,并恢复至室温。发现Na2CO3完全溶解,而NaHCO3有剩余。由此得出结论:在相同温度下,_______ 。
(2)某学生设计如图所示装置进行NaHCO3的分解实验,并证实产物中有CO2产生。
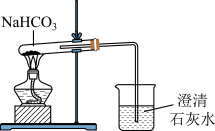
①试管中发生的化学反应方程式为_______ 。
②指出该学生设计的装置图的错误之处,并改正(文字说明即可)_______ 。
(3)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:
①称取mg样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,反应的化学方程式为_______ 。
③过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中Na2CO3的质量分数为_______ 。
(1)称取两种固体各1g分别放入两支试管中,再各加入5mL水,充分振荡,并恢复至室温。发现Na2CO3完全溶解,而NaHCO3有剩余。由此得出结论:在相同温度下,
(2)某学生设计如图所示装置进行NaHCO3的分解实验,并证实产物中有CO2产生。

①试管中发生的化学反应方程式为
②指出该学生设计的装置图的错误之处,并改正(文字说明即可)
(3)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:
①称取mg样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,反应的化学方程式为
③过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中Na2CO3的质量分数为
您最近一年使用:0次



