在 中加入蒸馏水,微热,
中加入蒸馏水,微热, 完全水解,产物之一是亚磷酸
完全水解,产物之一是亚磷酸 。
。
 易溶于水,它的结构式表示为
易溶于水,它的结构式表示为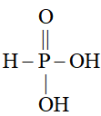 。
。 和
和 反应只生成
反应只生成 和
和 两种盐,其正盐溶液呈碱性。常温下,
两种盐,其正盐溶液呈碱性。常温下,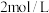 的亚磷酸溶液pH约为1。在
的亚磷酸溶液pH约为1。在 溶液中加入碘水振荡后,碘水的棕黄色褪去,再滴加溶液有黄
溶液中加入碘水振荡后,碘水的棕黄色褪去,再滴加溶液有黄 色沉淀析出。若在装有
色沉淀析出。若在装有 溶液的试管中加入
溶液的试管中加入 溶液,则析出黑色金属银沉淀,溶液中有无色气泡产生,在试管口变为红棕色。回答下列问题:
溶液,则析出黑色金属银沉淀,溶液中有无色气泡产生,在试管口变为红棕色。回答下列问题:
(1) 为
为__________ 盐(填“酸式”、“碱式”或“正”)。
(2)用化学方程式表示 和碘水的反应:
和碘水的反应:_______________ 。
 水溶液呈碱性的原因(用离子方程式表示):
水溶液呈碱性的原因(用离子方程式表示):_____________ 。
(3)根据上述事实,可以得知 是
是______ (填序号)。
A.强酸 B.弱酸 C.二元酸 D.三元酸 E.具有强氧化性 F.具有强还原性
 中加入蒸馏水,微热,
中加入蒸馏水,微热, 完全水解,产物之一是亚磷酸
完全水解,产物之一是亚磷酸 。
。 易溶于水,它的结构式表示为
易溶于水,它的结构式表示为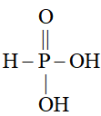 。
。 和
和 反应只生成
反应只生成 和
和 两种盐,其正盐溶液呈碱性。常温下,
两种盐,其正盐溶液呈碱性。常温下,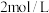 的亚磷酸溶液pH约为1。在
的亚磷酸溶液pH约为1。在 溶液中加入碘水振荡后,碘水的棕黄色褪去,再滴加溶液有黄
溶液中加入碘水振荡后,碘水的棕黄色褪去,再滴加溶液有黄 色沉淀析出。若在装有
色沉淀析出。若在装有 溶液的试管中加入
溶液的试管中加入 溶液,则析出黑色金属银沉淀,溶液中有无色气泡产生,在试管口变为红棕色。回答下列问题:
溶液,则析出黑色金属银沉淀,溶液中有无色气泡产生,在试管口变为红棕色。回答下列问题:(1)
 为
为(2)用化学方程式表示
 和碘水的反应:
和碘水的反应: 水溶液呈碱性的原因(用离子方程式表示):
水溶液呈碱性的原因(用离子方程式表示):(3)根据上述事实,可以得知
 是
是A.强酸 B.弱酸 C.二元酸 D.三元酸 E.具有强氧化性 F.具有强还原性
21-22高二下·上海徐汇·期末 查看更多[2]
上海市上海中学2021-2022学年高二下学期期末阶段练习化学试题(已下线)专题06 酸碱中和与盐类水解及难溶电解质的沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)
更新时间:2023-06-12 21:06:35
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有下列七种物质: ①酒精 ②CaO ③烧碱 ④NaCl ⑤Cu ⑥SO2 ⑦苏打
(1)上述物质中属于盐的是_______ (填编号,下同),属于氧化物的是_______ ,属于溶于水成碱性的是_______ 。
(2)请对上述七种物质进行分类(填编号):属于电解质的是_______ , 属于非电解质的是_______ 。
(3)在氢氧化钠溶液中通入足量⑥的离子反应方程式为_______ 。
(4)某同学用⑤和浓硫酸共热来制备⑥,化学方程式为:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
①请用单线桥 标出电子转移的情况:_____
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
②上述反应的还原产物是_______ 。
(1)上述物质中属于盐的是
(2)请对上述七种物质进行分类(填编号):属于电解质的是
(3)在氢氧化钠溶液中通入足量⑥的离子反应方程式为
(4)某同学用⑤和浓硫酸共热来制备⑥,化学方程式为:Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O①请用
Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O②上述反应的还原产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】2021年在四川广汉三星堆新发现大量青铜器,如青铜面具、青铜神树等等。如图中的文物是三星堆出土的青铜面具之一,由于时间久远,表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、O2、CO2作用产生的,其化学式为Cu2(OH)2CO3,请用学过的方法对其展开探究。

(1)根据以上信息,可以获知的Cu2(OH)2CO3的物理性质有___________ 、___________ (选取其中两点)。
(2)从不同的物质分类标准的角度分析,“铜绿”不属于___________ 。
A.铜盐 B.碳酸盐 C.碱式盐 D.碱 E.含氧酸盐
(3)“铜绿”热稳定性差,受热易分解,请写出“铜绿”受热分解的化学方程式___________ 。
(4)以“铜绿”为反应物可以实现以下物质转化:
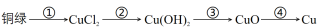
经观察反应①固体物质溶解,有气泡产生,请写出该反应的化学方程式___________ 。反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊。请写出反应④的化学方程式___________ 。

(1)根据以上信息,可以获知的Cu2(OH)2CO3的物理性质有
(2)从不同的物质分类标准的角度分析,“铜绿”不属于
A.铜盐 B.碳酸盐 C.碱式盐 D.碱 E.含氧酸盐
(3)“铜绿”热稳定性差,受热易分解,请写出“铜绿”受热分解的化学方程式
(4)以“铜绿”为反应物可以实现以下物质转化:
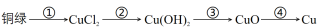
经观察反应①固体物质溶解,有气泡产生,请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 为黄棕色粉末,易溶于水,通常用作有机和无机反应催化剂、媒染剂、杀虫剂。回答下列问题:
为黄棕色粉末,易溶于水,通常用作有机和无机反应催化剂、媒染剂、杀虫剂。回答下列问题:
(1)按照物质的分类方法, 应属于
应属于___________ (填序号)。
①酸 ②氯化物 ③混合物 ④盐 ⑤化合物 ⑥电解质
(2) 可由金属铜和氯气化合制得,写出反应的化学方程式:
可由金属铜和氯气化合制得,写出反应的化学方程式:___________ ,其中作氧化剂的是___________ (填化学式)。
(3)孔雀石[主要成分为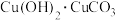 ]、蓝铜矿[主要成分为
]、蓝铜矿[主要成分为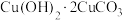 ]都是重要的矿物颜料。其中
]都是重要的矿物颜料。其中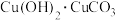 属于
属于___________ (填“纯净物”或“混合物”);请写出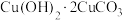 与盐酸反应的化学方程式:
与盐酸反应的化学方程式:___________ 。
(4)往氯化铜溶液中滴加氢氧化钠溶液时,可观察到的现象为________ ,写出反应的离子方程式:___________ 。
 为黄棕色粉末,易溶于水,通常用作有机和无机反应催化剂、媒染剂、杀虫剂。回答下列问题:
为黄棕色粉末,易溶于水,通常用作有机和无机反应催化剂、媒染剂、杀虫剂。回答下列问题:(1)按照物质的分类方法,
 应属于
应属于①酸 ②氯化物 ③混合物 ④盐 ⑤化合物 ⑥电解质
(2)
 可由金属铜和氯气化合制得,写出反应的化学方程式:
可由金属铜和氯气化合制得,写出反应的化学方程式:(3)孔雀石[主要成分为
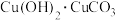 ]、蓝铜矿[主要成分为
]、蓝铜矿[主要成分为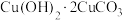 ]都是重要的矿物颜料。其中
]都是重要的矿物颜料。其中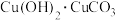 属于
属于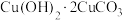 与盐酸反应的化学方程式:
与盐酸反应的化学方程式:(4)往氯化铜溶液中滴加氢氧化钠溶液时,可观察到的现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硫及其化合物在生产、生活中具有广泛的应用,根据所学知识,回答下列问题:
(1)室温下,在某NaHSO3、Na2SO3混合溶液中, 、
、 物质的量分数随pH的变化曲线如图所示,根据图示,
物质的量分数随pH的变化曲线如图所示,根据图示, 的水解平衡常数Kh=
的水解平衡常数Kh=_______

(2)室温下,某浓度的(NH4)2SO3溶液中:
①往(NH4)2SO3溶液中滴加少量的HClO溶液,发生反应的离子方程式为_______ 。
②此时所得溶液的pH_______ (“变大”、“变小”或“不变”)。
(3)亚磷酸(H3PO3)为二元弱酸,是重要的化工原料,可作尼龙增白剂、农药中间体等。25℃时,向一定体积的亚磷酸溶液中滴加等物质的量浓度的NaOH溶液,混合液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。
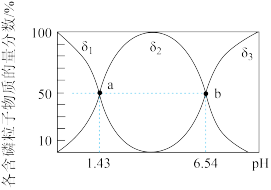
①NaH2PO3为_______ (填“正盐”或“酸式盐”),其溶液显_______ (填“酸性”、“中性”、“碱性”或“无法判断”)。
②写出NaH2PO3水解的离子方程式_______ ;
(4)现有浓度为0.02 mol/L的HCN与0.01 mol/LNaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是_______(填字母编号)。
(1)室温下,在某NaHSO3、Na2SO3混合溶液中,
 、
、 物质的量分数随pH的变化曲线如图所示,根据图示,
物质的量分数随pH的变化曲线如图所示,根据图示, 的水解平衡常数Kh=
的水解平衡常数Kh=
(2)室温下,某浓度的(NH4)2SO3溶液中:
①往(NH4)2SO3溶液中滴加少量的HClO溶液,发生反应的离子方程式为
②此时所得溶液的pH
(3)亚磷酸(H3PO3)为二元弱酸,是重要的化工原料,可作尼龙增白剂、农药中间体等。25℃时,向一定体积的亚磷酸溶液中滴加等物质的量浓度的NaOH溶液,混合液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。

①NaH2PO3为
②写出NaH2PO3水解的离子方程式
(4)现有浓度为0.02 mol/L的HCN与0.01 mol/LNaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是_______(填字母编号)。
| A.c(H+)>c(OH-) | B.c(H+)<c(OH-) |
| C.c(H+)+c(HCN)=c(OH-) | D.c(HCN)+c(CN-)=0.01 mol/L |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。根据所学知识回答下列问题:
(1) 是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为___________ (填化学式),标准状况下,每生成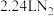 ,反应中转移的电子的物质的量为
,反应中转移的电子的物质的量为___________  。
。
(2)在一定条件下, 可与
可与 发生反应:
发生反应: ,在此过程中
,在此过程中 被
被___________ (填“氧化”或“还原”), 中
中 的化合价是
的化合价是___________ 价。
(3)某一反应体系有反应物和生成物共七种物质: 、
、 、
、 、
、 、
、 、
、 、
、 ,已知该反应中有气体生成。
,已知该反应中有气体生成。
①该反应中的还原剂是___________ (填化学式,下同),被还原的物质为___________ 。
②写出该反应的化学方程式:___________ 。
(1)
 是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为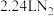 ,反应中转移的电子的物质的量为
,反应中转移的电子的物质的量为 。
。(2)在一定条件下,
 可与
可与 发生反应:
发生反应: ,在此过程中
,在此过程中 被
被 中
中 的化合价是
的化合价是(3)某一反应体系有反应物和生成物共七种物质:
 、
、 、
、 、
、 、
、 、
、 、
、 ,已知该反应中有气体生成。
,已知该反应中有气体生成。①该反应中的还原剂是
②写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1).2Na+2H2O=2NaOH+H2↑为氧化还原反应
氧化剂是_________ 还原剂是________
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮直至溶液呈____________ 色,即可制得Fe(OH)3胶体。
(3)Fe(OH)3胶体,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫________ ;胶体中加入电解质,胶体变得浑浊,这是发生了__________ 。
氧化剂是
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮直至溶液呈
(3)Fe(OH)3胶体,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在常温下,有下列五种溶液:A.0.1mol/LNH4Cl B.0.1mol/L CH3COONH4 C.0.1mol/LNH4HSO4 D.0.1mol/LNH4HCO3 E.0.1mol/LNaHCO3
请根据要求填写下列空白:
(1)溶液A呈___ 性(填“酸”、“碱”或“中”),其原因是:___ (用离子方程式表示)。
(2)溶液E呈___ 性(填“酸”、“碱”或“中”),其原因是:___ (用离子方程式表示)。
(3)比较溶液A、C中c(NH4+)的大小关系是A___ C(填“>”、“<”或“=”)。
(4)常温下,测得溶液B的pH= ,则CH3COO-的水解程度
,则CH3COO-的水解程度___ NH4+的水解程度(填“>”、“<”或“=”),CH3COO-与NH4+浓度的大小关系是:c(CH3COO-)___ c(NH4+)(填“>”、“<”或“=”)。
请根据要求填写下列空白:
(1)溶液A呈
(2)溶液E呈
(3)比较溶液A、C中c(NH4+)的大小关系是A
(4)常温下,测得溶液B的pH=
 ,则CH3COO-的水解程度
,则CH3COO-的水解程度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,向 溶液中逐滴加入
溶液中逐滴加入 的
的 溶液,图中所示曲线表示混合溶液的
溶液,图中所示曲线表示混合溶液的 变化情况(体积变化忽略不计)。回答下列问题:
变化情况(体积变化忽略不计)。回答下列问题:

(1)由图中信息可知 为强酸,理由是
为强酸,理由是_______ 。
(2)常温下一定浓度的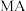 稀溶液的
稀溶液的 则a
则a_______ (填“>”“<”或“=”)7,此时,溶液中由水电离出的
_______ 。
(3)请写出K点所对应的溶液中离子浓度的大小关系:_______ 。
(4)K点对应的溶液中,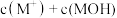
_______ (填“>”“<”或“=”) ;若此时溶液的
;若此时溶液的 ,则
,则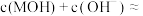
_______  。
。
 溶液中逐滴加入
溶液中逐滴加入 的
的 溶液,图中所示曲线表示混合溶液的
溶液,图中所示曲线表示混合溶液的 变化情况(体积变化忽略不计)。回答下列问题:
变化情况(体积变化忽略不计)。回答下列问题:
(1)由图中信息可知
 为强酸,理由是
为强酸,理由是(2)常温下一定浓度的
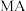 稀溶液的
稀溶液的 则a
则a
(3)请写出K点所对应的溶液中离子浓度的大小关系:
(4)K点对应的溶液中,
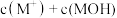
 ;若此时溶液的
;若此时溶液的 ,则
,则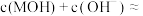
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】室温下,向20mL盐酸和硫酸的混合溶液中逐渐滴入0.05mol/L的 溶液,生成的
溶液,生成的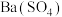 沉淀的质量和pH的变化如图所示(不考虑溶液混合时体积的变化)。
沉淀的质量和pH的变化如图所示(不考虑溶液混合时体积的变化)。
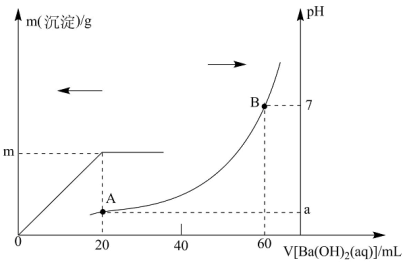
(1)原混合溶液中HCl的物质的量的浓度为___________ 。
(2)图中A点对应溶液的
___________ 。
(3)pH相等的NaOH溶液与 溶液,分别加热到相同的温度后,
溶液,分别加热到相同的温度后, 溶液的pH
溶液的pH___________ NaOH溶液的pH(填“>“=”或“<”)。
(4)将物质的量浓度相同的盐酸与氨水混合后,溶液中的 ,则盐酸的体积
,则盐酸的体积___________ 氨水的体积(填“>“=”或“<”)。
(5)将0.2mol/L HA溶液与0.1mol/L NaOH溶液等体积混合(混合后溶液体积变化忽略不计),测得混合溶液中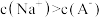 ,则:
,则:
①混合溶液中,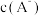
___________  (填“>”“=”或“<”,下同)。
(填“>”“=”或“<”,下同)。
②混合溶液中,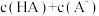
___________ 0.1mol/L。
(6)生活中常用明矾作净水剂,其原理是___________ (结合必要的离子方程式说明)。
(7)泡沫灭火器(硫酸铝和碳酸氢钠溶液)的作用原理是___________ (写出离子方程式)
(8)室温下,0.1mol/L的NaHA溶液中,测得溶液显碱性。则该溶液中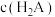
___________ 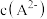 (填“>”<”或“=”)。
(填“>”<”或“=”)。
(9)①现有等物质的量浓度的下列五种溶液① 、②
、②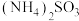 、③
、③ 、④
、④ 、⑤
、⑤ ,溶液中水的电离程度由大到小的排列顺序是
,溶液中水的电离程度由大到小的排列顺序是___________ (填序号)。
② 可以将碘盐中的
可以将碘盐中的 还原为碘单质,试写出此反应的离子方程式:
还原为碘单质,试写出此反应的离子方程式:___________ 。
 溶液,生成的
溶液,生成的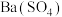 沉淀的质量和pH的变化如图所示(不考虑溶液混合时体积的变化)。
沉淀的质量和pH的变化如图所示(不考虑溶液混合时体积的变化)。
(1)原混合溶液中HCl的物质的量的浓度为
(2)图中A点对应溶液的

(3)pH相等的NaOH溶液与
 溶液,分别加热到相同的温度后,
溶液,分别加热到相同的温度后, 溶液的pH
溶液的pH(4)将物质的量浓度相同的盐酸与氨水混合后,溶液中的
 ,则盐酸的体积
,则盐酸的体积(5)将0.2mol/L HA溶液与0.1mol/L NaOH溶液等体积混合(混合后溶液体积变化忽略不计),测得混合溶液中
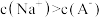 ,则:
,则:①混合溶液中,
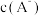
 (填“>”“=”或“<”,下同)。
(填“>”“=”或“<”,下同)。②混合溶液中,
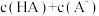
(6)生活中常用明矾作净水剂,其原理是
(7)泡沫灭火器(硫酸铝和碳酸氢钠溶液)的作用原理是
(8)室温下,0.1mol/L的NaHA溶液中,测得溶液显碱性。则该溶液中
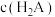
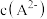 (填“>”<”或“=”)。
(填“>”<”或“=”)。(9)①现有等物质的量浓度的下列五种溶液①
 、②
、②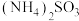 、③
、③ 、④
、④ 、⑤
、⑤ ,溶液中水的电离程度由大到小的排列顺序是
,溶液中水的电离程度由大到小的排列顺序是②
 可以将碘盐中的
可以将碘盐中的 还原为碘单质,试写出此反应的离子方程式:
还原为碘单质,试写出此反应的离子方程式:
您最近一年使用:0次


 MnCl2+2H2O+Cl2↑,请回答下列问题:
MnCl2+2H2O+Cl2↑,请回答下列问题:

