证明亚硫酸钠已经被氧化的实验方法___________
2023高三·全国·专题练习 查看更多[1]
(已下线)04 常考题空4 实验简答题的精准描述 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
更新时间:2023-04-13 11:34:54
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】纯碱是一种重要的工业原料,可用于生活洗涤、食品加工和工业制玻璃等,可用侯氏制碱法制备,其流程如下(部分物质已略去):
已知:通常状况下,1体积水大约溶解1体积 或700体积
或700体积 ;
; 溶于水后,溶液显碱性。
溶于水后,溶液显碱性。

(1)为除去食盐水中的 、
、 、
、 ,可先
,可先_______ (填选项字母),过滤后加适量盐酸,再蒸发浓缩得饱和溶液。
A.加NaOH溶液,后加 溶液,再加钡试剂溶液
溶液,再加钡试剂溶液
B.加NaOH溶液,后加钡试剂溶液,再加 溶液
溶液
C.加钡试剂溶液,后加NaOH溶液,再加 溶液
溶液
除去 时,该钡试剂最好为
时,该钡试剂最好为_______ 。
A. B.
B. C.
C.
(2)向饱和食盐水中先通入的气体为_______ ,分析其原因_______ 。
(3)过程①的实验操作为_______ 、洗涤、干燥,检验所得小苏打中不含 的方法为
的方法为_______ 。
(4)过程②的化学方程式为_______ 。
(5)该制备可得到的副产品为_______ 。
已知:通常状况下,1体积水大约溶解1体积
 或700体积
或700体积 ;
; 溶于水后,溶液显碱性。
溶于水后,溶液显碱性。
(1)为除去食盐水中的
 、
、 、
、 ,可先
,可先A.加NaOH溶液,后加
 溶液,再加钡试剂溶液
溶液,再加钡试剂溶液B.加NaOH溶液,后加钡试剂溶液,再加
 溶液
溶液C.加钡试剂溶液,后加NaOH溶液,再加
 溶液
溶液除去
 时,该钡试剂最好为
时,该钡试剂最好为A.
 B.
B. C.
C.
(2)向饱和食盐水中先通入的气体为
(3)过程①的实验操作为
 的方法为
的方法为(4)过程②的化学方程式为
(5)该制备可得到的副产品为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】非金属元素在化工生产中扮演着重要的角色。
(1)下列物质中,能吸收 的有
的有___________ (填字母序号)。
a.浓硫酸 b.酸性 溶液 c.生石灰
溶液 c.生石灰
(2)实验室用铜和浓硫酸加热制备二氧化硫,写出化学方程式___________ 。
(3)久置在空气中的 固体会部分变质,检验是否变质的方法是:取少量固体加水溶解,
固体会部分变质,检验是否变质的方法是:取少量固体加水溶解,___________ (将实验操作和现象补充完整)。
(4)工业上利用氨的催化氧化制取NO,写由化学方程式___________ 。
(1)下列物质中,能吸收
 的有
的有a.浓硫酸 b.酸性
 溶液 c.生石灰
溶液 c.生石灰(2)实验室用铜和浓硫酸加热制备二氧化硫,写出化学方程式
(3)久置在空气中的
 固体会部分变质,检验是否变质的方法是:取少量固体加水溶解,
固体会部分变质,检验是否变质的方法是:取少量固体加水溶解,(4)工业上利用氨的催化氧化制取NO,写由化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某研究性学习小组对二氧化硫的制备、性质以及含量测定进行探究。
Ⅰ.制备二氧化硫
用70%的浓硫酸与 固体反应制备
固体反应制备 气体。
气体。
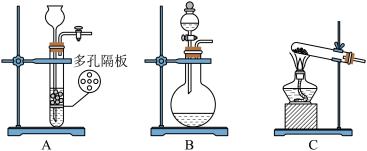
(1)制备 气体最合适的发生装置是
气体最合适的发生装置是___________ (填写字母),反应的化学方程式为___________ 。
Ⅱ.探究 的性质
的性质
在下图装置中先后三次加入相同浓度、相同体积、不同条件下的钡盐溶液,控制食用油油层厚度一致、打开开关K,通入 流速一致。三次实验现象如下表:
流速一致。三次实验现象如下表:

三次实验分别得到如下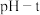 图:
图:
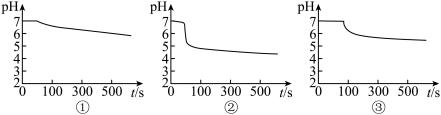
(2)A装置中覆盖食用油的目的是___________ 。
(3)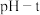 图中,曲线①呈缓慢下降趋势,这是因为
图中,曲线①呈缓慢下降趋势,这是因为___________ ;曲线②出现骤降,这是因为 与
与 溶液中溶解的
溶液中溶解的___________ 发生了氧化还原反应生成了 ;写出实验③中反应的离子方程式为
;写出实验③中反应的离子方程式为___________ 。
Ⅲ.测定空气中二氧化硫含量。
(4)将空气样品经过管道通入密闭容器中的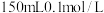 的酸性
的酸性 溶液,若管道中空气流量为
溶液,若管道中空气流量为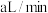 ,经过
,经过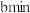 溶液恰好褪色,假设样品中的
溶液恰好褪色,假设样品中的 可被溶液充分吸收。则该空气样品中
可被溶液充分吸收。则该空气样品中 的含量为
的含量为___________  。
。
Ⅰ.制备二氧化硫
用70%的浓硫酸与
 固体反应制备
固体反应制备 气体。
气体。(1)制备
 气体最合适的发生装置是
气体最合适的发生装置是
Ⅱ.探究
 的性质
的性质在下图装置中先后三次加入相同浓度、相同体积、不同条件下的钡盐溶液,控制食用油油层厚度一致、打开开关K,通入
 流速一致。三次实验现象如下表:
流速一致。三次实验现象如下表:| ① | ② | ③ |
已煮沸的 溶液 溶液 | 未煮沸的 溶液 溶液 | 己煮沸的 溶液 溶液 |
| 无白色沉淀生成 | 有白色沉淀生成 | 有白色沉淀生成 |

三次实验分别得到如下
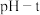 图:
图:
(2)A装置中覆盖食用油的目的是
(3)
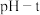 图中,曲线①呈缓慢下降趋势,这是因为
图中,曲线①呈缓慢下降趋势,这是因为 与
与 溶液中溶解的
溶液中溶解的 ;写出实验③中反应的离子方程式为
;写出实验③中反应的离子方程式为Ⅲ.测定空气中二氧化硫含量。
(4)将空气样品经过管道通入密闭容器中的
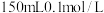 的酸性
的酸性 溶液,若管道中空气流量为
溶液,若管道中空气流量为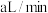 ,经过
,经过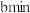 溶液恰好褪色,假设样品中的
溶液恰好褪色,假设样品中的 可被溶液充分吸收。则该空气样品中
可被溶液充分吸收。则该空气样品中 的含量为
的含量为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】菠菜营养丰富,素有“蔬菜之王”的美称。民间流传:菠菜豆腐同食,易得结石。某化学兴趣小组对“菠菜豆腐是否不能同食”等问题进行了探究。
【查阅资料】①菠菜含有丰富的铁、草酸盐、碳酸盐等,豆腐中含有丰富的蛋白质及钙盐。
②人体结石的主要成分:草酸钙(CaC2O4)
③醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐等。
【提出猜想】“菠菜豆腐不能同食”的原因可能是____________ 。
【探究一】菠菜中部分成分分析

(1)步骤③中判断加入的CaCl2溶液已足量的方法是___________ 。
(2)已知气体C能使澄清石灰水变浑浊,醋酸的化学式用HAc表示,写出步骤④的化学反应方程式________________ 。沉淀A、B的质量关系为:m(A)_________ m(B)(填“>”、“<”或“=”)。
(3)白色沉淀B的化学式为_________ ,由此可见菠菜豆腐不能同食。以下饮食观点正确的是__________ (填字母)
A.禁吃菠菜 B.高钙牛奶可与菠菜同食
C.菠菜烹饪时可用开水烫,可降低草酸盐含量
【探究二】某草酸钙晶体(CaC2O4·xH2O)热分解研究
(提示:CaC2O4·xH2O受热会失去结晶水成为CaC2O4 ;白色硫酸铜粉末遇水会变蓝。)
按下图装置将草酸钙晶体样品高温加热,使其完全分解,对所得气体产物进行探究(假设装置中各试剂均足量)
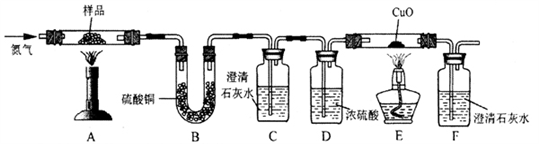
(4)①反应开始前通入氮气的目的是___________ ,装置C的作用是_______________ 。
②装置B中硫酸铜粉末变蓝,C、F中澄清石灰水均变浑浊,E中CuO变红,说明产物有__________________ ,经检验A中残留固体为氧化物。
③对上述装置从环保角度提一个改进建议_____________ 。
(5)某研究所利用SDT Q600热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,
获得相关数据,绘制成固体质量—分解温度的关系如图。

①800℃以上时,固体成分的化学式为_______ 。
②残留固体为CaC2O4时的温度范围__________ 。
③写出固体质量由12.8g变为10.0g时的化学方程式________________ 。
【查阅资料】①菠菜含有丰富的铁、草酸盐、碳酸盐等,豆腐中含有丰富的蛋白质及钙盐。
②人体结石的主要成分:草酸钙(CaC2O4)
③醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐等。
【提出猜想】“菠菜豆腐不能同食”的原因可能是
【探究一】菠菜中部分成分分析

(1)步骤③中判断加入的CaCl2溶液已足量的方法是
(2)已知气体C能使澄清石灰水变浑浊,醋酸的化学式用HAc表示,写出步骤④的化学反应方程式
(3)白色沉淀B的化学式为
A.禁吃菠菜 B.高钙牛奶可与菠菜同食
C.菠菜烹饪时可用开水烫,可降低草酸盐含量
【探究二】某草酸钙晶体(CaC2O4·xH2O)热分解研究
(提示:CaC2O4·xH2O受热会失去结晶水成为CaC2O4 ;白色硫酸铜粉末遇水会变蓝。)
按下图装置将草酸钙晶体样品高温加热,使其完全分解,对所得气体产物进行探究(假设装置中各试剂均足量)

(4)①反应开始前通入氮气的目的是
②装置B中硫酸铜粉末变蓝,C、F中澄清石灰水均变浑浊,E中CuO变红,说明产物有
③对上述装置从环保角度提一个改进建议
(5)某研究所利用SDT Q600热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,
获得相关数据,绘制成固体质量—分解温度的关系如图。

①800℃以上时,固体成分的化学式为
②残留固体为CaC2O4时的温度范围
③写出固体质量由12.8g变为10.0g时的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】“鱼浮灵”又称固态双氧水,主要成分为2Na2CO3·3H2O2,是水产品运输过程中常用的化学增氧剂。某小组为探究溶液酸碱性对H2O2溶液中溶解氧含量的影响,进行了如下实验。
[查阅资料]
i.Na2SO4 溶液显中性。
ii.pH<7时, pH越小,溶液的酸性越强; pH>7时,pH越大,溶液的碱性越强。
[进行实验]
向3个均盛有80 mL 4% H2O2溶液的烧杯中,依次加入20 mL的稀硫酸、Na2SO4 溶液、NaOH溶液,分别测定溶液的pH和溶解氧含量。实验记录如下表。
[分析解释]
(1)H2O2发生分解反应的产物是___________ 。
(2)由实验②可知,H2O2 溶液显___________ ( 填字母)。
a.酸性 b.碱性
(3)综合上述实验数据,可以得出的结论是____________ 。
[应用实践]
(4)结合上述实验分析,“鱼浮灵”可以提高水中溶解氧含量的可能原因有___________ 。
[查阅资料]
i.Na2SO4 溶液显中性。
ii.pH<7时, pH越小,溶液的酸性越强; pH>7时,pH越大,溶液的碱性越强。
[进行实验]
向3个均盛有80 mL 4% H2O2溶液的烧杯中,依次加入20 mL的稀硫酸、Na2SO4 溶液、NaOH溶液,分别测定溶液的pH和溶解氧含量。实验记录如下表。
| 实验编号 | ① | ② | ③ |
| 加入的试剂 | 稀硫酸 | Na2SO4溶液 | NaOH溶液 |
| pH | 0.44 | 5.97 | 11.74 |
| 溶解氧含量/ (mg·L-1) | 5.9 | 6.5 | 13.1 |
[分析解释]
(1)H2O2发生分解反应的产物是
(2)由实验②可知,H2O2 溶液显
a.酸性 b.碱性
(3)综合上述实验数据,可以得出的结论是
[应用实践]
(4)结合上述实验分析,“鱼浮灵”可以提高水中溶解氧含量的可能原因有
您最近一年使用:0次

 、
、 的
的 固体提纯,并制得纯净的
固体提纯,并制得纯净的


