已知:SO2+I2+2H2O=SO +2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:
+2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:
(1)所用碘水溶液的物质的量浓度_____ mol/L。
(2)空气样品中SO2的含量_____ mg/L。
(3)若空气中SO2的浓度不超过0.02mg/L为合格,则上述空气质量_____ (填“合格”或“不合格”)。
 +2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:
+2I—+4H+。现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:(1)所用碘水溶液的物质的量浓度
(2)空气样品中SO2的含量
(3)若空气中SO2的浓度不超过0.02mg/L为合格,则上述空气质量
22-23高一下·浙江·期中 查看更多[2]
更新时间:2023-05-16 11:38:05
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】实验室中经常需配制一定浓度的NaOH溶液,现将22.0g NaOH固体溶于水配成100.0mL溶液,其密度为1.2g.mL﹣1.
(1)该溶液中NaOH的质量分数约为 .
(2)从该溶液中取出10.0mL,其中NaOH的物质的量浓度为 ,含NaOH的物质的量为 .
(3)将取出的10.0mL溶液加水稀释到100.0mL,稀释后溶液中NaOH的物质的量浓度为 .
(1)该溶液中NaOH的质量分数约为 .
(2)从该溶液中取出10.0mL,其中NaOH的物质的量浓度为 ,含NaOH的物质的量为 .
(3)将取出的10.0mL溶液加水稀释到100.0mL,稀释后溶液中NaOH的物质的量浓度为 .
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将16.1g氯化铵固体与足量熟石灰混合加热,使之充分反应,能制得氨气_______ 升(标准状况)?将此气体通入100mL氯化铝溶液,恰好将溶液中的Al3+完全沉淀,求氯化铝溶液的物质的量浓度_________ 。(要有计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】在15℃下将氨气通入一盛水的玻璃球内,至氨气不再溶解为止。经称量得知玻璃球内的饱和溶液质量为3.400g,然后将玻璃球浸入体积为50.00mL浓度为0.5000mol/L的硫酸溶液中,将球击破。充分反应后溶液中剩余的酸还能与10.00mL 1.000mol/L的NaOH溶液恰好完全反应生成正盐。该氨水中的溶质全部以NH3计,则:
(1)饱和溶液中NH3的物质的量为____________________ 。
(2)饱和溶液中NH3的质量分数为__________ 。
(3)测得所得饱和氨水的密度为0.918g/cm3,则饱和溶液中NH3的物质的量浓度为__________ 。
(1)饱和溶液中NH3的物质的量为
(2)饱和溶液中NH3的质量分数为
(3)测得所得饱和氨水的密度为0.918g/cm3,则饱和溶液中NH3的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在标准状况下,取甲、乙、丙各100mL相同浓度的盐酸,然后分别慢慢加入组成相同的镁、铝合金粉末,得到的气体体积与合金的质量有关数据如表(设产生气体全部逸出):
请回答:
(1)反应产生的气体是_______ ;在甲组实验中,盐酸_______ (选填“适量”、“过量”或“不足量”,下同);丙组实验中盐酸_______ 。
(2)盐酸的物质的量浓度为_______ mol/L。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 2.55 | 3.85 | 4.59 |
| 气体体积/L | 2.80 | 3.36 | 3.36 |
请回答:
(1)反应产生的气体是
(2)盐酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
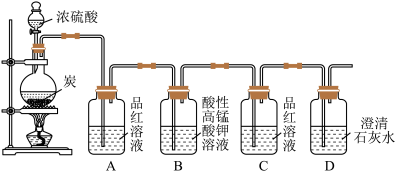
【推荐1】某同学欲验证碳与浓硫酸反应产物的性质。现已将装置如图连接,请回答下列问题。
(1)烧瓶中发生反应的化学反应方程式是___________ 。
(2)实验中两次使用到品红溶液,其目的不同。A的使用目的是_____ ,通过洗气瓶C中无现象和___ 的现象,证明反应有_______ (填化学式)生成。
(3)洗气瓶B中溶液颜色变浅,说明碳与浓硫酸反应的产物之一______ (填名称)具有______ 的性质。
(4)实验完成后,取出洗气瓶A中的无色溶液于试管中,加热,可观察到__________ 。
(1)烧瓶中发生反应的化学反应方程式是
(2)实验中两次使用到品红溶液,其目的不同。A的使用目的是
(3)洗气瓶B中溶液颜色变浅,说明碳与浓硫酸反应的产物之一
(4)实验完成后,取出洗气瓶A中的无色溶液于试管中,加热,可观察到
您最近一年使用:0次



