实验室中经常需配制一定浓度的NaOH溶液,现将22.0g NaOH固体溶于水配成100.0mL溶液,其密度为1.2g.mL﹣1.
(1)该溶液中NaOH的质量分数约为 .
(2)从该溶液中取出10.0mL,其中NaOH的物质的量浓度为 ,含NaOH的物质的量为 .
(3)将取出的10.0mL溶液加水稀释到100.0mL,稀释后溶液中NaOH的物质的量浓度为 .
(1)该溶液中NaOH的质量分数约为 .
(2)从该溶液中取出10.0mL,其中NaOH的物质的量浓度为 ,含NaOH的物质的量为 .
(3)将取出的10.0mL溶液加水稀释到100.0mL,稀释后溶液中NaOH的物质的量浓度为 .
更新时间:2016-03-08 10:36:38
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】按要求进行计算,直接写出结果
(1)标准状况下,2.24 L CH4所含氢原子的物质的量为____ mol。
(2)含0.2 mol氧原子的NO2的质量是____ g。
(3)100 mL 0.5mol· L-1 H2SO4溶液中,H+的物质的量浓度为____ mol· L-1。
(4)1mol碳在一定量氧气中反应,生成气体的质量为36 g。所得气体的物质的量为____ mol。
(1)标准状况下,2.24 L CH4所含氢原子的物质的量为
(2)含0.2 mol氧原子的NO2的质量是
(3)100 mL 0.5mol· L-1 H2SO4溶液中,H+的物质的量浓度为
(4)1mol碳在一定量氧气中反应,生成气体的质量为36 g。所得气体的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】将24.4gNaOH固体溶于水配成100mL溶液,其密度为1.219g/mL。
(1)该溶液中NaOH的物质的量浓度为__ 。
(2)该溶液中NaOH的质量分数为___ 。
(3)从该溶液中取出10mL,其中NaOH的物质的量浓度为___ 。
(1)该溶液中NaOH的物质的量浓度为
(2)该溶液中NaOH的质量分数为
(3)从该溶液中取出10mL,其中NaOH的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】按要求完成。
(1)19.6克硫酸是___________ molH2SO4,含有___________ 个原子,1.7克NH3在同温同压下与___________ 克H2S气体含有的氢原子数相同。
(2)标准状况下,密度为0.75g/L的NH3与CH4组成的混合气体中,NH3的体积分数___________ ,混合气体的平均摩尔质量为___________ 该气体对氢气的相对密度为___________ 。
(3)已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是___________ (其中阿伏加德罗常数用NA表示)。
(4)将MgCl2·xH2O的晶体4.06g溶于水配成100mL溶液,取出50mL溶液正好与0.02moL的AgNO3溶液完全作用,4.06g的MgCl2·xH2O物质的量为___________ 式中x的数值___________ 。
(5)配制100mL1mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为___________ mL。
(6)现要配制1mol·L-1Na2CO3溶液250mL
①需要含结晶水的碳酸钠晶体(Na2CO3·10H2O)___________ g;
②在配制上述溶液的过程中,可能导致配制溶液浓度偏小的有___________
A.固体Na2CO3·10H2O放在右盘(1g以下用游码);
B.容量瓶用碳酸钠溶液先润洗;
C.转移溶液时未洗涤烧杯
D.定容时溶液未冷却;
E.定容时视线仰视;
F.摇匀时,发现液面低于容量瓶刻度线,但未补加水;
G.容量瓶未干燥。
(1)19.6克硫酸是
(2)标准状况下,密度为0.75g/L的NH3与CH4组成的混合气体中,NH3的体积分数
(3)已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是
(4)将MgCl2·xH2O的晶体4.06g溶于水配成100mL溶液,取出50mL溶液正好与0.02moL的AgNO3溶液完全作用,4.06g的MgCl2·xH2O物质的量为
(5)配制100mL1mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为
(6)现要配制1mol·L-1Na2CO3溶液250mL
①需要含结晶水的碳酸钠晶体(Na2CO3·10H2O)
②在配制上述溶液的过程中,可能导致配制溶液浓度偏小的有
A.固体Na2CO3·10H2O放在右盘(1g以下用游码);
B.容量瓶用碳酸钠溶液先润洗;
C.转移溶液时未洗涤烧杯
D.定容时溶液未冷却;
E.定容时视线仰视;
F.摇匀时,发现液面低于容量瓶刻度线,但未补加水;
G.容量瓶未干燥。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的量是一个联系宏观和微观的重要物理量。请回答下列有关问题。
(1)同温同压下,A2气体与B2气体化合,生成AxBy气体,已知反应前后气体的密度不变,则AxBy的分子式为___________ 。
(2)已知 的电子数为a,M的质量数为A,则2 mol的M的中子数为
的电子数为a,M的质量数为A,则2 mol的M的中子数为___________ 。
(3)质量之比为16∶7∶6的三种气体SO2、CO、NO。分子个数之比为___________ ;氧原子个数之比为___________ ;相同条件下的体积之比为___________ 。
(4)稀硫酸与铝恰好完全反应,所得V mL Al2(SO4)3溶液中含有m g Al3+,则该溶液中 物质的量浓度为
物质的量浓度为___________ mol·L-1。
(5)标准状况下,将体积比为9∶1∶4的H2、Cl2、O2在密闭容器中用电火花点燃充分反应,恢复到原状态后,形成溶液的质量分数为___________ 。(保留三位小数)
(1)同温同压下,A2气体与B2气体化合,生成AxBy气体,已知反应前后气体的密度不变,则AxBy的分子式为
(2)已知
 的电子数为a,M的质量数为A,则2 mol的M的中子数为
的电子数为a,M的质量数为A,则2 mol的M的中子数为(3)质量之比为16∶7∶6的三种气体SO2、CO、NO。分子个数之比为
(4)稀硫酸与铝恰好完全反应,所得V mL Al2(SO4)3溶液中含有m g Al3+,则该溶液中
 物质的量浓度为
物质的量浓度为(5)标准状况下,将体积比为9∶1∶4的H2、Cl2、O2在密闭容器中用电火花点燃充分反应,恢复到原状态后,形成溶液的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】硫酸常用于金属表面除锈。(原理:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O)
(1)把50g质量分数为98%的浓硫酸,稀释成10%的稀硫酸,需要水的质量是多少____ ?
(2)要使16gFe2O3恰好完全反应,需消耗上述10%的稀硫酸的质量是多少_____ ?
(1)把50g质量分数为98%的浓硫酸,稀释成10%的稀硫酸,需要水的质量是多少
(2)要使16gFe2O3恰好完全反应,需消耗上述10%的稀硫酸的质量是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)①在质量分数为28%,密度为1.2g/mL的KOH水溶液中,OH-与H2O数目之比是________ ,KOH的物质的量浓度为___________ 。
②“质量摩尔浓度”是用溶液中溶质的物质的量除以溶剂的质量,称为该溶质的质量摩尔浓度。则该KOH溶液的质量摩尔浓度为________ mol/kg(小数点后保留两位有效数字)
③若用该溶液与质量分数为12%的KOH溶液等体积混合,所得混合液的质量分数________ 20%(填“大于”“小于”或“等于”)
(2)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1:4:8。
①配制该营养液后c(NH4+)=0.016mol/L,溶液中c(K+)=_______________ 。
②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为________ 。
②“质量摩尔浓度”是用溶液中溶质的物质的量除以溶剂的质量,称为该溶质的质量摩尔浓度。则该KOH溶液的质量摩尔浓度为
③若用该溶液与质量分数为12%的KOH溶液等体积混合,所得混合液的质量分数
(2)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1:4:8。
①配制该营养液后c(NH4+)=0.016mol/L,溶液中c(K+)=
②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)用20gNaOH配成250mL溶液,它的物质的量浓度为___ ;取出5mL该溶液,它的物质的量浓度为___ ,再加水稀释至100mL,则稀释后溶液的物质的量浓度为___ ,其中含NaOH的质量为___ 。
(2)现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。
①该混合气体的平均摩尔质量为___ 。
②混合气体中碳原子的个数为___ (用NA表示阿伏加 德罗常数)。
(2)现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。
①该混合气体的平均摩尔质量为
②混合气体中碳原子的个数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】完成以下填空。
(1)有下列物质:①石墨②硫酸③ ④
④ ⑤熔融
⑤熔融 ⑥
⑥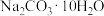 ⑦氨气⑧生石灰⑨食盐水⑩
⑦氨气⑧生石灰⑨食盐水⑩ ,以上物质中属于电解质的是:
,以上物质中属于电解质的是:_______ ;属于非电解质的是:______ (均填序号)。
(2)标准状况下,和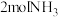 含有相同氢原子数的
含有相同氢原子数的 的体积为
的体积为_________ 。
(3)从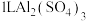 溶液中取出
溶液中取出 ,向其中加入
,向其中加入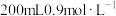 的
的 溶液恰好使
溶液恰好使 完全沉淀,则原溶液中
完全沉淀,则原溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
(4)用质量分数为 ,密度为
,密度为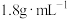 浓硫酸配制
浓硫酸配制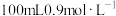 的稀硫酸,需用量筒量取浓硫酸的体积为
的稀硫酸,需用量筒量取浓硫酸的体积为___________  。
。
(1)有下列物质:①石墨②硫酸③
 ④
④ ⑤熔融
⑤熔融 ⑥
⑥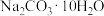 ⑦氨气⑧生石灰⑨食盐水⑩
⑦氨气⑧生石灰⑨食盐水⑩ ,以上物质中属于电解质的是:
,以上物质中属于电解质的是:(2)标准状况下,和
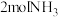 含有相同氢原子数的
含有相同氢原子数的 的体积为
的体积为(3)从
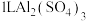 溶液中取出
溶液中取出 ,向其中加入
,向其中加入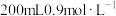 的
的 溶液恰好使
溶液恰好使 完全沉淀,则原溶液中
完全沉淀,则原溶液中 的物质的量浓度为
的物质的量浓度为 。
。(4)用质量分数为
 ,密度为
,密度为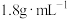 浓硫酸配制
浓硫酸配制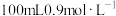 的稀硫酸,需用量筒量取浓硫酸的体积为
的稀硫酸,需用量筒量取浓硫酸的体积为 。
。
您最近一年使用:0次




