按要求回答下列问题。
(1)写出漂白粉有效成分的化学式___________ 。
(2)某元素的一种核素可用于文物的年代测定,写出该元素在周期表中的位置___________ 。
(3)写出稀盐酸与石灰石反应的离子方程式___________ 。
(4)写出红热的铁与水蒸气反应的化学方程式___________ 。
(1)写出漂白粉有效成分的化学式
(2)某元素的一种核素可用于文物的年代测定,写出该元素在周期表中的位置
(3)写出稀盐酸与石灰石反应的离子方程式
(4)写出红热的铁与水蒸气反应的化学方程式
更新时间:2023-04-22 20:10:54
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题:
(1)纯净物根据其组成和性质可进行如下分类:
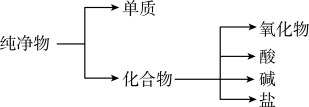
如图所示的分类方法属于___________ (填序号)
A.交叉分类法 B.树状分类法
(2)下列2组物质中均有一种物质的类别与其它2种不同
A.CaO、Na2O、SiO2 B.HClO、HNO3、CH3COOH
以上两组物质中,每组里与别的物质不同的物质依次是(填化学式)________ 、_________ 。
(3)写出下列反应的离子方程式:
①Cu(OH)2与盐酸反应___________
②NH4Fe(SO4)2与足量NaOH反应___________
③向足量澄清石灰水中通入少量二氧化碳___________ 。
(1)纯净物根据其组成和性质可进行如下分类:

如图所示的分类方法属于
A.交叉分类法 B.树状分类法
(2)下列2组物质中均有一种物质的类别与其它2种不同
A.CaO、Na2O、SiO2 B.HClO、HNO3、CH3COOH
以上两组物质中,每组里与别的物质不同的物质依次是(填化学式)
(3)写出下列反应的离子方程式:
①Cu(OH)2与盐酸反应
②NH4Fe(SO4)2与足量NaOH反应
③向足量澄清石灰水中通入少量二氧化碳
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学与生活、生产息息相关。请回答下列问题:
(1)以下为中学化学中常见的几种物质:①二氧化碳;②熔融KCl;③NaHSO4固体;④铜;⑤H2SO4溶液;⑥澄清石灰水,其中属于电解质的有______ (填序号,下同),属于非电解质的有______ 。
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。用小苏打片治疗胃酸过多的离子方程式为____________ 。
(3)工业上制备漂白粉常将氯气通入冷的石灰乳中,发生反应的化学方程式为_________ 。
(4)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,发生的化学反应如下:
①配平化学方程式:______ 。
______C+______K2Cr2O7+______H2SO4=______K2SO4+______CO2↑+______Cr2(SO4)3+______H2O。
②在上述反应中生成标准状况下的11.2LCO2,转移电子数为______ 。
③H2SO4在上述反应中表现出来的性质是______ (填选项编号)。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(1)以下为中学化学中常见的几种物质:①二氧化碳;②熔融KCl;③NaHSO4固体;④铜;⑤H2SO4溶液;⑥澄清石灰水,其中属于电解质的有
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。用小苏打片治疗胃酸过多的离子方程式为
(3)工业上制备漂白粉常将氯气通入冷的石灰乳中,发生反应的化学方程式为
(4)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,发生的化学反应如下:
①配平化学方程式:
______C+______K2Cr2O7+______H2SO4=______K2SO4+______CO2↑+______Cr2(SO4)3+______H2O。
②在上述反应中生成标准状况下的11.2LCO2,转移电子数为
③H2SO4在上述反应中表现出来的性质是
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】离子反应广泛用于化学研究、化工生产、医疗诊断和环境保护等各个领域。
(1) 是一种酸性氧化物。工业上,可用足量的稀氨水吸收少量
是一种酸性氧化物。工业上,可用足量的稀氨水吸收少量 ,写出发生反应的离子方程式:
,写出发生反应的离子方程式:___________ 。
(2) 具有较强的还原性,能使酸性高锰酸钾溶液褪色,反应中被还原的元素是
具有较强的还原性,能使酸性高锰酸钾溶液褪色,反应中被还原的元素是___________ (填元素符号)。
(3)某硫酸厂每天排放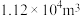 (标准状况)尾气,其中含0.2%(体积分数)的
(标准状况)尾气,其中含0.2%(体积分数)的 。现用浓度为
。现用浓度为 的NaOH废碱液(假设其他成分不参与反应)进行处理,每天至少需要这种废碱液的体积为
的NaOH废碱液(假设其他成分不参与反应)进行处理,每天至少需要这种废碱液的体积为___________ L。
(4)某同学向 溶液中通入
溶液中通入 ,未观察到有白色沉淀生成。取上述所得溶液进行下列操作,依然不能观察到有白色沉淀生成的是___________(填标号)。
,未观察到有白色沉淀生成。取上述所得溶液进行下列操作,依然不能观察到有白色沉淀生成的是___________(填标号)。
(5)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即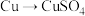
方案乙: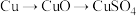
①方案甲中,铜和浓硫酸发生反应的化学方程式是___________ 。该反应体现了浓硫酸的___________ 。
②这两种方案,你认为哪一种方案更合理?___________ 。理由是___________ 。
(1)
 是一种酸性氧化物。工业上,可用足量的稀氨水吸收少量
是一种酸性氧化物。工业上,可用足量的稀氨水吸收少量 ,写出发生反应的离子方程式:
,写出发生反应的离子方程式:(2)
 具有较强的还原性,能使酸性高锰酸钾溶液褪色,反应中被还原的元素是
具有较强的还原性,能使酸性高锰酸钾溶液褪色,反应中被还原的元素是(3)某硫酸厂每天排放
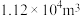 (标准状况)尾气,其中含0.2%(体积分数)的
(标准状况)尾气,其中含0.2%(体积分数)的 。现用浓度为
。现用浓度为 的NaOH废碱液(假设其他成分不参与反应)进行处理,每天至少需要这种废碱液的体积为
的NaOH废碱液(假设其他成分不参与反应)进行处理,每天至少需要这种废碱液的体积为(4)某同学向
 溶液中通入
溶液中通入 ,未观察到有白色沉淀生成。取上述所得溶液进行下列操作,依然不能观察到有白色沉淀生成的是___________(填标号)。
,未观察到有白色沉淀生成。取上述所得溶液进行下列操作,依然不能观察到有白色沉淀生成的是___________(填标号)。A.通入 | B.滴加稀硝酸 | C.滴加稀盐酸 | D.滴加NaOH溶液 |
方案甲:铜与浓硫酸加热直接反应,即
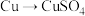
方案乙:
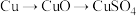
①方案甲中,铜和浓硫酸发生反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氯元素的单质及其化合物是生产和生活中非常重要的物质。回答下列问题:
(1) 是一种白色粉末,其化学名称为
是一种白色粉末,其化学名称为_______ ;漂白粉的主要成分是_______ (填化学式)。
(2)工业上利用 制取盐酸,其化学方程式为
制取盐酸,其化学方程式为_______ ; 溶于水可制得氯水,检验一瓶氯水是否已经完全变质,可选用的试剂是
溶于水可制得氯水,检验一瓶氯水是否已经完全变质,可选用的试剂是_______ (填字母)。
A.硝酸银溶液B.酚酞溶液C.碳酸钠溶液D.紫色石蕊溶液
(3)为了探究 、
、 、
、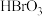 的氧化性强弱,进行如下实验:将
的氧化性强弱,进行如下实验:将 缓慢通入
缓慢通入 溶液至过量,溶液先变黄后变无色,且可检测到
溶液至过量,溶液先变黄后变无色,且可检测到 ;写出并配平该“变无色”反应的化学方程式
;写出并配平该“变无色”反应的化学方程式_______ ,若将 改为
改为 溶液,则溶液变为橙黄色,未检测到
溶液,则溶液变为橙黄色,未检测到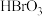 的存在;由上述事实推测,
的存在;由上述事实推测, 、
、 、
、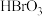 的氧化性由强到弱的次序是
的氧化性由强到弱的次序是_______ 。
(4)二氧化氯( )是国际上公认为安全、无毒的绿色消毒剂,在酸性条件下用
)是国际上公认为安全、无毒的绿色消毒剂,在酸性条件下用 还原
还原 (含少量
(含少量 )得到
)得到 。反应机理可分为以下四步:
。反应机理可分为以下四步:
①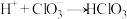
②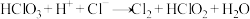
③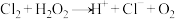
④_______ 。
请补充④的化学方程式。
(5) 对污水中
对污水中 有明显的去除效果。某工厂污水中含
有明显的去除效果。某工厂污水中含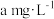 的
的 ,现用
,现用 将
将 氧化,生成了两种无毒无害的气体,处理
氧化,生成了两种无毒无害的气体,处理 这种污水,至少需要
这种污水,至少需要_______ 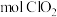 (用分数表示即可)。
(用分数表示即可)。
(1)
 是一种白色粉末,其化学名称为
是一种白色粉末,其化学名称为(2)工业上利用
 制取盐酸,其化学方程式为
制取盐酸,其化学方程式为 溶于水可制得氯水,检验一瓶氯水是否已经完全变质,可选用的试剂是
溶于水可制得氯水,检验一瓶氯水是否已经完全变质,可选用的试剂是A.硝酸银溶液B.酚酞溶液C.碳酸钠溶液D.紫色石蕊溶液
(3)为了探究
 、
、 、
、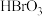 的氧化性强弱,进行如下实验:将
的氧化性强弱,进行如下实验:将 缓慢通入
缓慢通入 溶液至过量,溶液先变黄后变无色,且可检测到
溶液至过量,溶液先变黄后变无色,且可检测到 ;写出并配平该“变无色”反应的化学方程式
;写出并配平该“变无色”反应的化学方程式 改为
改为 溶液,则溶液变为橙黄色,未检测到
溶液,则溶液变为橙黄色,未检测到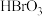 的存在;由上述事实推测,
的存在;由上述事实推测, 、
、 、
、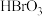 的氧化性由强到弱的次序是
的氧化性由强到弱的次序是(4)二氧化氯(
 )是国际上公认为安全、无毒的绿色消毒剂,在酸性条件下用
)是国际上公认为安全、无毒的绿色消毒剂,在酸性条件下用 还原
还原 (含少量
(含少量 )得到
)得到 。反应机理可分为以下四步:
。反应机理可分为以下四步:①
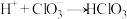
②
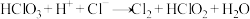
③
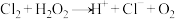
④
请补充④的化学方程式。
(5)
 对污水中
对污水中 有明显的去除效果。某工厂污水中含
有明显的去除效果。某工厂污水中含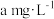 的
的 ,现用
,现用 将
将 氧化,生成了两种无毒无害的气体,处理
氧化,生成了两种无毒无害的气体,处理 这种污水,至少需要
这种污水,至少需要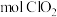 (用分数表示即可)。
(用分数表示即可)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】以化合价为纵坐标,物质类别为横坐标的图像称为“价—类”二维图。如图是氯元素的部分“价—类”二维图。

回答下列问题:
(1)Cl2呈________ 色,工业上干燥的Cl2贮存在________ 中。
(2)Y的化学式为________ 。已知反应:2ClO2+2NaOH=NaClO2+NaClO3+H2O,则ClO2________ (填“是”或“不是”)酸性氧化物。
(3)Cl2转化成T和HCl的离子方程式为________ 。
(4)实验室制备Cl2的化学方程式为________ 。
(5)除去Cl2中的HCl和水蒸气杂质,依次通过的试剂是________ 、________ 。
(6)已知酸性强弱:H2CO3>HClO>HCO 。向一定量的漂白液中通入少量CO2气体,发生反应的离子方程式为
。向一定量的漂白液中通入少量CO2气体,发生反应的离子方程式为________ 。

回答下列问题:
(1)Cl2呈
(2)Y的化学式为
(3)Cl2转化成T和HCl的离子方程式为
(4)实验室制备Cl2的化学方程式为
(5)除去Cl2中的HCl和水蒸气杂质,依次通过的试剂是
(6)已知酸性强弱:H2CO3>HClO>HCO
 。向一定量的漂白液中通入少量CO2气体,发生反应的离子方程式为
。向一定量的漂白液中通入少量CO2气体,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】钠及其化合物在化工生产中有着极其重要的应用,以氯化钠为原料可制备一系列物质。
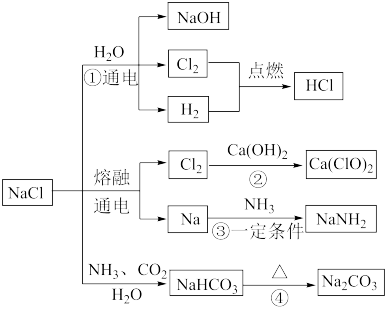
(1)反应①的离子方程式为_______ 。
(2)反应②的化学方程式为_______ ,漂白粉在空气中久置易变质的原因是_______ (用文字表述)。
(3)氨基钠(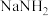 )是生产维生素A的原料。
)是生产维生素A的原料。
①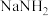 中氮元素的化合价为
中氮元素的化合价为_______ 。
②在一定条件下, 与
与 发生置换反应制得
发生置换反应制得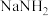 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(4)①证明反应④所得 中可能含有未分解的
中可能含有未分解的 的方法是
的方法是_______ 。
②将反应④所得a g固体与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b g固体,则a g固体中 的百分含量为
的百分含量为_______ (列出表达式,不要求计算结果)。若在蒸干过程中有少量液体溅出,则测得的 的百分含量
的百分含量_______ (填“偏高”“偏低”或“无影响”)。

(1)反应①的离子方程式为
(2)反应②的化学方程式为
(3)氨基钠(
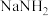 )是生产维生素A的原料。
)是生产维生素A的原料。①
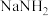 中氮元素的化合价为
中氮元素的化合价为②在一定条件下,
 与
与 发生置换反应制得
发生置换反应制得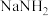 ,该反应的化学方程式为
,该反应的化学方程式为(4)①证明反应④所得
 中可能含有未分解的
中可能含有未分解的 的方法是
的方法是②将反应④所得a g固体与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b g固体,则a g固体中
 的百分含量为
的百分含量为 的百分含量
的百分含量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】写出下来化学方程式:
(1)铝和氢氧化钠溶液反应______
(2)铁在高温下与水反应______
(3) 制取氢氧化铝______
(4) 实验室氨气的制备______
(5)实验室制备氯气______
(1)铝和氢氧化钠溶液反应
(2)铁在高温下与水反应
(3) 制取氢氧化铝
(4) 实验室氨气的制备
(5)实验室制备氯气
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:___________ ;
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:___________ ;
(3)制漂白粉原理:___________ ;
(4)高温下Fe与水蒸气反应:___________ 。
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:___________ ;
(6)Al粉与NaOH溶液反应:___________ ;
(7)酸性条件下,向含铬废水中加FeSO4,将 还原为Cr3+:
还原为Cr3+:___________ ;
(8)制Fe(OH)3胶体:___________ 。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:
(3)制漂白粉原理:
(4)高温下Fe与水蒸气反应:
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:
(6)Al粉与NaOH溶液反应:
(7)酸性条件下,向含铬废水中加FeSO4,将
 还原为Cr3+:
还原为Cr3+:(8)制Fe(OH)3胶体:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表列出了A-R9种元素在周期表中的位置
(1)这9种元素中化学性质最不活泼的是_______ (填元素符号)
(2)D元素的最高价氧化物对应水化物与氢氧化钠反应的离子方程式是____________
(3)A、B、C三种元素按原子半径由大到小的顺序排列为______ (填元素符号)
(4)F元素氢化物的化学式是_____ ,该氢化物在常温下跟B发生反应的化学方程式是_______ ,所得溶液的pH____ 7。
(5)H元素跟A元素形成化合物的化学式___ ,高温灼烧该化合物时,火焰呈____ 色。
(6)G元素和H元素两者核电荷数之差是______ 。
| 周期\族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(1)这9种元素中化学性质最不活泼的是
(2)D元素的最高价氧化物对应水化物与氢氧化钠反应的离子方程式是
(3)A、B、C三种元素按原子半径由大到小的顺序排列为
(4)F元素氢化物的化学式是
(5)H元素跟A元素形成化合物的化学式
(6)G元素和H元素两者核电荷数之差是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,阅读表格回答问题:
(1)元素③的原子序数为___________ ,被选做相对原子质量标准的核素是___________ (填核素符号);
(2)①与②、③、④、⑦、⑧形成的化合物中,最稳定的是___________ (填化学式);表中所示元素最高价氧化物对应的水化物中酸性最强的是___________ (填化学式);
(3)请画出元素④与⑤按原子个数比1︰1组成的淡黄色固体物质的化学式___________ ;
(4)请写出⑤的最高价氧化物对应水化物与⑥的单质反应的离子方程式___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素③的原子序数为
(2)①与②、③、④、⑦、⑧形成的化合物中,最稳定的是
(3)请画出元素④与⑤按原子个数比1︰1组成的淡黄色固体物质的化学式
(4)请写出⑤的最高价氧化物对应水化物与⑥的单质反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表为长式周期表的一部分,其中的编号代表对应的元素。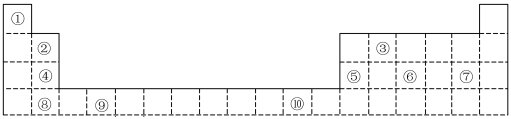
请回答下列问题:
(1)表中属于d区元素的是________ (填元素符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为____ ;③和⑦形成的一种常见溶剂的化学式为_____ 。
(3)元素④的第一电离能________ 元素⑤(选填“>”、“=”或“<”)的第一电离能;元素⑥的电负性________ 元素⑦(选填“>”、“=”或“<”)的电负性。
(4)元素⑦和⑧形成的化合物的电子式为________________ 。
(5)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:________ 。

请回答下列问题:
(1)表中属于d区元素的是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)元素④的第一电离能
(4)元素⑦和⑧形成的化合物的电子式为
(5)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次



