现有下列9种物质:① ②淀粉液 ③
②淀粉液 ③ ④
④ ⑤
⑤ ⑥Al ⑦纯醋酸 ⑧NaOH溶液 ⑨
⑥Al ⑦纯醋酸 ⑧NaOH溶液 ⑨ ⑩
⑩ ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:
(1)以上物质属于电解质的是______ (填写序号)。
(2)标准状况下,若④和⑤混合气体相对于氢气的密度为14.5,则④和⑤物质的量之比为______ 。标准状况下,VL  溶入100mL
溶入100mL  (1g/mL)中,溶液密度为
(1g/mL)中,溶液密度为 g/mL,则氨水物质的量浓度表达式为
g/mL,则氨水物质的量浓度表达式为______ mol/L。
(3)物质⑥对应的氧化物为______ (填“酸”、“碱”或“两性”)性氧化物,其与⑧反应的化学方程式为______ 。
(4)根据世界环保联盟的要求,⑩将逐渐取代 成为水的消毒剂。工业上常用
成为水的消毒剂。工业上常用 和
和 溶液混合并加入稀
溶液混合并加入稀 酸化后制得
酸化后制得 ,反应的离子方程式为:
,反应的离子方程式为:______ 。
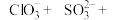 ______
______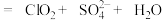 。
。
 ②淀粉液 ③
②淀粉液 ③ ④
④ ⑤
⑤ ⑥Al ⑦纯醋酸 ⑧NaOH溶液 ⑨
⑥Al ⑦纯醋酸 ⑧NaOH溶液 ⑨ ⑩
⑩ ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:(1)以上物质属于电解质的是
(2)标准状况下,若④和⑤混合气体相对于氢气的密度为14.5,则④和⑤物质的量之比为
 溶入100mL
溶入100mL  (1g/mL)中,溶液密度为
(1g/mL)中,溶液密度为 g/mL,则氨水物质的量浓度表达式为
g/mL,则氨水物质的量浓度表达式为(3)物质⑥对应的氧化物为
(4)根据世界环保联盟的要求,⑩将逐渐取代
 成为水的消毒剂。工业上常用
成为水的消毒剂。工业上常用 和
和 溶液混合并加入稀
溶液混合并加入稀 酸化后制得
酸化后制得 ,反应的离子方程式为:
,反应的离子方程式为: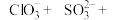 ______
______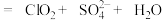 。
。
更新时间:2023-05-09 09:10:38
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】标准状况下336 L的NH3溶于1 L水中,所得溶液的质量分数为______ ,若该溶液的密度为a g/cm3,则物质的量浓度为______ 。将上述氨水全部转化为NH4Cl,所需4 mol·L-1的盐酸的体积为______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】“84消毒液”能有效杀灭甲型 病毒,某同学购买了一瓶“威露士”牌“84消毒液”,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:
病毒,某同学购买了一瓶“威露士”牌“84消毒液”,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:
(1)该“84消毒液”的物质的量浓度约为_________________ 。
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=_________________ mol·L-1。
(3)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.8 g·cm-3)的浓硫酸配制100 mL物质的量浓度为0.8 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①需要用量筒量取_________________ mL上述浓硫酸进行配制。
②稀释后的稀硫酸溶液中c(H+)为_________________ 。
 病毒,某同学购买了一瓶“威露士”牌“84消毒液”,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:
病毒,某同学购买了一瓶“威露士”牌“84消毒液”,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:| 84消毒液 有效成分NaClO 规格1 000 mL 质量分数25% 密度1.19 g·cm-3 |
(1)该“84消毒液”的物质的量浓度约为
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=
(3)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.8 g·cm-3)的浓硫酸配制100 mL物质的量浓度为0.8 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①需要用量筒量取
②稀释后的稀硫酸溶液中c(H+)为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】按要求填空
现有下列8种物质:①金刚石;②盐酸;③无水乙醇;④铜;⑤氨气;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧硫酸钡固体。
(1)属于电解质的是:_______ (填序号);
(2)属于非电解质的是:_______ (填序号);
(3)其中能导电的是:_______ (填序号);
(4)⑥在水溶液中的电离方程式为_______ 。
(5)上述8种物质中有两种物质之间可发生离子反应:H++OH-= H2O,该离子反应对应的化学方程式为_______ 。
现有下列8种物质:①金刚石;②盐酸;③无水乙醇;④铜;⑤氨气;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧硫酸钡固体。
(1)属于电解质的是:
(2)属于非电解质的是:
(3)其中能导电的是:
(4)⑥在水溶液中的电离方程式为
(5)上述8种物质中有两种物质之间可发生离子反应:H++OH-= H2O,该离子反应对应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】现有下列物质:①NaCl固体②HCl气体③ 固体④熔融KCl⑤铜⑥稀硫酸⑦CaO⑧
固体④熔融KCl⑤铜⑥稀硫酸⑦CaO⑧ ⑨氨水。
⑨氨水。
(1)上述物质中,属于电解质的是__________ (填序号)。
(2)写出②的水溶液和少量③反应的离子方程式:__________ .
 固体④熔融KCl⑤铜⑥稀硫酸⑦CaO⑧
固体④熔融KCl⑤铜⑥稀硫酸⑦CaO⑧ ⑨氨水。
⑨氨水。(1)上述物质中,属于电解质的是
(2)写出②的水溶液和少量③反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】现有 9 种物质:①NaCl 晶体;②CH3CH2OH(酒精);③ H2SO4 溶液;④铜丝;⑤盐酸;⑥熔融氯化钾;⑦SO2 气体;⑧液态氯化氢 ⑨Cl2回答下列问题:
(1)能够导电的是___________ ;
(2)溶于水能导电,但不是电解质的是___________ ;
(3)只有溶于水才能导电的电解质是___________ ;
(4)虽能导电,但不是电解质的是___________ ;
(5)虽不能导电,但也是电解质的是___________ 。
(1)能够导电的是
(2)溶于水能导电,但不是电解质的是
(3)只有溶于水才能导电的电解质是
(4)虽能导电,但不是电解质的是
(5)虽不能导电,但也是电解质的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】氧化还原反应在工业生产、环保及科研中有广泛的应用。氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50 ℃时反应可生成它。CuH具有的性质有:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体,Cu+在酸性条件下发生的反应是2Cu+=Cu2++Cu。
(1)写出CuH在氯气中燃烧的化学反应方程式:_______ 。
(2)CuH溶解在稀盐酸中反应的离子化学方程式是_______ 。
(3)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:_______ 。
(1)写出CuH在氯气中燃烧的化学反应方程式:
(2)CuH溶解在稀盐酸中反应的离子化学方程式是
(3)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
您最近一年使用:0次
【推荐2】高锰酸钾(KMnO4)是一种常用的氧化剂。
(1)有下列变化:CO32-→CO2、C2O42-→CO2、Fe3+→Fe2+,找出其中一个变化与“MnO4-→Mn2+”组成一个反应,写出该反应配平后的离子方程式_______ 。
(2)不同条件下高锰酸钾可发生不同如下反应: MnO4-+5e+8H+→Mn2++4H2O MnO4-+3e+2H2O→MnO2+4OH- MnO4-+e→MnO42-
由此可知,高锰酸根离子(MnO4-)反应后的产物与___ 有关。
(3)高锰酸钾可代替二氧化锰用来制取Cl2,反应中氧化剂和还原剂物质的量之比为________ 。
(4)高锰酸钾溶液与硫化亚铁在酸性条件下发生如下反应: 10FeS + 6KMnO4 + 24H2SO4 → 3K2SO4 + 6MnSO4 + 5Fe2(SO4)3 + 10S + 24H2O,若上述反应前后固体的质量减少了2.8g,则硫元素与KMnO4之间发生电子转移的数目为__ 。
(1)有下列变化:CO32-→CO2、C2O42-→CO2、Fe3+→Fe2+,找出其中一个变化与“MnO4-→Mn2+”组成一个反应,写出该反应配平后的离子方程式
(2)不同条件下高锰酸钾可发生不同如下反应: MnO4-+5e+8H+→Mn2++4H2O MnO4-+3e+2H2O→MnO2+4OH- MnO4-+e→MnO42-
由此可知,高锰酸根离子(MnO4-)反应后的产物与
(3)高锰酸钾可代替二氧化锰用来制取Cl2,反应中氧化剂和还原剂物质的量之比为
(4)高锰酸钾溶液与硫化亚铁在酸性条件下发生如下反应: 10FeS + 6KMnO4 + 24H2SO4 → 3K2SO4 + 6MnSO4 + 5Fe2(SO4)3 + 10S + 24H2O,若上述反应前后固体的质量减少了2.8g,则硫元素与KMnO4之间发生电子转移的数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】硫、氮、氯及其化合物在生产生活中应用广泛。请回答:
(1)将Cl2和SO2以1:1通入品红中,不能增强漂白性,用化学反应方程式解释原因________ 。
(2)NH3催化氧化制备NO是工业生产硝酸的基础,该反应的化学方程式为________ 。
(3)在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式为________ 。
(4)实验室可以用铜与稀硝酸反应制取NO,该反应的离子方程式为________ ,每生成2molNO,被还原的HNO3有________ mol。
(1)将Cl2和SO2以1:1通入品红中,不能增强漂白性,用化学反应方程式解释原因
(2)NH3催化氧化制备NO是工业生产硝酸的基础,该反应的化学方程式为
(3)在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式为
(4)实验室可以用铜与稀硝酸反应制取NO,该反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据你学过的有关金属的知识,回答下列问题(已知:铜、锌能与硝酸反应,而金不反应):
(1)铜钱在我国历史上曾经是一种广泛流通的货币,如图所示,铜常用于制造货币的原因可能是______________ (填字母)。

A.铜的熔点不是太高,易于冶炼,易于铸造成型
B.铜的性质不活没,不易被腐蚀
C.我国较早地掌握了湿法冶炼铜的技术
D.自然界有大量的游离态的铜
(2)铁制品的使用更为广泛,但是铁制品易生锈,铁锈的主要成分是________________________ (填化学式,下同),常见的铁的氧化物还有__________________ 、__________________ 。
(3)铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏,若使氧化铝与氢氧化钠溶液作用,反应的化学方程式为_____________________________________________ 。
(4)一位收藏者有一枚表面是黑色,且有少量绿色锈状物的货币,这肯定是_______________ 币,黑色物质是___________________ (填名称),形成这种物质的化学方程式为____________________ ,绿色物质是___________________ (填化学式),这枚金属币的真面目为________________ 色。另外一枚是闪闪发光的黄色金属币,它肯定是__________ 币,表面一直未被氧化的原因是________________________________________________________ 。
(1)铜钱在我国历史上曾经是一种广泛流通的货币,如图所示,铜常用于制造货币的原因可能是

A.铜的熔点不是太高,易于冶炼,易于铸造成型
B.铜的性质不活没,不易被腐蚀
C.我国较早地掌握了湿法冶炼铜的技术
D.自然界有大量的游离态的铜
(2)铁制品的使用更为广泛,但是铁制品易生锈,铁锈的主要成分是
(3)铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏,若使氧化铝与氢氧化钠溶液作用,反应的化学方程式为
(4)一位收藏者有一枚表面是黑色,且有少量绿色锈状物的货币,这肯定是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】世界因多样而精彩,求同是认识物质共性的分类思想,存异是尊重物质客观存在的包容思想。根据下列八种物质回答问题:① Cu ② S ③ CO2 ④ Al2O3 ⑤ Fe2O3 ⑥ Cu2(OH)2CO3 ⑦ 盐酸 ⑧ NaOH
(1)常温常压下,以上八种物质中,能导电的是______ (填写序号)。
(2)我国古代四大发明之一的黑火药是由一硫二硝三木炭的比例混合而成的,爆炸的反应为:S + 2KNO3 + 3C = K2S +______ ↑ + 3CO2↑ 请补齐化学方程式,硝酸钾作为反应的_____ 剂;32g硫粉充分反应,在标况下产生的CO2为______ L。
(3)Al2O3 和Fe2O3同为金属氧化物,均能溶于盐酸中,但Al2O3能溶于NaOH溶液中,而Fe2O3不能,试写出Al2O3与NaOH溶液反应的离子方程式________ 。
(4)铜生锈的产物为碱式碳酸铜Cu2(OH)2CO3,其属于_____ 类(填“酸”、“碱”或“盐”),铜在潮湿的空气中易生锈,试写出铜生锈的化学方程式___________ 。
(1)常温常压下,以上八种物质中,能导电的是
(2)我国古代四大发明之一的黑火药是由一硫二硝三木炭的比例混合而成的,爆炸的反应为:S + 2KNO3 + 3C = K2S +
(3)Al2O3 和Fe2O3同为金属氧化物,均能溶于盐酸中,但Al2O3能溶于NaOH溶液中,而Fe2O3不能,试写出Al2O3与NaOH溶液反应的离子方程式
(4)铜生锈的产物为碱式碳酸铜Cu2(OH)2CO3,其属于
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】钠、铝、铁是三种重要的金属。请回答下列问题:
(1)钠元素的金属活动性比铝的___________ (填“强”或“弱”)。
(2)将一小块金属钠投入水中,发生反应的离子方程式为___________ 。
(3)实验室中可用适量烧碱溶液除去 中的少量
中的少量 ,写出反应的化学方程式:
,写出反应的化学方程式:___________ 。
(4) 溶液一直作为传统的铜电路板蚀刻液。
溶液一直作为传统的铜电路板蚀刻液。
①蚀刻过程中的离子方程式为___________ 。
②蚀刻结束后,可以通过两步先分离出铜,再实现 溶液的再生。
溶液的再生。
ⅰ.分离铜时所加试剂和操作分别为___________ 。
ⅱ.为实现 溶液的再生可加入的物质是
溶液的再生可加入的物质是___________ (填一种即可)。
(1)钠元素的金属活动性比铝的
(2)将一小块金属钠投入水中,发生反应的离子方程式为
(3)实验室中可用适量烧碱溶液除去
 中的少量
中的少量 ,写出反应的化学方程式:
,写出反应的化学方程式:(4)
 溶液一直作为传统的铜电路板蚀刻液。
溶液一直作为传统的铜电路板蚀刻液。①蚀刻过程中的离子方程式为
②蚀刻结束后,可以通过两步先分离出铜,再实现
 溶液的再生。
溶液的再生。ⅰ.分离铜时所加试剂和操作分别为
ⅱ.为实现
 溶液的再生可加入的物质是
溶液的再生可加入的物质是
您最近一年使用:0次



