I.能源是现代文明的原动力,化学电池在生产生活中有着广泛的应用。
(1)根据构成原电池的本质判断,下列反应可以设计成原电池的是_____ (填序号)。
Ⅱ.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
(2)放电时负极反应为_____ 。
(3)放电时正极附近溶液的碱性_____ (填“增强”或“减弱”或“不变”)。
(4)放电时每转移_____ mol电子,正极有1molK2FeO4被还原。
Ⅲ.回答下列问题:
(5)科学家研发出一种有利于“碳中和”的新电池系统,通过二氧化碳溶于水触发电化学反应,其工作原理如图所示(钠超离子导体只允许Na+通过)。系统工作时,下列有关说法中错误的是_____ 。
Ⅳ.中国科学技术大学开发了一种高性能的水系锰基锌电池。其工作原理如图所示,已知该装置工作一段时间后,K2SO4溶液的浓度增大。_____ 。
(7)a膜为_____ (填“阳离子”或“阴离子”,下同)交换膜,b膜为_____ 交换膜。
(1)根据构成原电池的本质判断,下列反应可以设计成原电池的是
| A.CaO(s)+H2O(l)=Ca(OH)2(aq) | B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) |
| C.2CO(g)+O2(g)=2CO2(g) | D.Fe(s)+2FeCl3(aq)=3FeCl2(aq) |
Ⅱ.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。(2)放电时负极反应为
(3)放电时正极附近溶液的碱性
(4)放电时每转移
Ⅲ.回答下列问题:
(5)科学家研发出一种有利于“碳中和”的新电池系统,通过二氧化碳溶于水触发电化学反应,其工作原理如图所示(钠超离子导体只允许Na+通过)。系统工作时,下列有关说法中错误的是
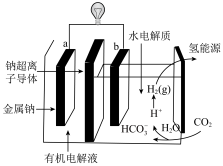
| A.Na+将从a极移动到b极 |
| B.该电池的电解液可以换成更易导电的饱和NaCl溶液 |
C.b极区可能会发生Na++HCO =NaHCO3↓ =NaHCO3↓ |
| D.b极区每生成1molH2转移2mol电子 |
Ⅳ.中国科学技术大学开发了一种高性能的水系锰基锌电池。其工作原理如图所示,已知该装置工作一段时间后,K2SO4溶液的浓度增大。

(7)a膜为
更新时间:2023-04-26 14:28:31
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
请回答:
(1)A极是电源的________ ,一段时间后,甲中溶液颜色__________ 。丁中X极附件的颜色逐渐变浅,Y极附件的颜色逐渐变深,这说明__________________ 。在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为__________ 。
(3)现用丙装置给铜件镀银,则G应该是________ (填“镀层金属”或“镀件”),电镀液是________ 溶液。当乙中溶液的c(OH-)=0.1mol· L-1(此时乙溶液体积为1000mL),丙中镀件上析出银的质量为________ ,甲中溶液的c(H+)pH________ (填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是_______________ 。

请回答:
(1)A极是电源的
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则G应该是
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有如下两个反应:(A)NaOH+HCl=NaCl+H2O
(B)2FeCl3+Cu=2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)
(A)___________________ (B)___________________
(2)如果(A或B)不能,说明其原因__________________________
(3)如果(A或B)可以,指出正、负极的电极材料,并写出电极反应式
负极:材料:_____ ;电极反应式:______________________________
正极:材料_______ ;电极反应式_______________________________ 。
(B)2FeCl3+Cu=2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)
(A)
(2)如果(A或B)不能,说明其原因
(3)如果(A或B)可以,指出正、负极的电极材料,并写出电极反应式
负极:材料:
正极:材料
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】利用反应Cu+2Ag+=2Ag+Cu2+设计一个化学电池。回答下列问题:
(1)该电池的负极材料是_______ ,发生_______ 反应(填“氧化”或“还原”);
(2)电解质溶液是_______ ;
(3)正极上出现的现象是_______ ;
(4)在外电路中,电子从_______ 极流向_______ 极。
(5)负极反应式:_______ ;正极反应式:_______ 。
(1)该电池的负极材料是
(2)电解质溶液是
(3)正极上出现的现象是
(4)在外电路中,电子从
(5)负极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.依据氧化还原反应: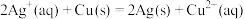 设计的原电池如下图所示,
设计的原电池如下图所示,
(1)电极X的材料是________ ;电解质溶液Y是________ ;
(2)银电极为原电池的_________ 极。(填“正”或“负”)
Ⅱ.如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:______ ,若初始时两电极质量相等,当电路中有0.2mole-通过时,两电极的质量差为______ g。
(4)当电极a为 ,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为
,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为______ ,对比(3)和(4),说明原电池中相对活泼的金属做正极还是负极,除了与金属本身的还原性有关外,还与______ 有关。
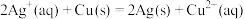 设计的原电池如下图所示,
设计的原电池如下图所示,
(1)电极X的材料是
(2)银电极为原电池的
Ⅱ.如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
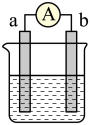
(4)当电极a为
 ,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为
,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有反应:①Ba(OH)2∙8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O②Fe+H2SO4=FeSO4+H2↑。试回答下列问题:
(1)两反应中属于吸热反应的是_______ (填序号,下同),能设计成原电池的是_______ 。
(2)Fe-Cu原电池的装置如图所示。
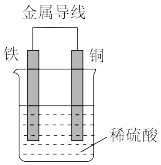
①铁作_______ (填“正极”或“负极”),溶液中H+向_______ (填“铁”或“铜”)电极方向移动。
②正极的现象是_______ ,负极的电极反应式为_______ 。
(1)两反应中属于吸热反应的是
(2)Fe-Cu原电池的装置如图所示。

①铁作
②正极的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电化学在生活中的应用广泛,请根据电化学原理回答下列问题:
(1)将锌片、铜片置于稀硫酸中并以导线连接起来组成原电池,可以获得电流,则Zn电极上发生的电极反应式为________ 。
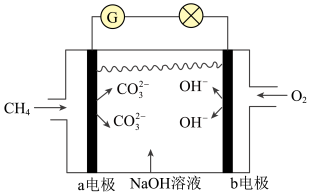
(2)如下图所示是甲烷燃料电池的原理示意图:
①电池的正极反应式为________ 。
②电池工作一段时间后,电解质溶液的pH________ (填“增大”、“减小”或“不变”)。
(3)按图所示装置,以石墨为电极电解氯化钠溶液,同时在两边各滴入几滴酚酞溶液,则电解时在X极附近观察到的现象是________ ,若将X电极材料换为Cu,则X电极上的电极反应式将________ (填“发生变化”或“不变”)。
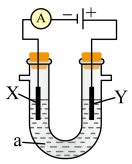
(4)某原电池装置初始状态如下图所示,电池总反应为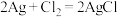 。
。
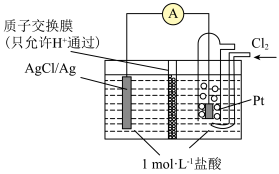
当电路中转移amol电子时,质子交换膜上通过________ mol离子,质子交换膜左侧的溶液中约减少________ mol离子(忽略溶液体积变化和 在水中的溶解)。
在水中的溶解)。
(1)将锌片、铜片置于稀硫酸中并以导线连接起来组成原电池,可以获得电流,则Zn电极上发生的电极反应式为
(2)如下图所示是甲烷燃料电池的原理示意图:
①电池的正极反应式为
②电池工作一段时间后,电解质溶液的pH

(3)按图所示装置,以石墨为电极电解氯化钠溶液,同时在两边各滴入几滴酚酞溶液,则电解时在X极附近观察到的现象是

(4)某原电池装置初始状态如下图所示,电池总反应为
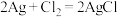 。
。
当电路中转移amol电子时,质子交换膜上通过
 在水中的溶解)。
在水中的溶解)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是某同学设计的一个简易的原电池装置,请回答下列问题。
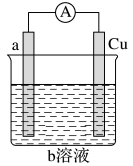
(1)若a电极材料为碳、b溶液为FeCl3溶液,则正极的电极反应式为___________________ ,当有3.2g的负极材料溶解时,导线中转移的电子的数目为________ 。
(2)氢氧燃料电池已用于航天飞机。这种电池以30%KOH溶液为电解质溶液,供电时总反应为2H2+O2===2H2O,则正极的电极反应式为_________________ ,该燃料电池的优点是_______________________ 。
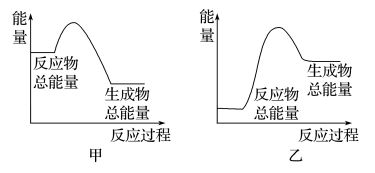
(3)已知H—H键、N—H键、N≡N键的键能分别为436kJ·mol-1、391kJ·mol-1、946kJ·mol-1,关于工业合成氨的反应,请根据键能的数据判断下列问题:
若有1molNH3生成,可________ (填“吸收”或“放出”)热量________ kJ;该反应的能量变化可用图______ (填“甲“或“乙”)表示。

(1)若a电极材料为碳、b溶液为FeCl3溶液,则正极的电极反应式为
(2)氢氧燃料电池已用于航天飞机。这种电池以30%KOH溶液为电解质溶液,供电时总反应为2H2+O2===2H2O,则正极的电极反应式为
(3)已知H—H键、N—H键、N≡N键的键能分别为436kJ·mol-1、391kJ·mol-1、946kJ·mol-1,关于工业合成氨的反应,请根据键能的数据判断下列问题:
若有1molNH3生成,可

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
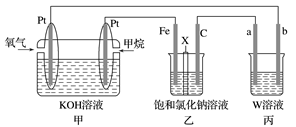
(1)石墨电极(C)作______ 极,甲中甲烷燃料电池的负极反应式为___________ 。
(2)若消耗2.24L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为_______ L。
(3)丙中以 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、An等杂质)的电解精炼。下列说法正确的是_______(填字母)。
溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、An等杂质)的电解精炼。下列说法正确的是_______(填字母)。
(4)若丙中以稀 为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为
为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为_________ 。
Ⅱ.依据氧化还原反应: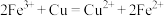 设计的原电池如图所示。请回答下列问题:
设计的原电池如图所示。请回答下列问题:

(5)电极X的材料是_______ (填化学式,下同);电解质Y是________ 。
(6)当X电极的质量减小了3.2g时,流经电流计的电子的物质的量为_______ mol。

(1)石墨电极(C)作
(2)若消耗2.24L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为
(3)丙中以
 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、An等杂质)的电解精炼。下列说法正确的是_______(填字母)。
溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、An等杂质)的电解精炼。下列说法正确的是_______(填字母)。| A.a电极为纯铜 | B.粗铜接电源正极,发生还原反应 |
C. 溶液的浓度保持不变 溶液的浓度保持不变 | D.利用阳极泥可回收Ag、Pt、Au等金属 |
 为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为
为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为Ⅱ.依据氧化还原反应:
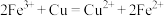 设计的原电池如图所示。请回答下列问题:
设计的原电池如图所示。请回答下列问题:
(5)电极X的材料是
(6)当X电极的质量减小了3.2g时,流经电流计的电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】I.一种利用电化学原理治污的装置如下图,其反应原理是6NO2+8NH3=7N2+12H2O
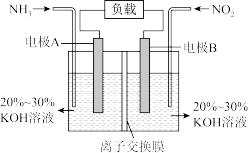
(1)A电极的电极反应式为___________ 。
(2)下列关于该电池说法正确的是___________(填序号)。
II.全钒液流电池(VFB)是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图为VFB放电工作原理。
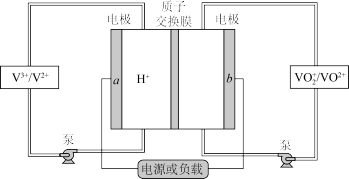
(3)电极b为___________ 极(填“正”或“负”)。充电时,该电极的反应为___________ 。
(4)若负载为如图2所示的装置,A、B、C、D均为石墨电极。
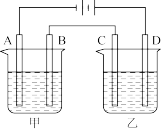
①甲槽是电极电解饱和食盐水的装置,产生40 g NaOH时,VFB电池中消耗___________ mol H+。
②乙槽为200 mLCuSO4溶液,当C电极析出0.64 g物质时,则乙槽中生成的H2SO4的物质的量为___________ mol。
③若通电一段时间后,向所得的乙槽溶液中加入0.2 mol的Cu(OH)2才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为___________ (用NA表示)
(5)锂离子电池的一种工作方式为Li+在电池两极的嵌入或迁出,以石墨做正极时,充电过程中,Li+在该石墨电极上___________ (填“嵌入”或“迁出”)。

(1)A电极的电极反应式为
(2)下列关于该电池说法正确的是___________(填序号)。
| A.电子从右侧电极经过负载后流向左侧电极 |
| B.为使电池持续放电,离子交换膜需选用阴离子交换膜 |
| C.电池工作一段时间,溶液的pH不变 |
| D.当有44.8 LNO2被处理时,转移电子的物质的量为8 mol |
II.全钒液流电池(VFB)是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图为VFB放电工作原理。

(3)电极b为
(4)若负载为如图2所示的装置,A、B、C、D均为石墨电极。

①甲槽是电极电解饱和食盐水的装置,产生40 g NaOH时,VFB电池中消耗
②乙槽为200 mLCuSO4溶液,当C电极析出0.64 g物质时,则乙槽中生成的H2SO4的物质的量为
③若通电一段时间后,向所得的乙槽溶液中加入0.2 mol的Cu(OH)2才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为
(5)锂离子电池的一种工作方式为Li+在电池两极的嵌入或迁出,以石墨做正极时,充电过程中,Li+在该石墨电极上
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】原电池原理广泛应用于科技、生产和生活中。
(1)一种处理垃圾渗透液并用其发电的装置工作示意图如下。

①在空气中,微生物将垃圾渗透液硝化,该反应的离子方程式为___________ 。
②Y电极的电极反应式为___________ 。
③盐桥中 移向
移向___________ (填“X或Y”)极;当转移0.15mol电子时,生成标准状况下 的体积为
的体积为___________ L。
(2)用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。
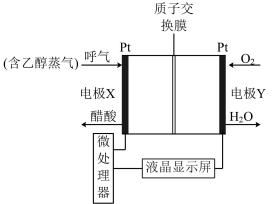
①电极X是该电池的___________ (填“正”或“负”)极,电池总反应式为___________ 。
②电池工作时,质子通过交换膜___________ (填“从左向右”或“从右向左”)迁移。
(1)一种处理垃圾渗透液并用其发电的装置工作示意图如下。

①在空气中,微生物将垃圾渗透液硝化,该反应的离子方程式为
②Y电极的电极反应式为
③盐桥中
 移向
移向 的体积为
的体积为(2)用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。

①电极X是该电池的
②电池工作时,质子通过交换膜
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氢气是未来最理想的能源。科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O=2H2↑+ O2↑,制得的氢气可用于制作燃料电池。试回答下列问题:
(1)分解海水时,实现了光能转化为____ 能。生成的氢气用于制作燃料电池时,实现了化学能转化为____ 能。分解海水的反应属于____ 反应(填“放热”或“吸热”)。
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为2H2+2O2--4e-=2H2O,则A极是电池的__ 极,B极电极反应式为__ 。
(1)分解海水时,实现了光能转化为
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为2H2+2O2--4e-=2H2O,则A极是电池的
您最近一年使用:0次




