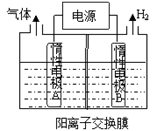
电化学在生活中的应用广泛,请根据电化学原理回答下列问题:
(1)将锌片、铜片置于稀硫酸中并以导线连接起来组成原电池,可以获得电流,则Zn电极上发生的电极反应式为________ 。
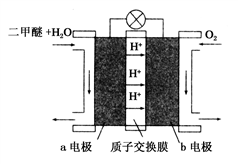
(2)如下图所示是甲烷燃料电池的原理示意图:
①电池的正极反应式为________ 。
②电池工作一段时间后,电解质溶液的pH________ (填“增大”、“减小”或“不变”)。
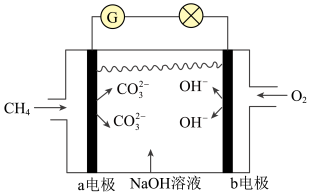
(3)按图所示装置,以石墨为电极电解氯化钠溶液,同时在两边各滴入几滴酚酞溶液,则电解时在X极附近观察到的现象是________ ,若将X电极材料换为Cu,则X电极上的电极反应式将________ (填“发生变化”或“不变”)。
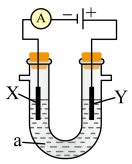
(4)某原电池装置初始状态如下图所示,电池总反应为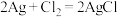 。
。
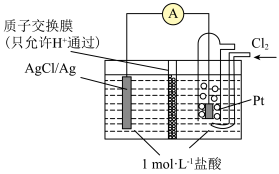
当电路中转移amol电子时,质子交换膜上通过________ mol离子,质子交换膜左侧的溶液中约减少________ mol离子(忽略溶液体积变化和 在水中的溶解)。
在水中的溶解)。
(1)将锌片、铜片置于稀硫酸中并以导线连接起来组成原电池,可以获得电流,则Zn电极上发生的电极反应式为
(2)如下图所示是甲烷燃料电池的原理示意图:
①电池的正极反应式为
②电池工作一段时间后,电解质溶液的pH

(3)按图所示装置,以石墨为电极电解氯化钠溶液,同时在两边各滴入几滴酚酞溶液,则电解时在X极附近观察到的现象是

(4)某原电池装置初始状态如下图所示,电池总反应为
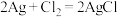 。
。
当电路中转移amol电子时,质子交换膜上通过
 在水中的溶解)。
在水中的溶解)。
更新时间:2023-12-17 21:01:07
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入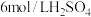 ,溶液中,乙同学将电极放入
,溶液中,乙同学将电极放入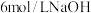 溶液中,如图:
溶液中,如图:

(1)原电池中的能量转化过程是将___________ 。
(2)甲中正极的电极反应式为___________ ,电子的流向是由___________ (填“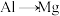 ”或“
”或“ ”)。
”)。
(3)乙中负极为___________ (填元素符号),该电池的总反应方程式为___________ 。
(4)如果甲同学和乙同学均认为:“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出___________ (填元素符号,下同)的金属活动性更强,而乙会判断出___________ 的金属活动性更强。
(5)由此实验得出的下列结论中,正确的是___________(填字母)。
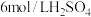 ,溶液中,乙同学将电极放入
,溶液中,乙同学将电极放入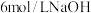 溶液中,如图:
溶液中,如图:
(1)原电池中的能量转化过程是将
(2)甲中正极的电极反应式为
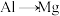 ”或“
”或“ ”)。
”)。(3)乙中负极为
(4)如果甲同学和乙同学均认为:“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出
(5)由此实验得出的下列结论中,正确的是___________(填字母)。
| A.镁的金属性不一定比铝的金属性强 |
| B.该实验说明金属活动性顺序已过时,已没有实用价值 |
| C.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析 |
| D.上述实验证明了“直接利用金属活动性顺序判断原电池中的正负极”这种做法不可靠 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】原电池是化学对人类的一项重大贡献。
(1)某兴趣小组为研究原电池原理,设计如图装置。

①a和b不连接时,烧杯中发生反应的离子方程式是_______ 。
②a和b用导线连接,Cu极为原电池_______ 极(填“正”或“负”),该电极反应式是_______ ,溶液中的H+移向_______ (填“Cu”或“Zn”)极。
③无论a和b是否连接,Zn片均被腐蚀,若转移了0.2 mol电子,则理论上Zn片质量减轻_______ g。
(2)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是_______ (填“a”或“b”)电极,该极的电极反应式为:_______ 。
②电池工作一段时间后电解质溶液的pH_______ (填“增大”“减小”或“不变”)。
(3)现有下列三个氧化还原反应:
A.2FeCl3+2KI=2FeCl2+2KCl+I2
B.2FeCl2+Cl2=2FeCl3
C.2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
Fe3+、I2、Cl2、MnO 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______
(1)某兴趣小组为研究原电池原理,设计如图装置。

①a和b不连接时,烧杯中发生反应的离子方程式是
②a和b用导线连接,Cu极为原电池
③无论a和b是否连接,Zn片均被腐蚀,若转移了0.2 mol电子,则理论上Zn片质量减轻
(2)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是
②电池工作一段时间后电解质溶液的pH
(3)现有下列三个氧化还原反应:
A.2FeCl3+2KI=2FeCl2+2KCl+I2
B.2FeCl2+Cl2=2FeCl3
C.2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
Fe3+、I2、Cl2、MnO
 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
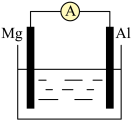
【推荐1】若烧杯中溶液为稀硫酸,两电极反应式为:正极______________________________ ;负极______________________________ ;

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示,组成一种原电池。试回答下列问题(灯泡功率合适):

(1)电解质溶液为稀硫酸时,灯泡亮,Mg电极上发生的反应为____________________ ;Al电极上发生的反应为_____________________________ 。溶液中 向
向_____ 移动(填“Mg电极”或“Al电极”)。当电路中转移0.5 mol电子时,理论上消耗负极材料的质量为___ g。
(2)电解质溶液为NaOH溶液时,灯泡________ (填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,Al电极上发生的反应为____________________________ 。
b.若灯泡不亮,其理由为________________________ 。

(1)电解质溶液为稀硫酸时,灯泡亮,Mg电极上发生的反应为
 向
向(2)电解质溶液为NaOH溶液时,灯泡
a.若灯泡亮,Al电极上发生的反应为
b.若灯泡不亮,其理由为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电化学应用广泛。请回答下列问题:
(1)自发进行的氧化还原反应可以设计成原电池。若电池放电时的反应式为:2FeCl3+Fe=3FeCl2,该电池的负极材料为__ ;正极的电极反应式为____ ;电解质溶液为_____ 。
(2)燃料电池和二次电池的应用非常广泛。

①如图为甲烷燃料电池的示意图,电池工作时,b极的电极为___ 极;负极的电极反应式为_________ ;
②铅蓄电池为生活中常用的二次电池。放电时的反应为:PbO2+Pb+2H2SO4=PbSO4+2H2O,铅蓄电池负极的电极反应式为_____ ;充电时,铅蓄电池的Pb极应与外加直流电源的__ 极相连,阳极的电极反应式为________ 。
(3)以铅蓄电池为电源精炼粗铜(含Fe、Pb、Ag、Au及其他不反应质)时,以硫酸铜溶液为电解质溶液,粗铜做___ 极;精炼一段时间后,当阴极增重128g时,铅蓄电池参加反应的硫酸的物质的量为_____ 。
(1)自发进行的氧化还原反应可以设计成原电池。若电池放电时的反应式为:2FeCl3+Fe=3FeCl2,该电池的负极材料为
(2)燃料电池和二次电池的应用非常广泛。

①如图为甲烷燃料电池的示意图,电池工作时,b极的电极为
②铅蓄电池为生活中常用的二次电池。放电时的反应为:PbO2+Pb+2H2SO4=PbSO4+2H2O,铅蓄电池负极的电极反应式为
(3)以铅蓄电池为电源精炼粗铜(含Fe、Pb、Ag、Au及其他不反应质)时,以硫酸铜溶液为电解质溶液,粗铜做
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】中国科学院长春应用化学研究所在甲醇(CH3OH)燃料电池方而获得新突破,研制出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示:

(1)该电池工作时,b处通入的物质为______________ ,c 通入 的物质为______ 。
(2)该电池负极的电极反应式为_________________ 。
(3)工作一段时间后,当12.8g甲醇完全反应生成 CO2时时,有_________ ×6.02×1023个电子发生转移。

(1)该电池工作时,b处通入的物质为
(2)该电池负极的电极反应式为
(3)工作一段时间后,当12.8g甲醇完全反应生成 CO2时时,有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】燃料电池是利用燃料与 反应从而将化学能转化为电能的装置。以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。(已知质子交换膜只允许
反应从而将化学能转化为电能的装置。以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。(已知质子交换膜只允许 通过)
通过)_______ (填“正”或“负”)极。
(2)正极反应式为_______ ,负极反应式为_______ 。
(3)放电过程中, 由
由_______ (填“正”或“负”,下同)极区向_______ 极区迁移。
(4)在电池反应中,每消耗1mol氧气,理论上能生成_______ L标准状况下 气体。
气体。
(5)该电池_______ (填“能”或“不能”)在高温下工作。
 反应从而将化学能转化为电能的装置。以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。(已知质子交换膜只允许
反应从而将化学能转化为电能的装置。以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。(已知质子交换膜只允许 通过)
通过)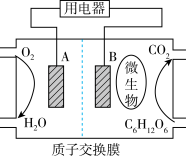
(2)正极反应式为
(3)放电过程中,
 由
由(4)在电池反应中,每消耗1mol氧气,理论上能生成
 气体。
气体。(5)该电池
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电化学的应用十分广泛,请分析下列几种电化学装置并回答问题:
Ⅰ.微生物燃料电池是废水处理中实现碳氮联合转化产生 和
和 的装置,如图所示,1、2为厌氧微生物电极,3为阳离子交换膜,4为好氧微生物反应器。请回答:
的装置,如图所示,1、2为厌氧微生物电极,3为阳离子交换膜,4为好氧微生物反应器。请回答:
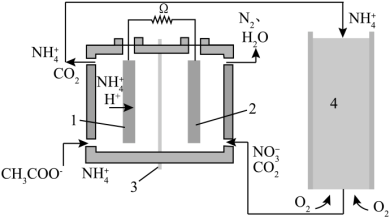
(1)电极1名称:_______ 极,电池工作一段时间后,电极2附近的pH_______ (填“增大”“减小”或“不变”)。
(2)电极1的电极反应式为_______ 。
(3)若好氧微生物反应器中消耗 (标准状况)
(标准状况) ,理论上电极2生成
,理论上电极2生成 物质的量为
物质的量为_______ mol。
Ⅱ.次磷酸钴(Ⅱ)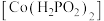 广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图。
广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图。
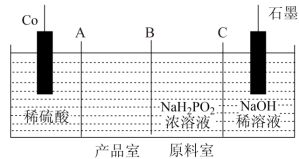
(4) A、B、C均为离子交换膜,其中为阳离子交换膜的是_______ 。
(5)石墨电极每生成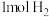 时,
时,_______ 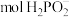 向
向_______ 迁移(填“阴极室”“阳极室”或“产品室”)。
(6)若以铅蓄电池为直流电源,则铅蓄电池中正极的电极反应式为_______ 。
Ⅰ.微生物燃料电池是废水处理中实现碳氮联合转化产生
 和
和 的装置,如图所示,1、2为厌氧微生物电极,3为阳离子交换膜,4为好氧微生物反应器。请回答:
的装置,如图所示,1、2为厌氧微生物电极,3为阳离子交换膜,4为好氧微生物反应器。请回答:
(1)电极1名称:
(2)电极1的电极反应式为
(3)若好氧微生物反应器中消耗
 (标准状况)
(标准状况) ,理论上电极2生成
,理论上电极2生成 物质的量为
物质的量为Ⅱ.次磷酸钴(Ⅱ)
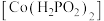 广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图。
广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图。
(4) A、B、C均为离子交换膜,其中为阳离子交换膜的是
(5)石墨电极每生成
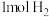 时,
时,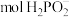 向
向(6)若以铅蓄电池为直流电源,则铅蓄电池中正极的电极反应式为
您最近一年使用:0次