Ⅰ.氢能是理想的能源之一。回答下列问题:
(1)利用太阳能催化光解水是制备
 的方法之一,其原理如图1所示,光解水中能量的转化形式为光能转化为
的方法之一,其原理如图1所示,光解水中能量的转化形式为光能转化为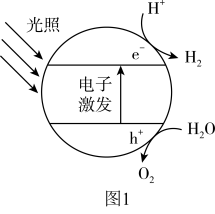
(2)在高温时,水蒸气与灼热的炭反应也能制得
 。该反应的能量变化如图2所示。
。该反应的能量变化如图2所示。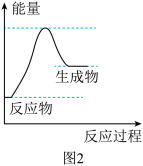
①该反应为
a.反应物的总能量高于产物的总能量
b.该反应过程中化学能全部转化为热能
c.该反应属于氧化还原反应
d.反应过程中,化学键的断裂与形成是化学反应中能量变化的主要原因
②
 、
、 、C都是常用的燃料。
、C都是常用的燃料。 、
、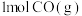 、
、 完全燃烧生成
完全燃烧生成 或
或 时,放出的热量分别为
时,放出的热量分别为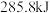 、
、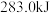 、
、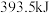 。相同质量的这三种燃料完全燃烧时放出的热量由大到小的顺序为
。相同质量的这三种燃料完全燃烧时放出的热量由大到小的顺序为Ⅱ.原电池是将化学能转化为电能的一种装置。
常温下,将除去表面氧化膜的铝片、铜片插入浓
 中组成原电池,装置如图甲所示,测得原电池的电流强度
中组成原电池,装置如图甲所示,测得原电池的电流强度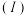 随时间
随时间 的变化如图乙所示,反应过程中有红棕色气体产生。后,外电路中电子的流动方向发生改变。
的变化如图乙所示,反应过程中有红棕色气体产生。后,外电路中电子的流动方向发生改变。
(3)
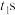 后,原电池的铜片是
后,原电池的铜片是 向
向相似题推荐
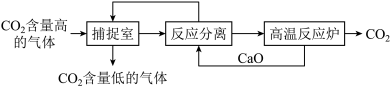
(1)下列有关该方法的叙述中正确的是
a.能耗大是该方法的一大缺点
b.整个过程中,只有一种物质可以循环利用
c.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤
d.该方法可减少碳排放,捕捉到的 CO2还可用来制备各种化工产品
(2)若所得溶液 pH=13,CO2 主要转化为
(3)CO2 与 CH4 经催化重整,制得合成气:CH4(g)+CO2(g)→2CO(g)+2H2(g)-120kJ,补全下图中 CO2 与 CH4 催化重整反应的能量变化示意图(即,注明生成物能量的大致位置及反应热效应数值)
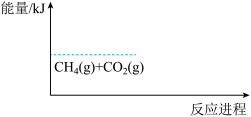
(4)常温下,在 2L 密闭容器中,下列能说明该反应达到平衡状态的是
a.每消耗 16gCH4 的同时生成 4gH2
b.容器中气体的压强不再改变
c.混和气体的平均相对分子质量不发生改变
d.容器中气体的密度不再改变
反应进行到 10 min 时,CO2 的质量减少了 8.8 g,则 0~10 min 内一氧化碳的反应速率是
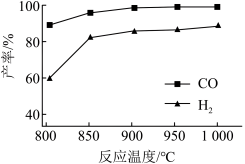
(5)按一定体积比加入 CH4 和 CO2,在恒压下发生反应,温度对 CO 和 H2 产率的影响如图所示。此反应优选温度为 900℃的原因是
 CO(g)+3H2(g)。
CO(g)+3H2(g)。(1)将1.0molCH4和2.0molH2O(g)通入该密闭容器中,10min时有0.1molCO生成,则10min内该反应的平均速率v(H2)=
(2)能说明该反应已达到平衡状态的是
a.容器内H2的物质的量保持不变
b.容器内各种气体共存
c.消耗1molCH4,同时生成1molCO
d.断裂2molH-O,同时断裂3molH-H
(3)已知该反应为吸热反应,则甲烷和水蒸气的总能量比一氧化碳和氢气的总能量
(4)电动汽车的某种燃料电池如图所示,其中一极通甲烷,一极通空气。则a极通的是
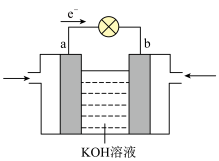
(1)已知:CH3OH(g) ===HCHO(g)+H2(g) ΔH=+84 kJ·mol-1
2H2(g)+O2(g) ===2H2O(g) ΔH=-484 kJ·mol-1
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)
 CH3OH(g),已知某些化学键的键能数据如下表:
CH3OH(g),已知某些化学键的键能数据如下表:| 化学键 | C—C | C—H | H—H | C—O | C≡O | O—H |
| 键能/ kJ·mol-1 | 348 | 413 | 436 | 358 | x | 463 |
请回答下列问题:
①该反应的ΔS

②已知CO中的C与O之间为三键,其键能为x kJ·mol-1,则x=
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池负极的电极反应式为
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
| 离子 | Cu2+ | H+ | Cl− | SO42 - |
| c/mol·L-1 | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为

(4)电解水蒸气和CO2产生合成气(H2+CO)。较高温度下(700~1 000 ℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2−,O2−穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2。由上图可知A为直流电源的
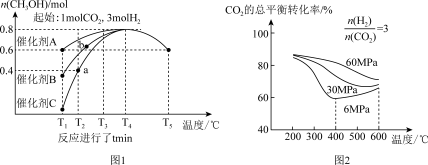
反应Ⅰ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)+Q1kJ(Q1>0),
反应Ⅱ:CO2(g)+H2(g) ⇌CO(g)+H2O(g)-Q2kJ(Q2>0)。
研究催化剂等外界条件对上述反应的影响,结果如图 1、图 2
完成下列填空:
(1)一定是碳12的同位素原子是
A.质子数为6,中子数为8 B.质子数为8,中子数为12
C.质子数为12,中子数为6 D.质子数为12,中子数为8
(2)分析图1:催化效果最佳的是催化剂
(3)分析图2:相同温度下,增大原料气压强,反应Ⅰ平衡常数
(4)若生成的CH3OH和CO物质的量之比为4:1,则消耗相同条件下的CO2和H2体积比是
(5)若有88gCO2发生反应Ⅰ,并放出akJ热量,则图3中A为
 的排放总量和减少总量相当,对于改善环境,实现绿色发展至关重要。
的排放总量和减少总量相当,对于改善环境,实现绿色发展至关重要。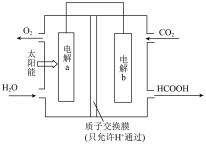
(1)将燃煤产生的
 回收再利用,可有效减少碳排放总量。以
回收再利用,可有效减少碳排放总量。以 和
和 为原料制备
为原料制备 和
和 的原电池装置如图所示。其中,电极a作
的原电池装置如图所示。其中,电极a作
 ;电池内部,
;电池内部, 的移动方向为
的移动方向为 ”或“
”或“ ”)。
”)。(2)以
 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为碳中和提供了一条新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应为碳中和提供了一条新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
①上述过程,能量变化形式主要由太阳能转化为
②根据上述信息可知,利用
 催化分解
催化分解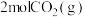 生成
生成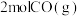 和
和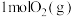 时需要
时需要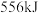 能量。
能量。(3)为发展低碳经济,科学家提出可以用氧化锆锌作催化剂,将
 转化为重要有机原料
转化为重要有机原料 ,该反应的化学方程式为
,该反应的化学方程式为 。在容积为
。在容积为 的恒温密闭容器中,充入
的恒温密闭容器中,充入 和
和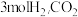 和
和 的物质的量随时间变化的曲线如图所示。分析图中数据,回答下列问题。
的物质的量随时间变化的曲线如图所示。分析图中数据,回答下列问题。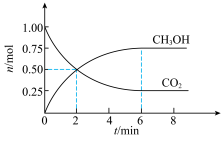
①反应在
 内,
内,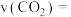
②
 时,反应是否达到化学平衡?
时,反应是否达到化学平衡? 时,正反应速率
时,正反应速率 时,将容器的容积变为
时,将容器的容积变为 ,此时化学反应速率
,此时化学反应速率③对于上述反应,下列叙述正确的是
a.当各气体的物质的量不再改变时,该反应已达平衡状态。
b.当该反应达到平衡后,
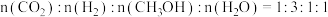 。
。c.由图可知,
 时
时 的生成速率大于
的生成速率大于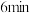 时
时 的分解速率。
的分解速率。d.提高反应的温度,可以实现
 的完全转化
的完全转化
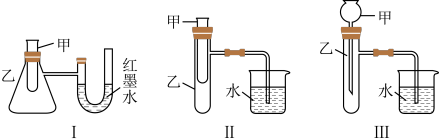
(1)上述装置中,不能证明“锌和稀硫酸反应是吸热反应还是放热反应”的是
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡晶体与氯化铵固体搅拌反应,U形管中可观察到的现象是
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。若观察到烧杯里产生气泡,则M可能是
(4)除了图示某些装置,还有其它方法能证明超氧化钾粉末与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是
 电极在原电池中的作用,设计并进行了以下一系列实验。已知:
电极在原电池中的作用,设计并进行了以下一系列实验。已知: 与
与 的化学性质基本相似,
的化学性质基本相似, 。回答下列问题:
。回答下列问题:(1)实验1:电极材料为
 和
和 ,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向
,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向 。
。①正极的电极反应式为
②每转移
 电子,此时负极材料减少的质量为
电子,此时负极材料减少的质量为(2)实验2:电极材料为
 和
和 ,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向
,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向 。
。由实验1和实验2可知,
 三种金属活动性由强到弱的顺序为
三种金属活动性由强到弱的顺序为(3)实验3:电极材料为石墨和
 ,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向石墨。
,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向石墨。①电池工作一段时间后,电解质溶液的
 将
将②石墨电极上发生
(4)实验4:电极材料为
 和
和 ,电解质溶液为氢氧化钠溶液,该电池工作时,电流表指针偏向
,电解质溶液为氢氧化钠溶液,该电池工作时,电流表指针偏向 。
。①负极的电极反应式为
②外电路中电子的流动方向为
 N2O4(g)的反应。恒温下,将一定量红棕色的NO2和无色N2O4(g)的混合气体充入容积固定的2L密闭容器中,其中各气体物质的量浓度随时间变化关系如图所示。
N2O4(g)的反应。恒温下,将一定量红棕色的NO2和无色N2O4(g)的混合气体充入容积固定的2L密闭容器中,其中各气体物质的量浓度随时间变化关系如图所示。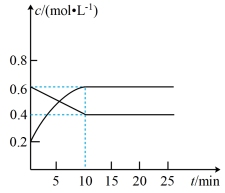
(1)由图可知开始时该反应的正逆反应速率大小为v(正)
(2)可作为判断上述可逆反应达到平衡状态的依据的是
A.2v(N2O4)=v(NO2) B.容器中压强不变 C.容器中气体的密度不变 D.容器中NO2的体积分数不变 E.容器内气体的颜色不变
(3)该条件下达到平衡状态时容器中气体压强是起始时压强的
Ⅱ.依据氧化还原反应:2Ag+(aq)+Cu(s)=2Ag(s)+Cu2+(aq)设计的原电池如下图所示。请回答下列问题:
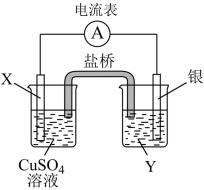
(4)电极X的材料是
(5)Y发生的电极反应为
(6)外电路中的电子是从
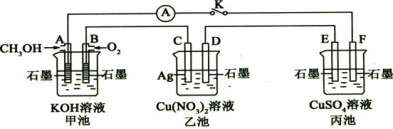
(1)甲池为
(2)丙池中E电极为
(4)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为
(5)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
【推荐1】甲醇是一种可再生能源,具有开发和应用的广阔前景,用Pt/Al2O3、Pd/C、Rh/SiO2作催化剂都可以采用如下反应来合成甲醇:2H2(g)+CO(g) CH3OH(g)
CH3OH(g)
(1)下表所列数据是各化学键的键能:
化学键 | H-H | C=O | C-H | C-O | O-H |
键能/(kJ●mol-1) | a | b | c | d | e |
则反应2H2(g)+CO(g) CH3OH(g)的△H=
CH3OH(g)的△H=
(2)三种不同催化剂作用时,CO的转化率如图1所示,则最适合作催化剂的是

(3)某化学研究性学习小组模拟工业合成甲醇的反应,在2 L的恒容密闭容器内充入2 mol H2和1molCO,加入合适催化剂后在某温度下开始反应,并用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
则从反应开始到20 min时,CO的平均反应速率为
(4)近日,美国Neah和Novellusnn公司宣布,两家公司合作开发了多孔硅甲醇直接燃料电池,其工作原理如图所示。

①石墨2为
②石墨1极发生的电极反应式为
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,写出CO2与NaOH溶液反应的主要化学方程式
(2)研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1= -53.7 kJ·mol-1Ⅰ
CH3OH(g)+H2O(g) ΔH1= -53.7 kJ·mol-1ⅠCO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2Ⅱ
CO(g)+H2O(g) ΔH2Ⅱ某实验室控制CO2和H2初始投料比为1∶2.2,经过相同反应时间测得如下实验数据:
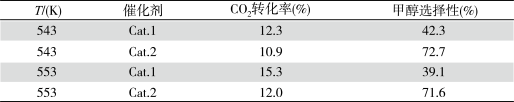
【备注】Cat.1∶Cu/ZnO纳米棒;Cat.2∶Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知: CO和H2的标准燃烧热分别为-283.0 kJ·mol-1和-285.8 kJ·mol-1;
H2O(l)= H2O(g) ΔH3 =+44.0 kJ·mol-1
请回答(不考虑温度对ΔH的影响):
①反应Ⅱ的ΔH2 =
②研究证实,CO2可在酸性水溶液中通过电解生成甲醇,则生成甲醇的电极反应式是
③表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是
(3)O2辅助的Al~CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。电池的负极反应式:
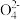 +6O2,反应过程中O2的作用是
+6O2,反应过程中O2的作用是
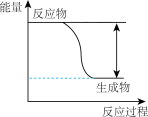
(1)该反应为
(2)若要使该反应的反应速率加快,下列措施可行的是
A.改铁片为铁粉 B.升高温度 C.减小压强 D.加入适量的Na2SO4固体
(3)若将上述反应设计成原电池,且铜为此原电池的某一电极材料,则铜为



