乳酸亚铁 常用作缺铁性贫血的补铁剂,能溶于水。
常用作缺铁性贫血的补铁剂,能溶于水。
(1)一般由乳酸钙与氯化亚铁两水溶液混合制得,通过重结晶提纯。
①写出制备乳酸亚铁的离子方程式___________ 。
②1mol乳酸亚铁受热至75℃和170℃时失水,失水质量分别为___________ g、___________ g。
③画出乳酸亚铁的空间立体结构___________ 。
(2)乳酸亚铁还原性的检验
①取乳酸亚铁溶于水,加入酸性高锰酸钾溶液,搅拌后紫色慢慢褪去,溶液变成棕黄色。1mol乳酸亚铁消耗了0.2mol ,化学方程式为
,化学方程式为___________ 。
②1mol乳酸亚铁溶液与5%的双氧水反应,反应剧烈且消耗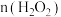 大于1.5mol。控制反应速率后,多次实验,发现消耗
大于1.5mol。控制反应速率后,多次实验,发现消耗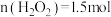 。消耗
。消耗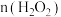 大于1.5mol的原因:
大于1.5mol的原因:___________ 、___________ 。
③双氧水与乳酸亚铁的反应速率远大于酸性高锰酸钾,为了进一步探寻原因,实验设计如下:___________ 。
 常用作缺铁性贫血的补铁剂,能溶于水。
常用作缺铁性贫血的补铁剂,能溶于水。(1)一般由乳酸钙与氯化亚铁两水溶液混合制得,通过重结晶提纯。
①写出制备乳酸亚铁的离子方程式
②1mol乳酸亚铁受热至75℃和170℃时失水,失水质量分别为
③画出乳酸亚铁的空间立体结构
(2)乳酸亚铁还原性的检验
①取乳酸亚铁溶于水,加入酸性高锰酸钾溶液,搅拌后紫色慢慢褪去,溶液变成棕黄色。1mol乳酸亚铁消耗了0.2mol
 ,化学方程式为
,化学方程式为②1mol乳酸亚铁溶液与5%的双氧水反应,反应剧烈且消耗
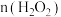 大于1.5mol。控制反应速率后,多次实验,发现消耗
大于1.5mol。控制反应速率后,多次实验,发现消耗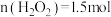 。消耗
。消耗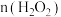 大于1.5mol的原因:
大于1.5mol的原因:③双氧水与乳酸亚铁的反应速率远大于酸性高锰酸钾,为了进一步探寻原因,实验设计如下:
更新时间:2023-05-25 22:45:25
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】写出符合下列要求的离子反应方程式。
(1)向NaHSO4溶液中滴加NaHSO3溶液的离子反应方程式为:__ 。
(2)向NaHSO4溶液中滴加过量氢氧化钡溶液,离子反应方程式为:__ 。
(3)向1Llmol/L的NH4Al(SO4)2溶液中滴加2L等浓度的Ba(OH)2溶液,离子反应方程式为:___ 。
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO 还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为
还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为__ 。
(5)利用 的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为
的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为__ 。
(6)Fe的一种含氧酸根FeO 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是__ 。
(1)向NaHSO4溶液中滴加NaHSO3溶液的离子反应方程式为:
(2)向NaHSO4溶液中滴加过量氢氧化钡溶液,离子反应方程式为:
(3)向1Llmol/L的NH4Al(SO4)2溶液中滴加2L等浓度的Ba(OH)2溶液,离子反应方程式为:
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO
 还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为
还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为(5)利用
 的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为
的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为(6)Fe的一种含氧酸根FeO
 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下列物质:① ②
② 溶液③
溶液③ ④干冰⑤
④干冰⑤ 溶液⑥熔融
溶液⑥熔融 ⑦蔗糖⑧
⑦蔗糖⑧ ⑨氨水⑩
⑨氨水⑩
(1)属于电解质的是_______ (填代号,以下同),属于非电解质的是_______ ,属于单质的是_______ ,能导电的是_______ 。属于酸性氧化物的是_______ 。
(2)上述物质中有两种物质在水溶液中发生反应,其离子方程式为 ,则该反应的化学程式为
,则该反应的化学程式为_______ 。
(3)书写离子方程式:
①醋酸与碳酸钙反应:_______
②过氧化钠与水反应:_______
 ②
② 溶液③
溶液③ ④干冰⑤
④干冰⑤ 溶液⑥熔融
溶液⑥熔融 ⑦蔗糖⑧
⑦蔗糖⑧ ⑨氨水⑩
⑨氨水⑩
(1)属于电解质的是
(2)上述物质中有两种物质在水溶液中发生反应,其离子方程式为
 ,则该反应的化学程式为
,则该反应的化学程式为(3)书写离子方程式:
①醋酸与碳酸钙反应:
②过氧化钠与水反应:
您最近一年使用:0次
【推荐1】亚硝酸钠(NaNO2)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生Na2O、N2和O2,其水溶液呈碱性,能与AgNO3溶液反应生成难溶于水、易溶于酸的AgNO2。由于NaNO2有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
NaNO2+ KI+ = NO↑+ I2+ K2SO4+ Na2SO4+ H2O
(1)补充并配平该化学方程式___________ (若系数为1,请标注“1”)。
(2)从物质分类角度来看,NaNO2是___________ (填字母)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.离子化合物 g.共价化合物
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是___________ 。
(4)下列方法不能用来区分固体NaNO2和NaCl的是___________(填字母)。
(5)误食NaNO2会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒,该过程中NaNO2表现出的性质与下列___________(填字母)反应中H2O2表现出的性质相同。
(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学方程式,并用单线桥表示其电子转移的方向和数目:___________ 。
NaNO2+ KI+ = NO↑+ I2+ K2SO4+ Na2SO4+ H2O
(1)补充并配平该化学方程式
(2)从物质分类角度来看,NaNO2是
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.离子化合物 g.共价化合物
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
(4)下列方法不能用来区分固体NaNO2和NaCl的是___________(填字母)。
| A.分别溶于水 |
| B.分别溶于水并滴加HNO3酸化的AgNO3溶液 |
| C.分别加强热并收集气体检验 |
| D.用筷子分别蘸取固体品尝味道 |
A.2H2O2 2H2O+O2↑ 2H2O+O2↑ |
| B.H2O2+Cl2=2HCl+O2↑ |
| C.H2O2+H2SO4+2KI=2H2O+I2+K2SO4 |
| D.5H2O2+2KMnO4+6HCl=2MnCl2+2KCl+5O2↑+8H2O |
您最近一年使用:0次
【推荐2】回答下列问题:
(1)配平下列反应,并用双线桥标明电子转移方向和数目_______ 。
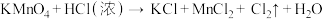
(2) 是一种新的消毒剂,工业上可用
是一种新的消毒剂,工业上可用 氧化
氧化 溶液制取
溶液制取 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ 。
(3)二氧化氯( )是国际上公认的高效、安全的杀菌消毒剂。工业上制备
)是国际上公认的高效、安全的杀菌消毒剂。工业上制备 的反应原理常采用:
的反应原理常采用: 。
。
①浓盐酸在反应中显示出来的性质是_______ (填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol ,则转移电子数约为
,则转移电子数约为_______ 。
(1)配平下列反应,并用双线桥标明电子转移方向和数目
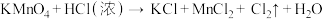
(2)
 是一种新的消毒剂,工业上可用
是一种新的消毒剂,工业上可用 氧化
氧化 溶液制取
溶液制取 ,写出该反应的化学方程式
,写出该反应的化学方程式(3)二氧化氯(
 )是国际上公认的高效、安全的杀菌消毒剂。工业上制备
)是国际上公认的高效、安全的杀菌消毒剂。工业上制备 的反应原理常采用:
的反应原理常采用: 。
。①浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol
 ,则转移电子数约为
,则转移电子数约为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是(可多选)__________ 。
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl→CH3CH2Cl+H2O
C.CH3CH3+Cl2 CH3CH2Cl+HCl
CH3CH2Cl+HCl
D.CH2=CHCl+H2 CH3CH2Cl
CH3CH2Cl
由上述四个反应可归纳出,原子经济性高的是_______ 反应(填反应类型)。
(2)有毒物质的无害化也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,还可将废水中少量的S2-、NO2-和CN-等有毒有害的还原性酸根离子氧化除去.请写出用ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式____________ ,并说明该方法的优点______ 。
(3)下图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图:

活性炭的作用是_______________ ;O3消毒的优点是__________________ ;A、B中放置的物质名称分别是:A_______ ;B__________ 。
(1)下列制备氯乙烷的反应中原子经济性最高的是(可多选)
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl→CH3CH2Cl+H2O
C.CH3CH3+Cl2
 CH3CH2Cl+HCl
CH3CH2Cl+HCl D.CH2=CHCl+H2
 CH3CH2Cl
CH3CH2Cl由上述四个反应可归纳出,原子经济性高的是
(2)有毒物质的无害化也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,还可将废水中少量的S2-、NO2-和CN-等有毒有害的还原性酸根离子氧化除去.请写出用ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式
(3)下图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图:

活性炭的作用是
您最近一年使用:0次

 +2H+=CO2↑+H2O
+2H+=CO2↑+H2O +H2O
+H2O

