亚硝酰氯NOCl常用于合成洗涤剂及合成中间体,某学习小组在实验室利用2NO+Cl2 2NOCl反应制备NOCl,设计如图实验装置(夹持装置略去)。
2NOCl反应制备NOCl,设计如图实验装置(夹持装置略去)。

已知:①NOCl为红褐色液体或黄色气体,熔点-64.5℃,沸点-5.5℃;
②NOCl遇水发生反应NOCl+H2O=HNO2+HCl。
回答下列问题:
(1)仪器a的名称是______ ,仪器a中反应的离子方程式为_____ 。
(2)实验过程中,某同学发现铜与稀硝酸反应较慢,于是有同学提议用“浓硝酸”代替将A装置中的“稀硝酸”,该同学的观点是否合理?______ (填“合理”或“不合理”),试说明原因:______ 。
(3)实验时,应先在三颈烧瓶内通入_____ (填“Cl2”或“NO”),另一种气体可以通入的标志是_____ 。
(4)实验中用NaOH溶液进行尾气处理。
①无水CaCl2的作用是______ 。
②尾气处理时,有同学认为尾气中的某种气体不能完全被吸收。为了充分吸收尾气,可将尾气与______ (填化学式)同时通入NaOH溶液中。
 2NOCl反应制备NOCl,设计如图实验装置(夹持装置略去)。
2NOCl反应制备NOCl,设计如图实验装置(夹持装置略去)。
已知:①NOCl为红褐色液体或黄色气体,熔点-64.5℃,沸点-5.5℃;
②NOCl遇水发生反应NOCl+H2O=HNO2+HCl。
回答下列问题:
(1)仪器a的名称是
(2)实验过程中,某同学发现铜与稀硝酸反应较慢,于是有同学提议用“浓硝酸”代替将A装置中的“稀硝酸”,该同学的观点是否合理?
(3)实验时,应先在三颈烧瓶内通入
(4)实验中用NaOH溶液进行尾气处理。
①无水CaCl2的作用是
②尾气处理时,有同学认为尾气中的某种气体不能完全被吸收。为了充分吸收尾气,可将尾气与
更新时间:2023-05-04 15:56:29
|
相似题推荐
【推荐1】某工厂拟综合处理含 的废水和工业废气(含N2、CO2、SO2、NO和CO),设计如下流程:
的废水和工业废气(含N2、CO2、SO2、NO和CO),设计如下流程:

已知:2NO2+2NaOH=NaNO3+NaNO2+H2O、NO+NO2+2NaOH=2NaNO2+H2O。
回答下列问题:
(1)固体Ⅰ中除含氢氧化钙外,还含有_______ (填化学式,下同),气体Ⅱ的组成为_______ 。
(2)处理含 的废水时,反应的离子方程式为
的废水时,反应的离子方程式为_______ 。
(3)向气体Ⅰ中不能通入过量空气的原因是_______ 。
(4)检验废水中 是否除尽的方法是
是否除尽的方法是_______ (写出实验操作及结果)。
 的废水和工业废气(含N2、CO2、SO2、NO和CO),设计如下流程:
的废水和工业废气(含N2、CO2、SO2、NO和CO),设计如下流程:
已知:2NO2+2NaOH=NaNO3+NaNO2+H2O、NO+NO2+2NaOH=2NaNO2+H2O。
回答下列问题:
(1)固体Ⅰ中除含氢氧化钙外,还含有
(2)处理含
 的废水时,反应的离子方程式为
的废水时,反应的离子方程式为(3)向气体Ⅰ中不能通入过量空气的原因是
(4)检验废水中
 是否除尽的方法是
是否除尽的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】硝酸铵是一种常用的化肥,其工业生产流程如下图。请回答下列问题。_______ 。
(2)吸收塔C中通入空气的目的是_______ ;C、D两个反应容器中发生的反应,属于氧化还原反应的是_______ (填反应容器代号)。
(3)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:_______ 。
(4)金属铜与稀硝酸反应的离子方程式是_____ ,该反应中稀硝酸表现的性质是_______ 。

(2)吸收塔C中通入空气的目的是
(3)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:
(4)金属铜与稀硝酸反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是吸入一半空气的注射器。请回答有关问题:
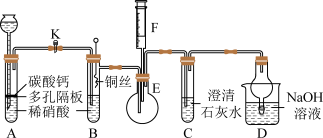
(1)设计装置A的目的是_____ ,为达此目的应进行的操作是____ 。
(2)在完成(1)中的“操作”后,将装置B中的铜丝插入稀硝酸,并微热之,观察到装置B中的现象是___ ,B中反应的离子方程式为____ 。
(3)装置E和F的作用是____ ,为实现此作用,将注射器中的空气推入E中,若气体变为____ 则可证明。
(4)装置D的作用是____ 。

(1)设计装置A的目的是
(2)在完成(1)中的“操作”后,将装置B中的铜丝插入稀硝酸,并微热之,观察到装置B中的现象是
(3)装置E和F的作用是
(4)装置D的作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】如图是中学化学中常见四种物质在一定条件下的转化关系(其他产物已略去)。根据所学知识,回答下列问题:
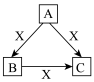
(1)若B、X都是气体单质,C遇空气变为红棕色气体,A遇湿润的红色石蕊试纸变蓝,A在纯氧气中点燃可生成单质B,则A是____ 。写出反应A→C的化学方程式_______
(2)若A是地壳中含量第二位的金属单质,X是一种常见最高价易挥发的含氧酸,常温下,发生如图转化关系,则X是____ (填化学名称),B是____ ,写出反应A→C的离子方程式:______ ;C→B的离子方程式:_______ 。

(1)若B、X都是气体单质,C遇空气变为红棕色气体,A遇湿润的红色石蕊试纸变蓝,A在纯氧气中点燃可生成单质B,则A是
(2)若A是地壳中含量第二位的金属单质,X是一种常见最高价易挥发的含氧酸,常温下,发生如图转化关系,则X是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下:
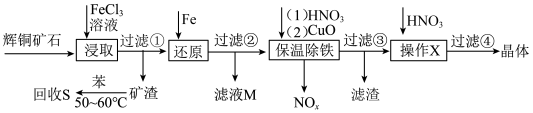
(1)写出浸取过程中Cu2S溶解的离子方程式:______ 。
(2)回收S过程中温度控制在50~60℃之间,不宜过高或过低的原因是______ 。
(3)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为______ ;向滤液M中加入(或通入)下列______ (填字母)物质,得到另一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾
(4)保温除铁过程中,加入CuO的目的是______ ;蒸发浓缩时,要用HNO3溶液调节溶液的pH,其理由是______ 。

(1)写出浸取过程中Cu2S溶解的离子方程式:
(2)回收S过程中温度控制在50~60℃之间,不宜过高或过低的原因是
(3)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为
a.铁 b.氯气 c.高锰酸钾
(4)保温除铁过程中,加入CuO的目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种离子(忽略和水的反应以及水的电离),离子浓度均为
中的若干种离子(忽略和水的反应以及水的电离),离子浓度均为 。某同学进行了如下实验:
。某同学进行了如下实验:
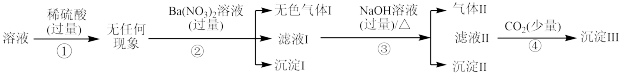
回答下列问题:
(1)通过过程①判断溶液中一定不存在___________ (填离子符号)。
(2)气体Ⅰ为___________ (填化学式,下同),沉淀Ⅰ为___________ 。
(3)过程③中生成气体的离子方程式为___________ 。
(4)下列说法正确的是___________ (填标号)。
a.滤液Ⅰ中一定含有 、
、 ,滤液Ⅰ中一定含有
,滤液Ⅰ中一定含有 、
、
b.将沉淀Ⅲ加入足量的稀盐酸中,无气泡产生
c.沉淀Ⅱ可溶于强酸,也可溶于强碱
(5)实验结束后,该同学得出结论,该溶液中一定含有___________ (填离子符号,下同),判断的理由是___________ ,该溶液中一定没有___________ 。
(6)根据(5)的结论,取少量该溶液于烧杯中,加入足量的烧碱溶液,观察到溶液中的现象是___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种离子(忽略和水的反应以及水的电离),离子浓度均为
中的若干种离子(忽略和水的反应以及水的电离),离子浓度均为 。某同学进行了如下实验:
。某同学进行了如下实验: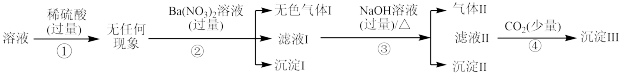
回答下列问题:
(1)通过过程①判断溶液中一定不存在
(2)气体Ⅰ为
(3)过程③中生成气体的离子方程式为
(4)下列说法正确的是
a.滤液Ⅰ中一定含有
 、
、 ,滤液Ⅰ中一定含有
,滤液Ⅰ中一定含有 、
、
b.将沉淀Ⅲ加入足量的稀盐酸中,无气泡产生
c.沉淀Ⅱ可溶于强酸,也可溶于强碱
(5)实验结束后,该同学得出结论,该溶液中一定含有
(6)根据(5)的结论,取少量该溶液于烧杯中,加入足量的烧碱溶液,观察到溶液中的现象是
您最近一年使用:0次



