回答下列问题:
(1)锌-空气电池是金属空气电池的一种,电解质溶液为KOH溶液,工作示意图如图1所示。
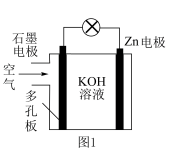
Zn电极作______ 极,写出通入空气一极的电极反应式:______ 。
(2)氯碱工业中电解饱和食盐水的原理示意图如图2所示:
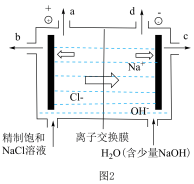
①a口产生的气体是______ ,c口获得的产品是______ ,当d口产生标况下2.24L气体时,电路中转移电子的物质的量为______ 。
②写出电解饱和食盐水的离子方程式______ 。
(3)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。鉴于腐蚀问题的严重性,国内外对防腐工作都很重视,采取各种措施来减轻腐蚀的危害,图3是金属防护的两个例子。
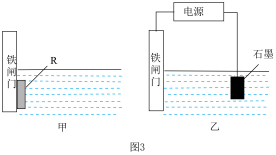
①为了降低某水库的铁闸门被腐蚀的速率,可以采用图3甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用______ (填字母)。
A.铜 B.石墨 C.锌
②图3乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的______ (填“正”或“负”)极,该金属防护的方法叫做______ 。
(1)锌-空气电池是金属空气电池的一种,电解质溶液为KOH溶液,工作示意图如图1所示。

Zn电极作
(2)氯碱工业中电解饱和食盐水的原理示意图如图2所示:

①a口产生的气体是
②写出电解饱和食盐水的离子方程式
(3)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。鉴于腐蚀问题的严重性,国内外对防腐工作都很重视,采取各种措施来减轻腐蚀的危害,图3是金属防护的两个例子。

①为了降低某水库的铁闸门被腐蚀的速率,可以采用图3甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.石墨 C.锌
②图3乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的
更新时间:2023-05-04 23:31:32
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】为验证反应Fe3++Ag⇌Fe2++Ag+,利用如图电池装置进行实验。
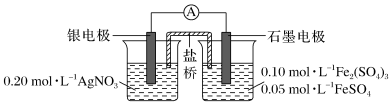
(1)由Fe2(SO4)3固体配制500 mL 0.1 mol·L-1 Fe2(SO4)3溶液,需要的仪器有胶头滴管、量筒、烧杯、玻璃棒、500 mL容量瓶、____ (填写名称);在烧杯中溶解固体时,先加入一定体积的____ 稀溶液,搅拌后再加入一定体积的水。
(2)电流表显示电流由银电极流向石墨电极。可知,盐桥中的阳离子进入____ 电极溶液中。
(3)根据(2)实验结果,可知石墨电极的电极反应式为_______ ,银电极的电极反应式为_______ 。因此,Fe3+氧化性小于____ 。
(4)电池装置中,盐桥连接两电极电解质溶液。如果盐桥中电解质为KNO3,反应一段时间后,可以观察到电流表指针反转,原因是_______ 。

(1)由Fe2(SO4)3固体配制500 mL 0.1 mol·L-1 Fe2(SO4)3溶液,需要的仪器有胶头滴管、量筒、烧杯、玻璃棒、500 mL容量瓶、
(2)电流表显示电流由银电极流向石墨电极。可知,盐桥中的阳离子进入
(3)根据(2)实验结果,可知石墨电极的电极反应式为
(4)电池装置中,盐桥连接两电极电解质溶液。如果盐桥中电解质为KNO3,反应一段时间后,可以观察到电流表指针反转,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应。请回答下列问题:
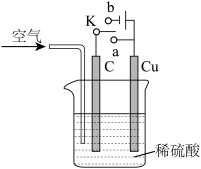
(1)甲同学认为,不通入空气,将 K 与_____ (填“a”或“b”)连接,即可实现。则总反应的离子方程式为_____ 。
(2)乙同学认为在通入空气的同时,将开关 K 与_____ 连通,也可以实现,则电池总反应的化学方程式为_____ 。

(1)甲同学认为,不通入空气,将 K 与
(2)乙同学认为在通入空气的同时,将开关 K 与
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.能源是现代文明的原动力,化学电池在生产生活中有着广泛的应用。
(1)根据构成原电池的本质判断,下列反应可以设计成原电池的是_____ (填序号)。
Ⅱ.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
(2)放电时负极反应为_____ 。
(3)放电时正极附近溶液的碱性_____ (填“增强”或“减弱”或“不变”)。
(4)放电时每转移_____ mol电子,正极有1molK2FeO4被还原。
Ⅲ.回答下列问题:
(5)科学家研发出一种有利于“碳中和”的新电池系统,通过二氧化碳溶于水触发电化学反应,其工作原理如图所示(钠超离子导体只允许Na+通过)。系统工作时,下列有关说法中错误的是_____ 。
Ⅳ.中国科学技术大学开发了一种高性能的水系锰基锌电池。其工作原理如图所示,已知该装置工作一段时间后,K2SO4溶液的浓度增大。_____ 。
(7)a膜为_____ (填“阳离子”或“阴离子”,下同)交换膜,b膜为_____ 交换膜。
(1)根据构成原电池的本质判断,下列反应可以设计成原电池的是
| A.CaO(s)+H2O(l)=Ca(OH)2(aq) | B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) |
| C.2CO(g)+O2(g)=2CO2(g) | D.Fe(s)+2FeCl3(aq)=3FeCl2(aq) |
Ⅱ.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。(2)放电时负极反应为
(3)放电时正极附近溶液的碱性
(4)放电时每转移
Ⅲ.回答下列问题:
(5)科学家研发出一种有利于“碳中和”的新电池系统,通过二氧化碳溶于水触发电化学反应,其工作原理如图所示(钠超离子导体只允许Na+通过)。系统工作时,下列有关说法中错误的是
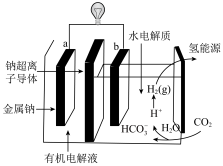
| A.Na+将从a极移动到b极 |
| B.该电池的电解液可以换成更易导电的饱和NaCl溶液 |
C.b极区可能会发生Na++HCO =NaHCO3↓ =NaHCO3↓ |
| D.b极区每生成1molH2转移2mol电子 |
Ⅳ.中国科学技术大学开发了一种高性能的水系锰基锌电池。其工作原理如图所示,已知该装置工作一段时间后,K2SO4溶液的浓度增大。

(7)a膜为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】电解原理在化学工业中有广泛应用。如上图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。
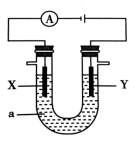
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则:
①电解池中X极上的电极反应式为_______ 。
②Y电极上的电极反应式为_______ ,检验该电极反应产物的方法及现象是_______ 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是_______ ,电极反应式是_______ 。
②Y电极的材料是_______ ,电极反应式是_______ 。
(说明:杂质发生的电极反应不必写出)。
(3)如利用该装置实现铁上镀锌,电极X上发生的反应为_______ ,电解池盛放的电镀液可以是_______ 或_______ (只要求填两种电解质溶液)。

请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则:
①电解池中X极上的电极反应式为
②Y电极上的电极反应式为
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是
②Y电极的材料是
(说明:杂质发生的电极反应不必写出)。
(3)如利用该装置实现铁上镀锌,电极X上发生的反应为
您最近一年使用:0次
【推荐2】工业废气、汽车尾气排放出的 SO2、NOx等,是形成雾霾的重要因素.霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾.
(1)NOx和 SO2在空气中存在下列平衡:
2NO(g) + O2(g) 2NO2(g) △ H =− 113.0kJ
2NO2(g) △ H =− 113.0kJ mol−1
mol−1
2SO2(g) + O2(g) 2SO3(g) △ H =− 196.6kJ
2SO3(g) △ H =− 196.6kJ mol−1
mol−1
SO2通常在二氧化氮的存在下,进一步被氧化,生成 SO3.
①写出 NO2和 SO2反应的热化学方程式为_____ .
②随温度升高,该反应化学平衡常数变化趋势是_____ .
(2)提高2SO2(g) + O2(g) 2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是
2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是_____ .②在①中条件下,反应达到平衡后,改变下列条件,能使 SO2的转化率提高的是_____ (填字母).
a.温度和容器体积不变,充入 1.0mol He
b.温度和容器体积不变,充入 1.0mol O2
c.在其他条件不变时,减少容器的体积
d.在其他条件不变时,改用高效催化剂
e.在其他条件不变时,升高体系温度

(3)工业上利用氯碱工业产品治理含二氧化硫的废气.如图是氯碱工业中电解饱和食盐水的原理示意图
①用溶液A吸收含二氧化硫的废气,其反应的离子方程式是_____ .
②用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是_____ .
(1)NOx和 SO2在空气中存在下列平衡:
2NO(g) + O2(g)
 2NO2(g) △ H =− 113.0kJ
2NO2(g) △ H =− 113.0kJ mol−1
mol−12SO2(g) + O2(g)
 2SO3(g) △ H =− 196.6kJ
2SO3(g) △ H =− 196.6kJ mol−1
mol−1SO2通常在二氧化氮的存在下,进一步被氧化,生成 SO3.
①写出 NO2和 SO2反应的热化学方程式为
②随温度升高,该反应化学平衡常数变化趋势是
(2)提高2SO2(g) + O2(g)
 2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是
2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是a.温度和容器体积不变,充入 1.0mol He
b.温度和容器体积不变,充入 1.0mol O2
c.在其他条件不变时,减少容器的体积
d.在其他条件不变时,改用高效催化剂
e.在其他条件不变时,升高体系温度

(3)工业上利用氯碱工业产品治理含二氧化硫的废气.如图是氯碱工业中电解饱和食盐水的原理示意图
①用溶液A吸收含二氧化硫的废气,其反应的离子方程式是
②用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)一种燃料电池中发生的化学反应为:在酸性溶液中甲醇(CH3OH)与氧作用生成水和二氧化碳。该电池负极发生的反应是___________ 。
(2)要实现铁上镀银,则阳极为___________ ,电极反应式为___________ ,阴极为___________ ,电极反应式为___________ ,电镀液为___________ 。
(3)电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
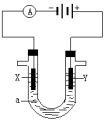
①若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则电解池中X极上的电极反应为___________ ,在X极附近观察到的现象是 :___________ 。
②Y电极上的电极反应式是___________ ,检验该电极反应产物的方法是 :___________ 。
③如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是___________ ,电极反应式是___________ ,Y电极的材料是___________ ,电极反应式是___________ 。(假设粗铜中含铁、锌、银、金)
(4)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2
 2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):
2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):
放电时:正极的电极反应式是___________ ;电解液中H2SO4的浓度将变___________ ;当外电路通过1 mol电子时,理论上负极板的质量增加___________ g.充电时:阴极的电极反应式是___________ 。
(1)一种燃料电池中发生的化学反应为:在酸性溶液中甲醇(CH3OH)与氧作用生成水和二氧化碳。该电池负极发生的反应是
(2)要实现铁上镀银,则阳极为
(3)电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

①若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则电解池中X极上的电极反应为
②Y电极上的电极反应式是
③如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是
(4)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2

 2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):
2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):放电时:正极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: 溶液,则反应一段时间后:
溶液,则反应一段时间后:
①乙池中阳极的电极反应式是_______ 。
②若要保护金属铁,可将甲池中的C棒换成 棒,则该防护方法称为
棒,则该防护方法称为_______ 。
(2)若两池中电解质溶液均为饱和 溶液:
溶液:
①写出乙池中总反应的离子方程式_______ 。
②甲池中碳极上电极反应式是_______ 。
③若乙池转移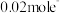 后停止实验,池中电解质溶液体积是
后停止实验,池中电解质溶液体积是 ,则室温下溶液混合均匀后的
,则室温下溶液混合均匀后的
_______ 。

 溶液,则反应一段时间后:
溶液,则反应一段时间后:①乙池中阳极的电极反应式是
②若要保护金属铁,可将甲池中的C棒换成
 棒,则该防护方法称为
棒,则该防护方法称为(2)若两池中电解质溶液均为饱和
 溶液:
溶液:①写出乙池中总反应的离子方程式
②甲池中碳极上电极反应式是
③若乙池转移
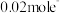 后停止实验,池中电解质溶液体积是
后停止实验,池中电解质溶液体积是 ,则室温下溶液混合均匀后的
,则室温下溶液混合均匀后的
您最近一年使用:0次
【推荐2】如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:

(1)若两装置中均为 溶液,反应一段时间后:
溶液,反应一段时间后:
①有红色物质析出的是甲装置中的___________ 棒,乙装置中的___________ 棒;
②乙装置的电化学防护法称为___________ ,其中碳极的电极反应式是:___________ 。
③取少量甲装置中负极附近溶液加入2滴 溶液,现象为
溶液,现象为___________ ,生成沉淀的化学式为___________ 。
(2)若两装置中均为饱和 溶液:
溶液:
①写出乙装置中总反应的离子方程式:___________ 。
②将湿润的淀粉 试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因
试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因___________
(3)用铂作电极电解饱和的下列物质的水溶液,一会儿后,向剩余电解液中加适量水,能使溶液和电解前相同的是___________。

(1)若两装置中均为
 溶液,反应一段时间后:
溶液,反应一段时间后:①有红色物质析出的是甲装置中的
②乙装置的电化学防护法称为
③取少量甲装置中负极附近溶液加入2滴
 溶液,现象为
溶液,现象为(2)若两装置中均为饱和
 溶液:
溶液:①写出乙装置中总反应的离子方程式:
②将湿润的淀粉
 试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因
试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因(3)用铂作电极电解饱和的下列物质的水溶液,一会儿后,向剩余电解液中加适量水,能使溶液和电解前相同的是___________。
A. | B. | C. | D. |
您最近一年使用:0次
【推荐3】在劳动过程中能够感受到劳动的乐趣,获得自信和满足。请回答下列问题:
(1)家务劳动:小江用肥皂洗衣服过程中发现水中浮渣多泡沫少、衣服洗不干净,原因可能是_____ ,生活中可用_____ (选填“酱油”、“洗洁精”或“食醋”)清洗水壶中的水垢(主要成分是碳酸钙)。
(2)田间劳动:小江向秧苗施加尿素,尿素是_____ (选填“氮肥”、“钾肥”、“磷粉”或“复合肥”),检验肥料包装塑料袋是否具有热塑性的方法是_____ 。
(3)工厂劳动:小江参观工厂时发现工人们可用_____ (合理即可)清洗铁锈、在钢铁表面刷漆,刷漆的防锈原理是_____ 。
(1)家务劳动:小江用肥皂洗衣服过程中发现水中浮渣多泡沫少、衣服洗不干净,原因可能是
(2)田间劳动:小江向秧苗施加尿素,尿素是
(3)工厂劳动:小江参观工厂时发现工人们可用
您最近一年使用:0次



