氢气既是一种清洁能源,又是重要的化工原料。回答下列问题:
(1)已知:断裂1molH-H、1molO=O、1molH-O键吸收的能量依次为436kJ、498kJ、467kJ,在2H2(g)+O2(g)=2H2O(g)反应中,44.8LH2(标准状况治好完全反应放出的能量为_____ kJ。
(2)实验室用纯净的铝片与稀硫酸反应制取氢气。
①实验过程如图所示,分析判断_____ 段化学反应速率最快(填OE、EF或FG)。
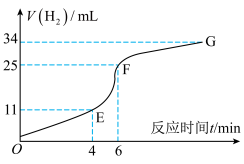
②将铝片投入盛有稀硫酸的烧杯中,刚开始时产生H2的速率逐渐加快,其原因是_____ 。
(3)要加快铝与硫酸溶液制H2的反应速率,小组成员提出一系列方案,比如:①加入某种催化剂;②加入蒸馏水:③将铝片换成铝粉;④增加硫酸的浓度至18mol/L;⑤_____ ;⑥_____ 。以上方案不合理的有_____ ;请你再补充两种合理方案,填入空白⑤⑥处。
(1)已知:断裂1molH-H、1molO=O、1molH-O键吸收的能量依次为436kJ、498kJ、467kJ,在2H2(g)+O2(g)=2H2O(g)反应中,44.8LH2(标准状况治好完全反应放出的能量为
(2)实验室用纯净的铝片与稀硫酸反应制取氢气。
①实验过程如图所示,分析判断

②将铝片投入盛有稀硫酸的烧杯中,刚开始时产生H2的速率逐渐加快,其原因是
(3)要加快铝与硫酸溶液制H2的反应速率,小组成员提出一系列方案,比如:①加入某种催化剂;②加入蒸馏水:③将铝片换成铝粉;④增加硫酸的浓度至18mol/L;⑤
更新时间:2023-05-07 21:56:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表中的数据是破坏1 mol物质中的化学键所消耗的能量(kJ):
根据上述数据回答(1)~(5)题。
(1)下列物质本身具有的能量最低的是____ 。
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中,最稳定的是____ 。
A.HCl B.HBr C.HI
(3)X2+H2 2HX(X代表Cl、Br、I )的反应是吸热反应还是放热反应?答:
2HX(X代表Cl、Br、I )的反应是吸热反应还是放热反应?答:___________ 。
(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是_____ 。
(5)若无上表中的数据,你能正确回答出问题(4)吗?
答:_____ ,你的根据是____________ 。
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量/kJ | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
根据上述数据回答(1)~(5)题。
(1)下列物质本身具有的能量最低的是
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中,最稳定的是
A.HCl B.HBr C.HI
(3)X2+H2
 2HX(X代表Cl、Br、I )的反应是吸热反应还是放热反应?答:
2HX(X代表Cl、Br、I )的反应是吸热反应还是放热反应?答:(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是
(5)若无上表中的数据,你能正确回答出问题(4)吗?
答:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题
(1)从能量的变化和反应的快慢等角度研究反应:2H2 + O2 = 2H2O。已知该反应为放热反应,如图能正确表示该反应中能量变化的是_______ 。(填“A”或“B”)

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如表:
则生成1mol水可以放出热量 _______ kJ
(2)以下反应:①木炭与水制备水煤气②氯酸钾分解③炸药爆炸④酸与碱的中和反应⑤生石灰与水作用制熟石灰⑥ Ba(OH)2·8H2O与NH4Cl ⑦气态水液化,属于放热反应的有:_______ (填序号)。
(3)分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:

①以下叙述中,正确的是_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中 向铜片方向移动
向铜片方向移动
②乙中能量转化的主要形式为_______ 。
③在乙实验中,如果把稀硫酸换成硫酸铜溶液,铜电极的电极反应式是_______ ,当电路中转移0.25 mol电子时,消耗负极材料的质量为_______ g。
(1)从能量的变化和反应的快慢等角度研究反应:2H2 + O2 = 2H2O。已知该反应为放热反应,如图能正确表示该反应中能量变化的是

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如表:
| 化学键 | H-H | O=O | H-O |
| 键能kJ/mol | 436 | 496 | 463 |
(2)以下反应:①木炭与水制备水煤气②氯酸钾分解③炸药爆炸④酸与碱的中和反应⑤生石灰与水作用制熟石灰⑥ Ba(OH)2·8H2O与NH4Cl ⑦气态水液化,属于放热反应的有:
(3)分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:

①以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中
 向铜片方向移动
向铜片方向移动②乙中能量转化的主要形式为
③在乙实验中,如果把稀硫酸换成硫酸铜溶液,铜电极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硫—碘循环分解水制氢主要涉及下列反应:
① SO2+2H2O+I2===H2SO4+2HI ② 2HI H2+I2 ③ 2H2SO4 === 2SO2+O2+2H2O
H2+I2 ③ 2H2SO4 === 2SO2+O2+2H2O
(1)整个过程中SO2、I2的作用是______ 。
(2)一定温度下,向1L密闭容器中加入1mol HI(g),发生反应②,已知H2的物质的量随时间的变化如图所示,则在0~2 min内的平均反应速率v (HI) =______ ;
(3)已知拆开1 mol H—I键需要消耗298kJ能量,形成1mol H—H键能够释放436kJ能量,形成1mol I—I键能够释放151kJ能量,则在反应②中,分解0.2mol HI时会______ (填“吸收”或“释放”)______ kJ能量。
(4)实验室用Zn和硫酸制H2,为了加快反应速率下列措施不可行 的是__ (填序号)
a.加入浓硝酸 b.加入少量CuSO4 固体 c.用粗锌代替纯锌 d.加热 e.把锌粒弄成锌粉 f.用98.3%的浓硫酸
(5)氢气可用于制燃料电池,某种氢氧燃料电池是用固体金属化合物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2--4e-== 2H2O ,B极:O2+4e-== 2O2-,则A极是电池的___ 极;电子从该极___ (填“流入”或“流出”)。
① SO2+2H2O+I2===H2SO4+2HI ② 2HI
 H2+I2 ③ 2H2SO4 === 2SO2+O2+2H2O
H2+I2 ③ 2H2SO4 === 2SO2+O2+2H2O(1)整个过程中SO2、I2的作用是
(2)一定温度下,向1L密闭容器中加入1mol HI(g),发生反应②,已知H2的物质的量随时间的变化如图所示,则在0~2 min内的平均反应速率v (HI) =

(3)已知拆开1 mol H—I键需要消耗298kJ能量,形成1mol H—H键能够释放436kJ能量,形成1mol I—I键能够释放151kJ能量,则在反应②中,分解0.2mol HI时会
(4)实验室用Zn和硫酸制H2,为了加快反应速率下列措施
a.加入浓硝酸 b.加入少量CuSO4 固体 c.用粗锌代替纯锌 d.加热 e.把锌粒弄成锌粉 f.用98.3%的浓硫酸
(5)氢气可用于制燃料电池,某种氢氧燃料电池是用固体金属化合物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2--4e-== 2H2O ,B极:O2+4e-== 2O2-,则A极是电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】请根据所学知识回答下列问题:
(1)已知反应Fe+H2SO4=FeSO4+H2↑。若要加快该反应的速率,在其他条件不变的情况下,下列措施可行的是______ (填字母)。
(2)近年来,科学家致力于将二氧化碳和氢气转化为甲醇(CH3OH)的技术研究,为解决环境与能源问题提供了新途径。某温度下在2L的恒容密闭容器中,充入4molCO2和4molH2,发生如下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
①能判断该反应已达到化学反应限度的是______ (填字母)。
A.容器内压强保持不变
B.容器中CO2浓度与H2浓度之比为1:3
C.容器中CO2的物质的量分数保持不变
D.CO2的生成速率与CH3OH的生成速率相等
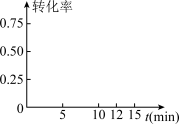
②现测得H2的浓度随时间变化如图所示。从反应开始经过12min达到平衡,则0~5min内CO2的平均反应速率v(CO2)=______ ,第12min时,甲醇的物质的量浓度为______ 。

③请在图中画出0~15min内H2转化率随时间变化的示意图______ 。
(3)燃料电池能有效提高能源利用率,写出甲醇(CH3OH)空气燃料电池在碱性条件(KOH溶液)中的负极电极反应式______ 。
(1)已知反应Fe+H2SO4=FeSO4+H2↑。若要加快该反应的速率,在其他条件不变的情况下,下列措施可行的是
| A.升高温度 | B.改稀硫酸为98%的浓硫酸 |
| C.将纯铁改为生铁 | D.往稀硫酸中加入少量Na2SO4(s) |
 CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。①能判断该反应已达到化学反应限度的是
A.容器内压强保持不变
B.容器中CO2浓度与H2浓度之比为1:3
C.容器中CO2的物质的量分数保持不变
D.CO2的生成速率与CH3OH的生成速率相等
②现测得H2的浓度随时间变化如图所示。从反应开始经过12min达到平衡,则0~5min内CO2的平均反应速率v(CO2)=

③请在图中画出0~15min内H2转化率随时间变化的示意图

(3)燃料电池能有效提高能源利用率,写出甲醇(CH3OH)空气燃料电池在碱性条件(KOH溶液)中的负极电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】可逆反应 A(g) + 2B(g)  2C(g) ΔH<0,在一定条件下达到平衡,若改变条件,将变化结果(“增大”、“减小”或“不变”)填入空格。
2C(g) ΔH<0,在一定条件下达到平衡,若改变条件,将变化结果(“增大”、“减小”或“不变”)填入空格。
(1)升高温度,B的转化率_____________ ,v(正)____________ ,v(逆)____________ 。
(2)保持温度和压强不变,加入惰性气体,则C的物质的量_____________ ,A的转化率_____________ 。
(3) 保持温度和体积不变,加入惰性气体,A的转化率_____________ 。
(4)若温度和体积不变,反应从开始到平衡,容器内气体的密度_____________ ,压强____________ 。
 2C(g) ΔH<0,在一定条件下达到平衡,若改变条件,将变化结果(“增大”、“减小”或“不变”)填入空格。
2C(g) ΔH<0,在一定条件下达到平衡,若改变条件,将变化结果(“增大”、“减小”或“不变”)填入空格。(1)升高温度,B的转化率
(2)保持温度和压强不变,加入惰性气体,则C的物质的量
(3) 保持温度和体积不变,加入惰性气体,A的转化率
(4)若温度和体积不变,反应从开始到平衡,容器内气体的密度
您最近一年使用:0次
填空题
|
适中
(0.65)
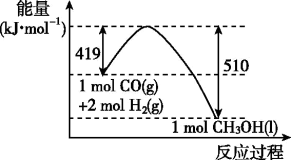
【推荐3】如图是CO和H2反应生成CH3OH的能量变化图:
(1)写出该反应的化学方程式:_______
(2)从图中可知,1molCO和2molH2化学键的断裂共_______ (“放出”或“吸收”,下同)419kJ的热量,形成1molCH3OH_______ 510kJ热量。
(3)该反应是_______ (“放热”或“吸热”)反应。比较1molCH3OH(液体)和1molCH3OH(气体)的稳定性,稳定性好的是_______ (“前者”或“后者”)
(4)下列措施能加快该反应速率的是_______

(1)写出该反应的化学方程式:
(2)从图中可知,1molCO和2molH2化学键的断裂共
(3)该反应是
(4)下列措施能加快该反应速率的是_______
| A.降低温度 | B.缩小体积 | C.体积不变加入Ar | D.使用催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】汽车尾气中的主要污染物是NOx和CO,它们是现代化城市中的重要大气污染物。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其能量变化如图1所示,则图1中三种分子最稳定的是_______ ,图1中对应反应的热化学方程式为________________ 。
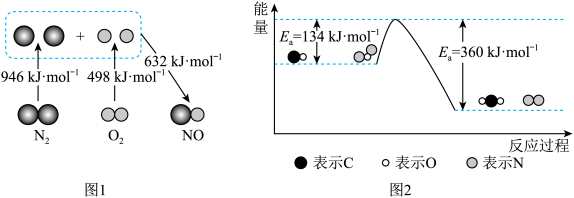
(2)N2O和CO均是有害气体,可在 表面转化为无害气体,其反应原理如下:N2O(g)+CO(g)=CO2(g) + N2(g) ΔH。有关化学反应的能量变化过程如图2所示。
表面转化为无害气体,其反应原理如下:N2O(g)+CO(g)=CO2(g) + N2(g) ΔH。有关化学反应的能量变化过程如图2所示。
①图2中反应是_______ (填“放热”或“吸热”)反应,该反应的活化能为_______ ,该反应的ΔH=_______ ;
②在反应体系中加入Pt2O+作为该反应的催化剂,则Ea_______ (填“增大”“减小”或“不变”,下同), ΔH _______ 。
(3)利用NH3还原法可将NOx还原为N2进行脱除。已知:
4NH3(g)+6NO(g)=5N2(g)+6H2O(g) ΔH=﹣2070 kJ·mol-1
若有0.5 mol NO被还原,则_____ (填“释放”或“吸收”)的热量为______ 。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其能量变化如图1所示,则图1中三种分子最稳定的是

(2)N2O和CO均是有害气体,可在
 表面转化为无害气体,其反应原理如下:N2O(g)+CO(g)=CO2(g) + N2(g) ΔH。有关化学反应的能量变化过程如图2所示。
表面转化为无害气体,其反应原理如下:N2O(g)+CO(g)=CO2(g) + N2(g) ΔH。有关化学反应的能量变化过程如图2所示。①图2中反应是
②在反应体系中加入Pt2O+作为该反应的催化剂,则Ea
(3)利用NH3还原法可将NOx还原为N2进行脱除。已知:
4NH3(g)+6NO(g)=5N2(g)+6H2O(g) ΔH=﹣2070 kJ·mol-1
若有0.5 mol NO被还原,则
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照以下方案完成实验。
(1)实验①和②的目的是___ 。
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图1。分析图1能够得出的实验结论是__ 。

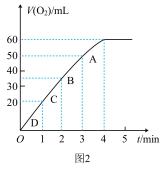
(3)加入0.1gMnO2粉末于50mLH2O2溶液中,在标准状况下放出气体的体积和时间的关系如图2所示。反应速率变化的原因是__ 。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2%H2O2溶液 | 无 |
| ② | 10mL5%H2O2溶液 | 无 |
| ③ | 10mL5%H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ④ | 10mL5%H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ⑤ | 10mL5%H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(1)实验①和②的目的是
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图1。分析图1能够得出的实验结论是

(3)加入0.1gMnO2粉末于50mLH2O2溶液中,在标准状况下放出气体的体积和时间的关系如图2所示。反应速率变化的原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐3】反应A(g)+B(g)  C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
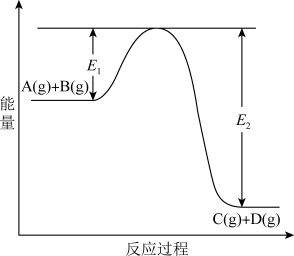
(1)该反应是____________________ 反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率______ (填“增大”“减小”“不变”),原因是_______________________________ ;
(3)反应体系中加入催化剂对反应热是否有影响?________ ,原因是_________ :
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________ ,E2________ (填“增大”“减小、”“不变”)。
 C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是
(2)当反应达到平衡时,升高温度,A的转化率
(3)反应体系中加入催化剂对反应热是否有影响?
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某科研小组将微电池技术用于去除天然气中的 ,装置如图所示,
,装置如图所示, 。
。
1.写出负极的电极反应式为_______ 。
2.一段时间后,单位时间内 的去除率降低,其可能的原因是
的去除率降低,其可能的原因是_______ 。
 ,装置如图所示,
,装置如图所示,
 。
。1.写出负极的电极反应式为
2.一段时间后,单位时间内
 的去除率降低,其可能的原因是
的去除率降低,其可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定量的盐酸和过量的锌粒反应产生氢气,为了减慢反应速率,又不影响产生的氢气的总量,下列措施可行的是________ ①加入NaOH固体 ②加入一定量的水 ③加入少量硫酸钠溶液 ④加入少量硫酸铜溶液 ⑤加入CH3COONa固体 ⑥加入KNO3溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】研究化学反应的快慢和限度具有十分重要的意义。
回答下列问题:
(1)反应2SO2(g) + O2(g) 2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率
2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率_________ ;使用催化剂V2O5,正反应的速率__________ (以上填“增加”、“不变”或“减小”), 催化剂对该反应的平衡状态_________ 影响(“有”或“无”)。
(2)常温下,实验室用100 mL 6.0 mol·L-1硫酸跟足量锌粉反应制取氢气。
①为降低反应进行的速率,又不影响生成氢气的量,可向反应物中加入____ (填序号 )。
A.CH3COONa固体 B.KNO3固体
C.K2SO4溶液 D.KHSO4溶液
②向溶液中滴加少量硫酸铜溶液,反应速率加快,原因是___________________ 。
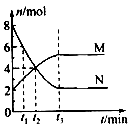
(3)一定温度下,在体积固定的密闭容器中,有色气体N与无色气体M的物质的量随时间变化曲线如图所示。图中能够表明起始加入的物质是__________________ ,反应达平衡的时间是____________ ,该反应的化学方程式可表示为______________________________ ;下列说法中能够判定该反应处于平衡状态的是______________ 填 序号)。
A.容器的压强不再变化
B.气体的颜色不再变化
C.每反应2 mol的N生成1 mol的M
D.气体的密度不再发生变化
回答下列问题:
(1)反应2SO2(g) + O2(g)
 2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率
2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率(2)常温下,实验室用100 mL 6.0 mol·L-1硫酸跟足量锌粉反应制取氢气。
①为降低反应进行的速率,又不影响生成氢气的量,可向反应物中加入
A.CH3COONa固体 B.KNO3固体
C.K2SO4溶液 D.KHSO4溶液
②向溶液中滴加少量硫酸铜溶液,反应速率加快,原因是
(3)一定温度下,在体积固定的密闭容器中,有色气体N与无色气体M的物质的量随时间变化曲线如图所示。图中能够表明起始加入的物质是

A.容器的压强不再变化
B.气体的颜色不再变化
C.每反应2 mol的N生成1 mol的M
D.气体的密度不再发生变化
您最近一年使用:0次



