19世纪60年代,德国化学家凯库勒在梦中“看见”苯分子中原子的排列顺序,提出了两点假设。
i.苯的六个碳原子形成闭合环状,即平面六边形;

ii.每个碳原子均连接一个氢原子,各碳原子间存在着单、双键交替形式。
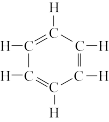
【交流研讨】
(1)如果苯分子为上述结构,则其可能具有什么重要的化学性质_________ ?若存在碳碳双键,则性质应与乙烯性质相似
(2)能否设计实验方案来证明________ ?
i.苯的六个碳原子形成闭合环状,即平面六边形;

ii.每个碳原子均连接一个氢原子,各碳原子间存在着单、双键交替形式。

【交流研讨】
(1)如果苯分子为上述结构,则其可能具有什么重要的化学性质
(2)能否设计实验方案来证明
更新时间:2023-05-17 21:00:47
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】为了验证凯库勒有关苯环结构的观点,甲同学设计了如下实验方案。
①按如图所示的装置图连接好各仪器;

②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题。
(1)A中所发生反应的反应类型为_________ ,能证明凯库勒观点错误的实验现象是_______ 。
(2)装置B的作用是__________ 。
(3)C中烧瓶的容积为500 mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对H2的相对密度为37.9,则实验结束时,进入烧瓶中的水的体积为________ mL(空气的平均相对分子质量为29)。
(4)实验前应对A、B、C三个装置的气密性进行逐一检查,则检查装置C气密性的操作为________ 。
①按如图所示的装置图连接好各仪器;

②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题。
(1)A中所发生反应的反应类型为
(2)装置B的作用是
(3)C中烧瓶的容积为500 mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对H2的相对密度为37.9,则实验结束时,进入烧瓶中的水的体积为
(4)实验前应对A、B、C三个装置的气密性进行逐一检查,则检查装置C气密性的操作为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
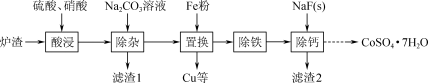
【推荐2】实验室从某废弃炉渣(含Cu、Ni、Co、Ca、Fe等金属及其氧化物)中回收Cu、Ni、Co,其部分实验过程如下:___________ (答2条即可)。
(2)将“置换”后溶液中的Fe2+氧化为Fe3+,控制pH可形成Na2Fe6(SO4)4(OH)12沉淀。写出该反应的离子方程式:___________ 。
(3)向“除铁”后的滤液中加入NaF,使Ca2+转化为CaF2沉淀除去。若溶液pH偏低,将会导致CaF2沉淀不完全,其原因是___________ 。[Ksp(CaF2)=5.3×10-9、Ka(HF)=6.3×10-4]
(4)“除钙”后的溶液经过萃取、反萃取等操作可分离钴和镍,其中萃取原理可表示为Co2+(水层)+2HA(有机层) CoA2(有机层)+2H+(水层)。
CoA2(有机层)+2H+(水层)。___________ (已知Co2+、Ni2+的萃取率与pH的关系曲线如图所示。实验中须使用的试剂有Cyanex272、H2SO4溶液、NaOH溶液)。
(2)将“置换”后溶液中的Fe2+氧化为Fe3+,控制pH可形成Na2Fe6(SO4)4(OH)12沉淀。写出该反应的离子方程式:
(3)向“除铁”后的滤液中加入NaF,使Ca2+转化为CaF2沉淀除去。若溶液pH偏低,将会导致CaF2沉淀不完全,其原因是
(4)“除钙”后的溶液经过萃取、反萃取等操作可分离钴和镍,其中萃取原理可表示为Co2+(水层)+2HA(有机层)
 CoA2(有机层)+2H+(水层)。
CoA2(有机层)+2H+(水层)。①与萃取剂Cyanex272(磷酸酯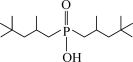 )相比,芳香基磷酸酯更适合高酸度废水中Co2+的萃取,原因是
)相比,芳香基磷酸酯更适合高酸度废水中Co2+的萃取,原因是

您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】根据下列实验,总结苯的某些性质。
(1)向试管中加入 苯,再加入
苯,再加入 溴水,振荡后静置。观察到的现象是
溴水,振荡后静置。观察到的现象是________________________ 。
(2)向试管中加入 苯,再加入
苯,再加入 酸性高锰酸钾溶液,振荡后静置。观察到的现象是
酸性高锰酸钾溶液,振荡后静置。观察到的现象是_________________________________________________________________________________________ 。
(3)实验结论:苯________ (填“能”或“不能”)与溴水和酸性高锰酸钾溶液发生反应。
(4)根据上述实验结论可知:苯分子中________ (填“存在”或“不存在”)碳碳双键。
(1)向试管中加入
 苯,再加入
苯,再加入 溴水,振荡后静置。观察到的现象是
溴水,振荡后静置。观察到的现象是(2)向试管中加入
 苯,再加入
苯,再加入 酸性高锰酸钾溶液,振荡后静置。观察到的现象是
酸性高锰酸钾溶液,振荡后静置。观察到的现象是(3)实验结论:苯
(4)根据上述实验结论可知:苯分子中
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】以下是用苯作原料制备一系列化合物的转化关系图:
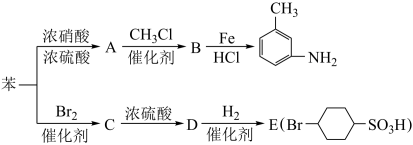
已知: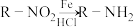
(1)生成A的化学方程式是___________
(2)B中的所有原子___________ (填“是”或“不是”)在同一平面上。
(3)生成C过程中的另一种无机产物是___________ 。
(4)D与氢气的反应类型为___________ 。
(5)E的环上一氯代物有___________ 种。

已知:
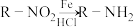
(1)生成A的化学方程式是
(2)B中的所有原子
(3)生成C过程中的另一种无机产物是
(4)D与氢气的反应类型为
(5)E的环上一氯代物有
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】中国科学院动物研究所康乐院士团队在《自然》上发表了一项揭示蝗虫聚群成灾奥秘的研究成果,发现了一种蝗虫群聚信息素分子4VA(4-乙烯基苯甲醚)。这项研究不仅揭示了蝗虫群居的奥秘,而且使蝗虫的绿色和可持续防控成为可能。4VA的一种合成路线如图。
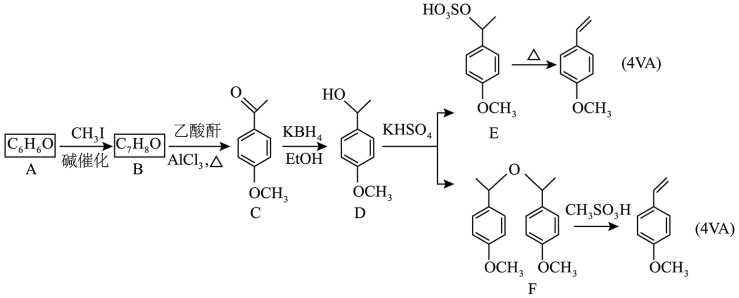
(1)B的结构简式为_______ ;C→D的反应类型为_______ 。
(2)乙酸酐的结构简式为(CH3CO)2O,则B→C的化学方程式为_______ 。
(3)C可以在催化剂、加热条件下与 发生加成反应生成D,对比合成路线中的反应条件,说明不选择
发生加成反应生成D,对比合成路线中的反应条件,说明不选择 的主要原因
的主要原因_______ 。
(4)C有多种同分异构体,其中能满足下列条件的芳香族化合物的结构简式为_______ 、_______ 。
①能发生银镜反应,也能发生水解反应,且水解后的产物之一能与 溶液发生显色反应;
溶液发生显色反应;
②核磁共振氢谱有四组峰,峰面积比为1:1:2:6。
(5)H(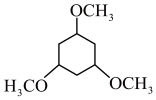 )是有机合成中重要的中间体,设计由1,3,5-三氯苯(
)是有机合成中重要的中间体,设计由1,3,5-三氯苯( )制备H的合成路线。(无机试剂和四个碳以下的有机试剂任选)
)制备H的合成路线。(无机试剂和四个碳以下的有机试剂任选)______ 。

(1)B的结构简式为
(2)乙酸酐的结构简式为(CH3CO)2O,则B→C的化学方程式为
(3)C可以在催化剂、加热条件下与
 发生加成反应生成D,对比合成路线中的反应条件,说明不选择
发生加成反应生成D,对比合成路线中的反应条件,说明不选择 的主要原因
的主要原因(4)C有多种同分异构体,其中能满足下列条件的芳香族化合物的结构简式为
①能发生银镜反应,也能发生水解反应,且水解后的产物之一能与
 溶液发生显色反应;
溶液发生显色反应;②核磁共振氢谱有四组峰,峰面积比为1:1:2:6。
(5)H(
 )是有机合成中重要的中间体,设计由1,3,5-三氯苯(
)是有机合成中重要的中间体,设计由1,3,5-三氯苯( )制备H的合成路线。(无机试剂和四个碳以下的有机试剂任选)
)制备H的合成路线。(无机试剂和四个碳以下的有机试剂任选)
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)下列说法不正确的是____ (填序号)。
①石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃
②煤干馏可以得到甲烷,苯和氨等重要化工原料
③75%(体积分数)的乙醇溶液常用于医疗消毒
④设NA为阿伏加德罗常数的值,0.1mol的-OH含有的电子数为NA
(2)已知:①
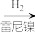
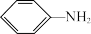 (易被氧化);
(易被氧化);
②羧基为间位定位基(当苯环上已有这类定位取代基时,再引入的其他基团主要进入它的间位)。
如图为以甲苯为原料经三步合成2,4,6-三氨基苯甲酸的路线:
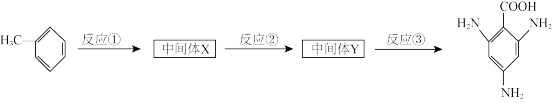
请分析:反应①的试剂和条件为____ ;中间体Y的结构简式为___ ;反应③的试剂和条件为____ 。
(1)下列说法不正确的是
①石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃
②煤干馏可以得到甲烷,苯和氨等重要化工原料
③75%(体积分数)的乙醇溶液常用于医疗消毒
④设NA为阿伏加德罗常数的值,0.1mol的-OH含有的电子数为NA
(2)已知:①

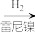
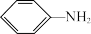 (易被氧化);
(易被氧化);②羧基为间位定位基(当苯环上已有这类定位取代基时,再引入的其他基团主要进入它的间位)。
如图为以甲苯为原料经三步合成2,4,6-三氨基苯甲酸的路线:
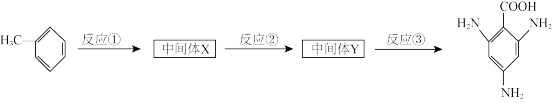
请分析:反应①的试剂和条件为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:
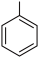 +KMnO4→
+KMnO4→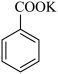 + MnO2
+ MnO2
 +HCl→
+HCl→ +KCl
+KCl
实验步骤:

(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 mol)高锰酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
(2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为1.0 g。
(3)纯度测定:称取0. 122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25. 00 mL溶液,用0.01000 mol·L−1的KOH标准溶液滴定,三次滴定平均消耗21. 50 mL的KOH标准溶液。
回答下列问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为______ (填标号)。
A.100 mL B.250 mL C.500 mL D.1000 mL
(2)当回流液不再出现油珠即可判断反应已完成,其判断理由是______ 。
(3)加入适量饱和亚硫酸氢钠溶液的目的是______ ;该步骤亦可用草酸在酸性条件下处理,请用反应的离子方程式表达其原理______ 。
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是______ 。
(5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是______ 。
(6)本实验制备的苯甲酸的纯度为______ ;据此估算本实验中苯甲酸的产率最接近于______ (填标号)。
A.70% B.60% C.50% D.40%
(7)若要得到纯度更高的苯甲酸,可通过在水中______ 的方法提纯。
 +KMnO4→
+KMnO4→ + MnO2
+ MnO2 +HCl→
+HCl→ +KCl
+KCl| 名称 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g·mL−1) | 溶解性 |
| 甲苯 | 92 | −95 | 110.6 | 0.867 | 不溶于水,易溶于乙醇 |
| 苯甲酸 | 122 | 122.4(100℃左右开始升华) | 248 | —— | 微溶于冷水,易溶于乙醇、热水 |

(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 mol)高锰酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
(2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为1.0 g。
(3)纯度测定:称取0. 122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25. 00 mL溶液,用0.01000 mol·L−1的KOH标准溶液滴定,三次滴定平均消耗21. 50 mL的KOH标准溶液。
回答下列问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为
A.100 mL B.250 mL C.500 mL D.1000 mL
(2)当回流液不再出现油珠即可判断反应已完成,其判断理由是
(3)加入适量饱和亚硫酸氢钠溶液的目的是
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是
(5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是
(6)本实验制备的苯甲酸的纯度为
A.70% B.60% C.50% D.40%
(7)若要得到纯度更高的苯甲酸,可通过在水中
您最近半年使用:0次

 ,其官能团的性质与一般链烃官能团性质相似,已知A具有下列性质:
,其官能团的性质与一般链烃官能团性质相似,已知A具有下列性质: ;
;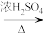 C
C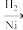
 ;
;

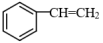 )与HBr发生生成A(
)与HBr发生生成A( )。同时生成一种副产物B,B与A互为同分异构体,则B为
)。同时生成一种副产物B,B与A互为同分异构体,则B为

