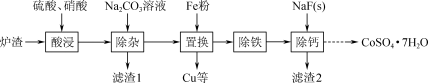
实验室从某废弃炉渣(含Cu、Ni、Co、Ca、Fe等金属及其氧化物)中回收Cu、Ni、Co,其部分实验过程如下:___________ (答2条即可)。
(2)将“置换”后溶液中的Fe2+氧化为Fe3+,控制pH可形成Na2Fe6(SO4)4(OH)12沉淀。写出该反应的离子方程式:___________ 。
(3)向“除铁”后的滤液中加入NaF,使Ca2+转化为CaF2沉淀除去。若溶液pH偏低,将会导致CaF2沉淀不完全,其原因是___________ 。[Ksp(CaF2)=5.3×10-9、Ka(HF)=6.3×10-4]
(4)“除钙”后的溶液经过萃取、反萃取等操作可分离钴和镍,其中萃取原理可表示为Co2+(水层)+2HA(有机层) CoA2(有机层)+2H+(水层)。
CoA2(有机层)+2H+(水层)。___________ (已知Co2+、Ni2+的萃取率与pH的关系曲线如图所示。实验中须使用的试剂有Cyanex272、H2SO4溶液、NaOH溶液)。
(2)将“置换”后溶液中的Fe2+氧化为Fe3+,控制pH可形成Na2Fe6(SO4)4(OH)12沉淀。写出该反应的离子方程式:
(3)向“除铁”后的滤液中加入NaF,使Ca2+转化为CaF2沉淀除去。若溶液pH偏低,将会导致CaF2沉淀不完全,其原因是
(4)“除钙”后的溶液经过萃取、反萃取等操作可分离钴和镍,其中萃取原理可表示为Co2+(水层)+2HA(有机层)
 CoA2(有机层)+2H+(水层)。
CoA2(有机层)+2H+(水层)。①与萃取剂Cyanex272(磷酸酯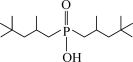 )相比,芳香基磷酸酯更适合高酸度废水中Co2+的萃取,原因是
)相比,芳香基磷酸酯更适合高酸度废水中Co2+的萃取,原因是

2024高三·全国·专题练习 查看更多[1]
(已下线)FHgkyldyjhx08
更新时间:2024-05-04 15:08:05
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】Ⅰ.学习有机化学,掌握有机物的组成、结构、命名和官能团性质是必备知识。
(1)请根据官能团的不同对下列有机物进行分类,把正确答案序号 填写在相应横线上。___________ ;醇:___________ ;羧酸:___________ 。
(2)下列说法中正确的是___________。
(3)苯环实际上不具有碳碳单键和双键的简单交替结构,可作为证据的事实有___________ 。
①苯的邻位二元取代物只有一种
②苯不能使KMnO4酸性溶液褪色
③苯分子中碳碳键的键长均相等(键长是指在分子中两个成键的核间距离)
(4)写出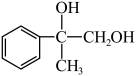 在铜催化作用下被氧气氧化的化学方程式:
在铜催化作用下被氧气氧化的化学方程式:___________ 。
Ⅱ.第四周期某些过渡元素在工业生产中有着极其重要的作用。
(5)铬(Cr)被称为“不锈钢的添加剂”。
①Cr位于元素周期表的___________ 区。
②基态Cr原子的价电子轨道 表示式___________ 。
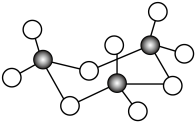
(6)钒(V)是我国的丰产元素,被誉为“工业的味精”,广泛用于催化及钢铁工业。V2O5常用作SO2转化为SO3的催化剂。SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型 为___________ 。
(1)请根据官能团的不同对下列有机物进行分类,把正确答案
①CH3CH=CH2 ②CH3CH2OH ③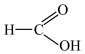 ④
④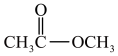 ⑤
⑤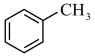 ⑥
⑥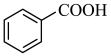
(2)下列说法中正确的是___________。
| A.乙醇、乙酸均能与Na反应放出H2 |
B.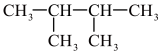 与 与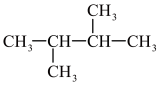 互为同分异构体 互为同分异构体 |
| C.相同物质的量的乙烯和乙醇完全燃烧消耗的氧气的量相同 |
| D.乙烯能使溴水和酸性KMnO4溶液褪色,两者的反应原理相同 |
(3)苯环实际上不具有碳碳单键和双键的简单交替结构,可作为证据的事实有
①苯的邻位二元取代物只有一种
②苯不能使KMnO4酸性溶液褪色
③苯分子中碳碳键的键长均相等(键长是指在分子中两个成键的核间距离)
(4)写出
 在铜催化作用下被氧气氧化的化学方程式:
在铜催化作用下被氧气氧化的化学方程式:Ⅱ.第四周期某些过渡元素在工业生产中有着极其重要的作用。
(5)铬(Cr)被称为“不锈钢的添加剂”。
①Cr位于元素周期表的
②基态Cr原子的
(6)钒(V)是我国的丰产元素,被誉为“工业的味精”,广泛用于催化及钢铁工业。V2O5常用作SO2转化为SO3的催化剂。SO3的三聚体环状结构如图所示,该结构中S原子的
您最近一年使用:0次
【推荐2】乙烯是石油化学工业最重要的基础原料。下图是乙烯制氯乙烯的简单流程图:

(1)乙烯的结构简式为_______ 。
(2)反应①的化学方程式为:_______ ;该反应属于_______ 反应。
(3)苯乙烯(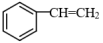 )与HBr发生生成A(
)与HBr发生生成A( )。同时生成一种副产物B,B与A互为同分异构体,则B为
)。同时生成一种副产物B,B与A互为同分异构体,则B为_______ 。
(4)乙烯可以使酸性高锰酸钾溶液褪色,而苯不可以,为什么_______ ?

(1)乙烯的结构简式为
(2)反应①的化学方程式为:
(3)苯乙烯(
 )与HBr发生生成A(
)与HBr发生生成A( )。同时生成一种副产物B,B与A互为同分异构体,则B为
)。同时生成一种副产物B,B与A互为同分异构体,则B为(4)乙烯可以使酸性高锰酸钾溶液褪色,而苯不可以,为什么
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】苯的分子结构
(1)分子式为_______ ,结构简式为 和
和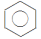 ,为
,为_______ 结构。
(2)化学键形成
苯分子中的6个碳原子均采取_______ 杂化,分别与氢原子及相邻碳原子以_______ 键结合,键间夹角均为120°,连接成六元环。每个碳碳键的键长相等,都是139 pm,介于______ 和______ 的键长之间。每个碳原子余下的_______ 轨道垂直于碳、氢原子构成的平面,相互平行重叠形成大_______ 键,均匀地对称分布在苯环平面的上下两侧。
(1)分子式为
 和
和 ,为
,为(2)化学键形成
苯分子中的6个碳原子均采取
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海水中蕴藏的元素高达80多种,是人类财富的重要集散地。如图是海水综合利用的示意图:

(1)实验室进行实验操作①中过滤所需要的玻璃仪器有烧杯、玻璃棒、______ 。
(2)除去粗盐溶液中杂质离子(Mg2+、 、Ca2+),加入的药品顺序不合理的是
、Ca2+),加入的药品顺序不合理的是_____ (填序号)。
a.NaOH→BaCl2→Na2CO3→盐酸
b.Na2CO3→NaOH→BaCl2→盐酸
c.BaCl2→NaOH→Na2CO3→盐酸
(3)电解饱和食盐水的化学方程式为______ 。
(4)“滤液(Br-)”中通Cl2,反应的离子方程式为______ 。
(5)操作③是“鼓入热空气”,利用了溴单质的______ 性。
(6)“精制”过程中,包含萃取、______ 、蒸馏等操作。
(7)Mg(OH)2和盐酸反应的离子方程式______ ;海水中c(Mg2+)=0.05mol•L-1,取10L海水实验,操作④中产生标准状况下8.96LCl2,则镁元素的提取率为______ %。

(1)实验室进行实验操作①中过滤所需要的玻璃仪器有烧杯、玻璃棒、
(2)除去粗盐溶液中杂质离子(Mg2+、
 、Ca2+),加入的药品顺序不合理的是
、Ca2+),加入的药品顺序不合理的是a.NaOH→BaCl2→Na2CO3→盐酸
b.Na2CO3→NaOH→BaCl2→盐酸
c.BaCl2→NaOH→Na2CO3→盐酸
(3)电解饱和食盐水的化学方程式为
(4)“滤液(Br-)”中通Cl2,反应的离子方程式为
(5)操作③是“鼓入热空气”,利用了溴单质的
(6)“精制”过程中,包含萃取、
(7)Mg(OH)2和盐酸反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:

(1)操作③可选用的有机试剂是________ (只填一种)。步骤②生成 的离子方程式
的离子方程式_______ 。
(2)操作过程③可以分解为如下几步:
A.将分液漏斗放在铁架台的铁圈中静置、分层;
B.把50.0 mL碘水和15.0mL所选有机溶剂加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.将漏斗上口玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准,旋开活塞,用烧杯接收液体;
F.从分液漏斗上口倒出上层液体;
(a)过程③正确操作步骤的顺序是(填编号字母)__________ ;
(b)上述E步操作中“将漏斗上口玻璃塞上的凹槽对准小孔”的目的是___________ 。

(1)操作③可选用的有机试剂是
 的离子方程式
的离子方程式(2)操作过程③可以分解为如下几步:
A.将分液漏斗放在铁架台的铁圈中静置、分层;
B.把50.0 mL碘水和15.0mL所选有机溶剂加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.将漏斗上口玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准,旋开活塞,用烧杯接收液体;
F.从分液漏斗上口倒出上层液体;
(a)过程③正确操作步骤的顺序是(填编号字母)
(b)上述E步操作中“将漏斗上口玻璃塞上的凹槽对准小孔”的目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】由铁铬合金(主要成分Cr、Fe,含少量Co、Ni等)可以制取Cr2O3、FeC2O4·2H2O和LiFePO4。实验流程如下:

(1)“酸溶”时应先向反应器中加入硫酸,再分批加入铬铁合金粉末,同时需保持强制通风。
①分批加入铬铁合金粉末并保持强制通风的原因是_______ 。
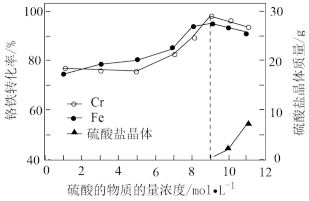
②其他条件相同,实验测得相同时间内铬铁转化率[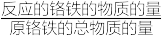 ×100%]、析出硫酸盐晶体的质量随硫酸浓度变化情况如图所示。当硫酸的浓度为9~11mol·L-1,铬铁转化率下降的原因:
×100%]、析出硫酸盐晶体的质量随硫酸浓度变化情况如图所示。当硫酸的浓度为9~11mol·L-1,铬铁转化率下降的原因:_______ 。(已知硫酸浓度大于12mol·L-1时铁才会钝化)
(2)向酸溶所得溶液中加入0.5mol·L-1Na2S溶液,使Co2+和Ni2+转化为CoS和NiS沉淀。当上层清液中c(Ni2+)=1.0×10-5mol·L-1时,c(Co2+)=_______ 。[已知:Ksp(CoS)=1.8×10-22,Ksp(NiS)=3.0×10-21]
(3)在N2的氛围中将FeC2O4·2H2O与LiH2PO4按物质的量之比1:1混合,360°C条件下反应可获得LiFePO4,同时有CO和CO2生成。写出该反应的化学方程式:_______ 。
(4)设计由沉铁后的滤液(含Cr3+和少量Fe2+)制备Cr2O3的实验方案:_______ ,过滤、洗涤、干燥、500°C煅烧。已知:①P507萃取剂密度小于水,萃取Fe3+时萃取率与溶液pH的关系如图所示。②该实验中Cr3+在pH6.0时开始沉淀,pH=8.0时沉淀完全。pH=12时Cr(OH)3开始溶解。实验中须选用试剂:P507萃取剂、H2O2、NaOH溶液]


(1)“酸溶”时应先向反应器中加入硫酸,再分批加入铬铁合金粉末,同时需保持强制通风。
①分批加入铬铁合金粉末并保持强制通风的原因是
②其他条件相同,实验测得相同时间内铬铁转化率[
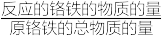 ×100%]、析出硫酸盐晶体的质量随硫酸浓度变化情况如图所示。当硫酸的浓度为9~11mol·L-1,铬铁转化率下降的原因:
×100%]、析出硫酸盐晶体的质量随硫酸浓度变化情况如图所示。当硫酸的浓度为9~11mol·L-1,铬铁转化率下降的原因:
(2)向酸溶所得溶液中加入0.5mol·L-1Na2S溶液,使Co2+和Ni2+转化为CoS和NiS沉淀。当上层清液中c(Ni2+)=1.0×10-5mol·L-1时,c(Co2+)=
(3)在N2的氛围中将FeC2O4·2H2O与LiH2PO4按物质的量之比1:1混合,360°C条件下反应可获得LiFePO4,同时有CO和CO2生成。写出该反应的化学方程式:
(4)设计由沉铁后的滤液(含Cr3+和少量Fe2+)制备Cr2O3的实验方案:

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】锗(Ge)是门捷列夫在1871年所预言的元素“亚硅”,高纯度的锗已经成为目前重要的半导体材料,其化合物在治疗癌症方面也有着独特的功效。下图是以锗锌矿(主要成分为GeO2、ZnS,另外含有少量的Fe2O3等)为主要原料生产高纯度锗的工艺流程:

已知:GeO2可溶于强碱溶液,生成锗酸盐。GeCl4的熔点为-49.5 ℃,沸点为84℃,在水中或酸的稀溶液中易水解。
(1)Ge基态价层电子排布式是___________ ,GeC14晶体所属类别是___________ 。
(2)步骤①NaOH溶液碱浸时发生的离子反应方程式为___________ 。
(3)步骤③沉锗过程中,当温度为90℃,pH为14时,加料量(CaC12/Ge质量比)对沉锗的影响如表所示,选择最佳加料量为__________ (填“10-15”“15-20”或“20-25”)。
(4)步骤⑤中选择浓盐酸而不选择稀盐酸的原因是___________ 。
(5)步骤⑥的化学反应方程式为___________ 。
(6)晶体Ge是优良的半导体,可作高频率电流的检波和交流电的整流用。如图为Ge单晶的晶胞,设Ge原子半径为r pm,其晶胞体对角线长度为8r pm,阿伏加德罗常数的值为NA,则该锗晶体的密度计算式为ρ=___________ g/cm3.(已知相对原子盘:Ge 73) (不需化简)


已知:GeO2可溶于强碱溶液,生成锗酸盐。GeCl4的熔点为-49.5 ℃,沸点为84℃,在水中或酸的稀溶液中易水解。
(1)Ge基态价层电子排布式是
(2)步骤①NaOH溶液碱浸时发生的离子反应方程式为
(3)步骤③沉锗过程中,当温度为90℃,pH为14时,加料量(CaC12/Ge质量比)对沉锗的影响如表所示,选择最佳加料量为
| 编号 | 加料量(CaC12/Ge ) | 母液体积/mL | 过滤后滤液含锗(mg/L) | 过滤后滤液pH | 锗沉淀率 (%) |
| 1 | 10 | 500 | 76 | 8 | 93.67 |
| 2 | 15 | 500 | 20 | 8 | 98.15 |
| 3 | 20 | 500 | 2 | 11 | 99.78 |
| 4 | 25 | 500 | 1.5 | 12 | 99.85 |
(4)步骤⑤中选择浓盐酸而不选择稀盐酸的原因是
(5)步骤⑥的化学反应方程式为
(6)晶体Ge是优良的半导体,可作高频率电流的检波和交流电的整流用。如图为Ge单晶的晶胞,设Ge原子半径为r pm,其晶胞体对角线长度为8r pm,阿伏加德罗常数的值为NA,则该锗晶体的密度计算式为ρ=

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】重晶石矿的主要成分为硫酸钡,纯净的硫酸钡才能供医用作“钡餐”,在对某些内脏器官进行X 射线透视时服用。硫化钡是可溶于水的盐。讨论用重晶石矿制硫酸钡,设计流程如下:
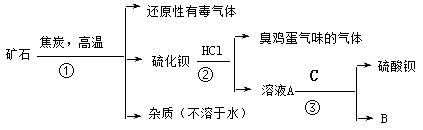
(1)写出步骤①的化学反应方程式___________ ,该反应产生的气体具有____ 、_____ 等用途。
(2)为进行②反应先要分离出硫化钡溶液,采用的方法是__________ 。在此之前要在溶液中滴入少量Ba(OH)2溶液,其作用是___________ 。
(3)若B物质在该生产过程中可循环使用,则③反应的化学方程式是:___________ 。
(4)有人提出②反应产生了有臭有毒的气体,可采用改变反应物的方法使无该气体产生,则②反应的化学方程式是:__________________________ 。
此时若要B物质还能循环使用,则C为__________ (写化学式)。
(5)BaSO4是因为具有_________ 、_________ 等性质而可用作“钡餐”的。

(1)写出步骤①的化学反应方程式
(2)为进行②反应先要分离出硫化钡溶液,采用的方法是
(3)若B物质在该生产过程中可循环使用,则③反应的化学方程式是:
(4)有人提出②反应产生了有臭有毒的气体,可采用改变反应物的方法使无该气体产生,则②反应的化学方程式是:
此时若要B物质还能循环使用,则C为
(5)BaSO4是因为具有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】Ⅰ、元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、 (绿色)、
(绿色)、 (橙红色)、
(橙红色)、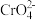 (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是_________ 。
(2)+6价铬的化合物毒性较大,常用NaHSO3将酸性废液中的 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为______________ 。
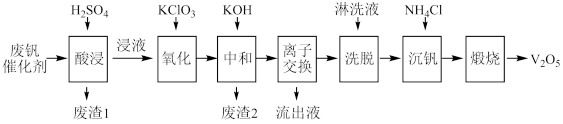
Ⅱ、以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
以下是一种废钒催化剂回收工艺路线:
(3)“酸浸”时V2O5转化为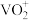 ,反应的离子方程式为
,反应的离子方程式为___________
(4)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________ 。
III、氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有Fe(Ⅱ), Mn(Ⅱ), Ni(Ⅱ)等杂质)的流程如下:
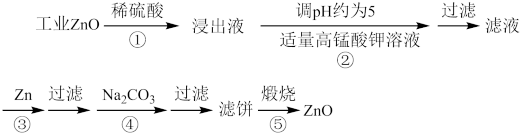
(5)在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2,回答下列问题:
反应②中发生反应的离子方程式为___________ ,___________ 。
 (绿色)、
(绿色)、 (橙红色)、
(橙红色)、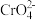 (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:(1)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是
(2)+6价铬的化合物毒性较大,常用NaHSO3将酸性废液中的
 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为Ⅱ、以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:

(3)“酸浸”时V2O5转化为
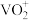 ,反应的离子方程式为
,反应的离子方程式为(4)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式
III、氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有Fe(Ⅱ), Mn(Ⅱ), Ni(Ⅱ)等杂质)的流程如下:

(5)在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2,回答下列问题:
反应②中发生反应的离子方程式为
您最近一年使用:0次



