Ⅰ.学习有机化学,掌握有机物的组成、结构、命名和官能团性质是必备知识。
(1)请根据官能团的不同对下列有机物进行分类,把正确答案序号 填写在相应横线上。___________ ;醇:___________ ;羧酸:___________ 。
(2)下列说法中正确的是___________。
(3)苯环实际上不具有碳碳单键和双键的简单交替结构,可作为证据的事实有___________ 。
①苯的邻位二元取代物只有一种
②苯不能使KMnO4酸性溶液褪色
③苯分子中碳碳键的键长均相等(键长是指在分子中两个成键的核间距离)
(4)写出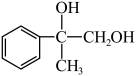 在铜催化作用下被氧气氧化的化学方程式:
在铜催化作用下被氧气氧化的化学方程式:___________ 。
Ⅱ.第四周期某些过渡元素在工业生产中有着极其重要的作用。
(5)铬(Cr)被称为“不锈钢的添加剂”。
①Cr位于元素周期表的___________ 区。
②基态Cr原子的价电子轨道 表示式___________ 。
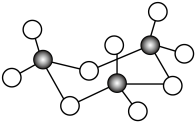
(6)钒(V)是我国的丰产元素,被誉为“工业的味精”,广泛用于催化及钢铁工业。V2O5常用作SO2转化为SO3的催化剂。SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型 为___________ 。
(1)请根据官能团的不同对下列有机物进行分类,把正确答案
①CH3CH=CH2 ②CH3CH2OH ③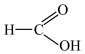 ④
④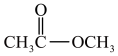 ⑤
⑤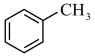 ⑥
⑥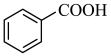
(2)下列说法中正确的是___________。
| A.乙醇、乙酸均能与Na反应放出H2 |
B.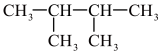 与 与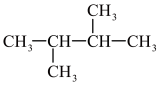 互为同分异构体 互为同分异构体 |
| C.相同物质的量的乙烯和乙醇完全燃烧消耗的氧气的量相同 |
| D.乙烯能使溴水和酸性KMnO4溶液褪色,两者的反应原理相同 |
(3)苯环实际上不具有碳碳单键和双键的简单交替结构,可作为证据的事实有
①苯的邻位二元取代物只有一种
②苯不能使KMnO4酸性溶液褪色
③苯分子中碳碳键的键长均相等(键长是指在分子中两个成键的核间距离)
(4)写出
 在铜催化作用下被氧气氧化的化学方程式:
在铜催化作用下被氧气氧化的化学方程式:Ⅱ.第四周期某些过渡元素在工业生产中有着极其重要的作用。
(5)铬(Cr)被称为“不锈钢的添加剂”。
①Cr位于元素周期表的
②基态Cr原子的
(6)钒(V)是我国的丰产元素,被誉为“工业的味精”,广泛用于催化及钢铁工业。V2O5常用作SO2转化为SO3的催化剂。SO3的三聚体环状结构如图所示,该结构中S原子的
更新时间:2024-04-28 11:07:59
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】近年科学家提出“绿色自由”构想。把含有大量 的空气吹入
的空气吹入 溶液中,再把
溶液中,再把 从溶液中提取出来,并使之与
从溶液中提取出来,并使之与 反应生成可再生能源甲醇(
反应生成可再生能源甲醇( )。其工艺流程如图所示:
)。其工艺流程如图所示:

(1)甲醇具有的官能团是_______ 。
(2)在吸收池中,发生的反应的化学方程式为_______ 。
(3)在合成塔中的反应条件下,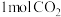 参与反应生成
参与反应生成 ,转移的电子的物质的量为
,转移的电子的物质的量为_______  。
。
 的空气吹入
的空气吹入 溶液中,再把
溶液中,再把 从溶液中提取出来,并使之与
从溶液中提取出来,并使之与 反应生成可再生能源甲醇(
反应生成可再生能源甲醇( )。其工艺流程如图所示:
)。其工艺流程如图所示:
(1)甲醇具有的官能团是
(2)在吸收池中,发生的反应的化学方程式为
(3)在合成塔中的反应条件下,
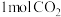 参与反应生成
参与反应生成 ,转移的电子的物质的量为
,转移的电子的物质的量为 。
。
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】芳香族化合物A是一种生产化妆品的原料,分子式为C9H8O2。
(1)为探究其结构,某同学设计并进行如下实验。
(2)已知A是苯的一取代物,其可能的结构简式为___________ 。
(3)A可用来合成肉桂酸甲酯D等有机物,其合成信息如下。

①根据信息确认A的结构,A→B反应的化学方程式为_________ 。
②已知D为由两分子C反应形成的包含三个六元环的酯。C→D反应的化学方程式为_________ 。
③ C生成D的过程中会有另一种高聚物副产物产生,其结构简式为_________ 。
(1)为探究其结构,某同学设计并进行如下实验。
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量待测液,加入一定量浓溴水 | 溴水褪色,无白色沉淀产生 | 不含有 |
| ②取一定量待测液,向内加入NaHCO3溶液 | 有气泡产生 | 含有 |
(3)A可用来合成肉桂酸甲酯D等有机物,其合成信息如下。

①根据信息确认A的结构,A→B反应的化学方程式为
②已知D为由两分子C反应形成的包含三个六元环的酯。C→D反应的化学方程式为
③ C生成D的过程中会有另一种高聚物副产物产生,其结构简式为
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】D是一种香料,常以A(C5H12O)为原料按如图流程合成:回答下列问题:

(1)A中所含官能团的名称是_______ 。
(2)A→B的反应条件是_______ 。
(3)A分子中含有3个甲基,则B的结构简式是_______ ;A+C→D的化学方程式是_______ 。
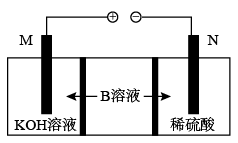
(4)将B溶液按如图所示装置进行电解,生成C对应的钾盐和A.该装置工作时,C对应的钾盐在_______ 极(填“M”或“N”)生成,N极的电极反应式为_______ 。

(1)A中所含官能团的名称是
(2)A→B的反应条件是
(3)A分子中含有3个甲基,则B的结构简式是
(4)将B溶液按如图所示装置进行电解,生成C对应的钾盐和A.该装置工作时,C对应的钾盐在

您最近半年使用:0次
【推荐1】甲、乙、丙、丁分别是甲烷、乙烯、丙烯(CH3—CH===CH2)、苯中的一种;
(1)甲、乙能使溴水褪色,甲分子中所有原子共平面,但乙分子不是所有原子共平面。
(2)丙既不能使Br2的CCl4溶液褪色,也不能使酸性KMnO4溶液褪色。
(3)丁既不能使Br2的CCl4溶液褪色,也不能使酸性KMnO4溶液褪色,但在一定条件下可与液溴发生取代反应。一定条件下,1 mol丁可以和3 mol H2完全加成。
请根据以上叙述完成下列填空:
(1)甲的结构简式________ ,乙的名称________ ,丙是________ 结构。
(2)丁与H2在催化剂作用下发生加成反应的化学方程式____________________ 。
(1)甲、乙能使溴水褪色,甲分子中所有原子共平面,但乙分子不是所有原子共平面。
(2)丙既不能使Br2的CCl4溶液褪色,也不能使酸性KMnO4溶液褪色。
(3)丁既不能使Br2的CCl4溶液褪色,也不能使酸性KMnO4溶液褪色,但在一定条件下可与液溴发生取代反应。一定条件下,1 mol丁可以和3 mol H2完全加成。
请根据以上叙述完成下列填空:
(1)甲的结构简式
(2)丁与H2在催化剂作用下发生加成反应的化学方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】德国化学家凯库勒认为:苯分子是由6个碳原子以单双键相互交替结合而成的环状结构,为了验证凯库勒有关苯环的观点,甲同学设计了如图实验方案。

①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题。
(1)A中所发生反应的反应方程式为_____ ,能证明凯库勒观点错误的实验现象是_____ 。
(2)装置B的作用是_________ 。
(3)C中烧瓶的容器为500 mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对H2的相对密度为37.9,那么实验结束时,可计算进入烧瓶中的水的体积为_______ mL。(空气的平均相对分子质量为29)
(4)已知乳酸的结构简式为: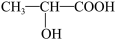 。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:
。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:______ 。

①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题。
(1)A中所发生反应的反应方程式为
(2)装置B的作用是
(3)C中烧瓶的容器为500 mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对H2的相对密度为37.9,那么实验结束时,可计算进入烧瓶中的水的体积为
(4)已知乳酸的结构简式为:
 。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:
。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】甲、乙、丙、丁分别是乙烷、乙烯、乙炔、苯中的一种;
①甲、乙能使溴的四氯化碳溶液褪色。乙与等物质的量的H2反应生成甲,甲与等物质的量的H2反应生成丙。
②丙既不能使溴的四氯化碳溶液褪色,也不能使KMnO4酸性溶液褪色。
③丁能使溴水褪色的原因与甲能使溴水褪色的原因不同,丁也不能使KMnO4酸性溶液褪色,但丁在一定条件下可与溴发生取代反应。相同条件下,丁蒸气的密度是乙密度的3倍。
据以上叙述完成下列问题:
(1)写出甲的结构简式__________ 、乙的结构式____________ 、丙分子中含有的化学键类型是__________ ;
(2)写出丁与液溴在催化剂作用下发生取代反应的方程式_________________ ;
(3)写出甲使溴的四氯化碳溶液褪色的化学方程式_______________________ 。
①甲、乙能使溴的四氯化碳溶液褪色。乙与等物质的量的H2反应生成甲,甲与等物质的量的H2反应生成丙。
②丙既不能使溴的四氯化碳溶液褪色,也不能使KMnO4酸性溶液褪色。
③丁能使溴水褪色的原因与甲能使溴水褪色的原因不同,丁也不能使KMnO4酸性溶液褪色,但丁在一定条件下可与溴发生取代反应。相同条件下,丁蒸气的密度是乙密度的3倍。
据以上叙述完成下列问题:
(1)写出甲的结构简式
(2)写出丁与液溴在催化剂作用下发生取代反应的方程式
(3)写出甲使溴的四氯化碳溶液褪色的化学方程式
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】分别取1 molA、B、C、D、E、F六种有机物,使它们充分燃烧,都生成44.8LCO2(标况),D和E是碳、氢、氧的化合物,两者互为同分异构体,E被氧化成A,A继续氧化成B,C、F都能发生加聚反应,C和氯化氢加成生成F。试推断有机化合物A、B、C、D、E、F的结构简式。
(1)A.______ 、B.______ 、C.______ 、D.______ 、E.______ 、F.______ 。
(2)写出下列反应的化学方程式
E→A:_________________________________________ 。
实验室制备C:__________________________________ 。
(1)A.
(2)写出下列反应的化学方程式
E→A:
实验室制备C:
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
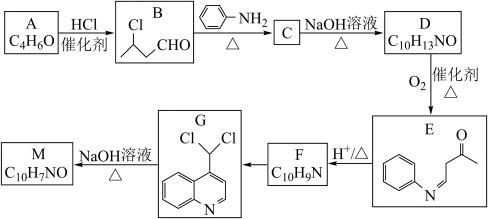
【推荐2】化合物M是一种医药中间体,实验室中M的一种合成路线如下:
回答下列问题:
(1)A中官能团的名称为______ ;B的化学名称为______ ;由C生成D的反应类型为______ 。
(2)F的结构简式为______ ;由F生成G 化学方程式为______ 。
(3)由G生成M的化学方程式为______ 。
(4)Q为D的同分异构体,同时满足下列条件的Q的所有结构简式有______ 种(不含立体异构)。
①苯环上连有5个取代基;
②既含-NH2,又能与银氨溶液发生银镜反应。
(5)参照上述合成路线和信息,以2-丙醇和苯为原料(无机试剂任选),设计制备 的合成路线
的合成路线______ 。
已知:①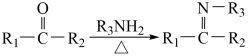
②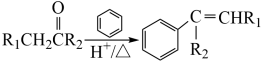
回答下列问题:
(1)A中官能团的名称为
(2)F的结构简式为
(3)由G生成M的化学方程式为
(4)Q为D的同分异构体,同时满足下列条件的Q的所有结构简式有
①苯环上连有5个取代基;
②既含-NH2,又能与银氨溶液发生银镜反应。
(5)参照上述合成路线和信息,以2-丙醇和苯为原料(无机试剂任选),设计制备
 的合成路线
的合成路线
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】温室气体CO2资源化利用的一种途径如下,生成物H和I可用作锂离子电池的电解质。___________ ,它的芳香同分异构体中,核磁共振氢谱为四组峰,峰面积比为 的结构简式为
的结构简式为___________ (写一种)。
(2)根据化合物E的结构特征,分析预测其可能的化学性质,完成下表。
(3)A与x反应生成B,该反应的原子利用率为100%,x为___________ 。
(4)C到D反应的化学方程式为___________ 。
(5)下列有关说法正确的有___________。
(6)I中的手性碳原子有___________ 种。
(7)选用A的同系物和x为原料,参考上述信息,制备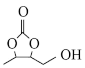 和
和 。写出该合成路线
。写出该合成路线___________ (无机试剂任选)。

 的结构简式为
的结构简式为(2)根据化合物E的结构特征,分析预测其可能的化学性质,完成下表。
| 序号 | 反应试剂、条件 | 反应形成的新结构 | 反应类型 |
| a |  、催化剂/ 、催化剂/ |  或 或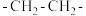 | 加成反应 |
| b | 氧化反应(生成有机产物) |
(4)C到D反应的化学方程式为
(5)下列有关说法正确的有___________。
| A.F到G的反应过程中,有C=C双键的断裂和C-O键的形成 |
| B.G到H的反应过程中,有C=O双键和C-O键的形成 |
| C.化合物E中的碳原子只有sp和sp2两种杂化方式,且不存在手性碳原子 |
| D.CO2属于非极性分子,其分子空间结构为直线型 |
(7)选用A的同系物和x为原料,参考上述信息,制备
 和
和 。写出该合成路线
。写出该合成路线
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的原子序数依次增大。A是宇宙中含量最丰富的元素,B、D原子的L层有2个未成对电子。E3+离子M层3d轨道电子为半满状态,F比E原子序数大1且位于同一族。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出F的价电子排布图_______ ,E位于周期表____ 区。
(2)B、C、D的电负性由小到大的顺序为___________ 。
(3)A、B、D三种元素可以形成组成为A2BD、A4BD、A2BD2的分子,其中B原子采取sp3 杂化的是_______ (填结构简式)
(4)F可形成分子式均为F(NH3)5BrSO4的两种配合物,往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时产生淡黄色沉淀,则这种配合物的化学式为_______
(5)B元素在自然界有多种同素异形体,硬度最大晶体中每个晶胞平均含有___ 个B原子。
(1)写出F的价电子排布图
(2)B、C、D的电负性由小到大的顺序为
(3)A、B、D三种元素可以形成组成为A2BD、A4BD、A2BD2的分子,其中B原子采取sp3 杂化的是
(4)F可形成分子式均为F(NH3)5BrSO4的两种配合物,往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时产生淡黄色沉淀,则这种配合物的化学式为
(5)B元素在自然界有多种同素异形体,硬度最大晶体中每个晶胞平均含有
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硼、铝、镓、铟等第ⅢA族元素及其化合物在材料化学、工业生产和生活中具有广泛的应用。回答下列问题:
(1)基态镓原子核外价电子排布图为___________ ;同周期主族元素基态原子与其具有相同数目未成对电子的有___________ 。
(2)氨硼烷(NH3BH3)是目前最具潜力的储氢材料之一、
①氨硼烷晶体中B原子的杂化方式为___________ 。
②氨硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键,用“N-H∙∙∙H-B”表示。以下物质之间可能形成双氢键的是___________ (填序号)。
a.N2H4和AlH3 b.C3H6和C2H6 c.B2H6和HCN
(3)氟化铝和氯化铝的熔点分别为1090℃和192.6℃,它们熔点差异很大的原因可能是___________ 。
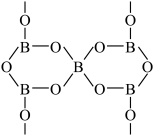
(4)硼酸盐常用于制作光学玻璃。一种无限网状结构的多聚硼酸根离子,其结构单元如图,若该硼酸根离子表示为(B5Ox)y-,则x=___________ ,y=___________ 。
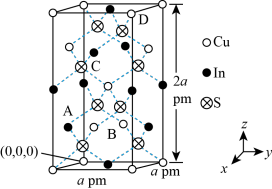
(5)太阳能材料CuInS2晶体为四方晶系,其晶胞参数及结构如图所示,晶胞棱边夹角均为90°。已知A处In原子坐标为(0.5,0,0.25),B处Cu原子坐标为(0,0.5,0.25)。
①C处S原子坐标为___________ 。
②设阿伏加德罗常数的值为NA,则该晶体密度为___________ g∙cm-3。(列出计算式即可)
(1)基态镓原子核外价电子排布图为
(2)氨硼烷(NH3BH3)是目前最具潜力的储氢材料之一、
①氨硼烷晶体中B原子的杂化方式为
②氨硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键,用“N-H∙∙∙H-B”表示。以下物质之间可能形成双氢键的是
a.N2H4和AlH3 b.C3H6和C2H6 c.B2H6和HCN
(3)氟化铝和氯化铝的熔点分别为1090℃和192.6℃,它们熔点差异很大的原因可能是
(4)硼酸盐常用于制作光学玻璃。一种无限网状结构的多聚硼酸根离子,其结构单元如图,若该硼酸根离子表示为(B5Ox)y-,则x=

(5)太阳能材料CuInS2晶体为四方晶系,其晶胞参数及结构如图所示,晶胞棱边夹角均为90°。已知A处In原子坐标为(0.5,0,0.25),B处Cu原子坐标为(0,0.5,0.25)。

①C处S原子坐标为
②设阿伏加德罗常数的值为NA,则该晶体密度为
您最近半年使用:0次
【推荐3】我国科学家研发Fe2O3/C3N4催化剂设计锂氧电池。请回答下列问题:
(1)Fe2O3中基态铁离子的价层电子排布图为___________ 。
(2)基态O原子核外电子云轮廓图为哑铃形的原子轨道上占据___________ 个电子。
(3)C3N4晶体的熔点为3550℃,耐磨,它的晶体类型是___________ 。
(4)我国科学家利用足球烯成功制备次晶金刚石,金刚石中C原子杂化类型为___________ 。石墨晶体层与层之间以___________ 结合。
(5)某新型材料碳化铁的晶胞如图所示。

①1个铁原子与___________ 个铁原子最近且等距离。
②该晶胞有___________ 个碳原子。
③每个晶胞中由铁原子形成的正四面体空隙有___________ 个。
(1)Fe2O3中基态铁离子的价层电子排布图为
(2)基态O原子核外电子云轮廓图为哑铃形的原子轨道上占据
(3)C3N4晶体的熔点为3550℃,耐磨,它的晶体类型是
(4)我国科学家利用足球烯成功制备次晶金刚石,金刚石中C原子杂化类型为
(5)某新型材料碳化铁的晶胞如图所示。

①1个铁原子与
②该晶胞有
③每个晶胞中由铁原子形成的正四面体空隙有
您最近半年使用:0次



