下列离子组能大量共存且加入(或通入)少量试剂发生的离子反应方程式正确的是
| 选项 | 离子组 | 试剂 | 离子方程式 |
| A | 新制氯水中: 、 、 、 、 、 、 | KI |  |
| B | 无色溶液中: 、 、 、 、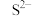 、 、 | 硫酸 | 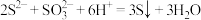 |
| C | 25℃水电离 的水溶液中: 的水溶液中: 、 、 、 、 、 、 | KOH |  |
| D | NaClO溶液中: 、 、 、 、 、 、 |  | 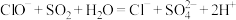 |
| A.A | B.B | C.C | D.D |
更新时间:2023-06-26 21:28:29
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式正确的是
A.小苏打中加入过量的澄清石灰水:Ca2++2OH-+2HCO =CaCO3↓+2H2O+CO =CaCO3↓+2H2O+CO |
| B.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ |
C.铜与浓硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO +6H++2MnO +6H++2MnO =5SO =5SO +2Mn2++3H2O +2Mn2++3H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列离子方程式与所述事实相符且正确的是
| A.H218O中投入Na2O2固体:2H218O+ 2O22-=4OH-+18O2↑ |
| B.用双氧水和稀硫酸处理铜板:Cu+H2O2+2H+=Cu2++2H2O |
| C.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
| D.铵明矾[AlNH4(SO4)2·12H2O]溶液中加入过量氢氧化钡溶液:Al3++NH4++2SO42-+2Ba2++5OH-= AlO2-+2BaSO4↓+NH3·H2O+2H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】某溶液仅由Na+、K+、Ba2+、Fe3+、 、
、 、Cl-中的若干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:
、Cl-中的若干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:
①加过量盐酸无明显变化,得到无色溶液;
②取操作①后的溶液,加入过量的Ba(OH)2,产生白色沉淀1;
③取操作②后的滤液,加入过量的HNO3和AgNO3溶液,产生白色沉淀2;
根据以上实验判断,下列推断错误的是
 、
、 、Cl-中的若干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:
、Cl-中的若干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:①加过量盐酸无明显变化,得到无色溶液;
②取操作①后的溶液,加入过量的Ba(OH)2,产生白色沉淀1;
③取操作②后的滤液,加入过量的HNO3和AgNO3溶液,产生白色沉淀2;
根据以上实验判断,下列推断错误的是
A.根据操作①现象,推断一定不存在CO |
| B.原溶液中一定存在Na+和K+ |
| C.白色沉淀2是AgNO3 |
| D.原溶液中可能存在Cl- |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列关于离子共存或离子反应的说法正确的是
A.某无色溶液中可能大量存在: 、 、 、 、 |
B.能与 反应能放出 反应能放出 的溶液中可能大量存在: 的溶液中可能大量存在: 、 、 、 、 、 、 |
C. 与 与 在酸性溶液中的反应: 在酸性溶液中的反应: |
D.稀硫酸与 溶液的反应: 溶液的反应: |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】为探究SO2与Fe3+能否发生氧化还原反应,按如图装置进行实验(夹持、加热仪器略),下列说法正确的是


| A.铜和浓硫酸反应需要加热的原因是低温下铜被钝化 |
| B.试剂a为饱和NaHSO3溶液,其作用是观察气流速率 |
| C.一段时间,向C中滴加氯化钡溶液,产生白色沉淀,说明Fe3+氧化了SO2 |
| D.一段时间,向C中滴加酸性高锰酸钾,溶液褪色,说明SO2还原了Fe3+ |
您最近一年使用:0次
多选题
|
适中
(0.65)
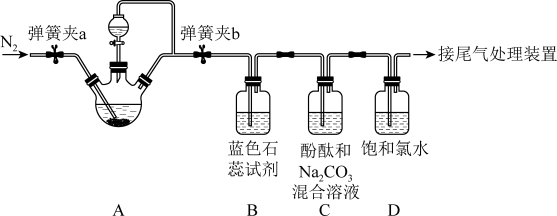
【推荐2】某学习小组设计制取 并验证其部分性质的实验装置图如下(夹持装置省略),下列说法错误的是
并验证其部分性质的实验装置图如下(夹持装置省略),下列说法错误的是
 并验证其部分性质的实验装置图如下(夹持装置省略),下列说法错误的是
并验证其部分性质的实验装置图如下(夹持装置省略),下列说法错误的是
A.A中固体物质是 ,A中发生的反应属于氧化还原反应 ,A中发生的反应属于氧化还原反应 |
| B.滴入浓硫酸前先通入氮气,防止空气中的氧气影响二氧化硫性质的检验 |
C.B装置溶液变红色,说明 是酸性氧化物;C装置中溶液红色褪去,说明 是酸性氧化物;C装置中溶液红色褪去,说明 具有漂白性 具有漂白性 |
D.取反应后D溶液少许,滴入品红溶液,红色褪去;另取该反应后D溶液少许,滴加 溶液,产生白色沉淀,以上现象不能说明 溶液,产生白色沉淀,以上现象不能说明 具有还原性 具有还原性 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】下列实验方案设计中,能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 证明SO2具有还原性 | 将SO2气体通入到酸性KMnO4溶液中,溶液褪色 |
| B | 检验产物中是否含有CO2 | 将炽热的木炭与浓硝酸混合所得的气体先通入饱和NaHCO3溶液除去NO2,再通入澄清石灰水中,石灰水变浑浊 |
| C | 酸性:HClO<CH3COOH | 室温下,用pH计分别测定等物质的量浓度的NaClO溶液和CH3COONa溶液的pH |
| D | 酸性:H2SO3>H2CO3 | 通常情况下,将SO2和CO2分别通入水中制得饱和溶液,再用pH计测定pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】已知40℃时水的离子积常数为Kw。该温度下,将浓度为0.1 mol·L-1的一元酸HX与a mol·L-1的NaOH等体积混和,能说明该溶液一定呈中性的依据是
| A.a=0.1 | B.混和后溶液中pH=7 |
C.混和后溶液中,c(H+)=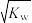 mol·L-1 mol·L-1 | D.混和后溶液中,c(Na+)=c(X-) |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】已知某弱酸的酸式盐有NaH2XO4和Na2HXO4,其中NaH2XO4的溶液呈酸性,Na2HXO4溶液呈碱性。30°C时,浓度均为0.1mol/LNaH2XO4溶液和Na2HXO4溶液中均存在的关系是
| A.c(H+)·c(OH-)>1×10-14 |
B.c(H+)+2c(H3XO4)+ c(H2XO )= c(XO )= c(XO )+ c(OH-) )+ c(OH-) |
C.c(H+)+ c(H3XO4)= c(HXO )+2c(XO )+2c(XO )+ c(OH-) )+ c(OH-) |
D.c(Na+)+ c(H+)= c(H2XO )+ c(OH-)+2c(HXO )+ c(OH-)+2c(HXO )+3c(XO )+3c(XO ) ) |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】某温度下的溶液中c(H+)=10xmol•L-1,c(OH-)=10ymol•L-1. 与
与 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是

 与
与 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是
| A.该温度高于25℃ |
| B.图中b点溶液呈碱性 |
| C.该温度下,若溶液中由水电离的c(H+)=10-9mol•L-1,则该溶液的pH=6或9 |
| D.该温度下,pH=13的NaOH溶液和pH=1的盐酸等体积混合后,溶液呈中性 |
您最近一年使用:0次

 CH3COO-+NH4++2Ag↓+3NH3+H2O
CH3COO-+NH4++2Ag↓+3NH3+H2O 、
、 、Fe2+、Mg2+
、Fe2+、Mg2+ 、Ca2+、Ba2+
、Ca2+、Ba2+ 、
、

