某小组同学利用下面的实验装置(气密性已检验,试管内预先充满氮气)验证硝酸的性质。
试填空:
(1)步骤i中,红棕色气体是___________ 。
(2)步骤ii中,浓硝酸被稀释成稀硝酸,能说明稀硝酸具有氧化性的现象是___________ 。
(3)步骤iii中,注射器中无色气体变为红棕色,发生反应的化学方程式为___________ 。
(4)上述实验能否证明铜与稀硝酸反应生成NO,并说明理由___________ 。
| 实验装置 | 实验步骤 | 实验现象 |
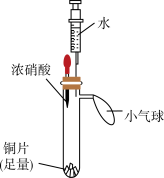 | i.挤压胶头,使浓硝酸滴入试管 | 产生红棕色气体,溶液变为绿色 |
| ii.一段时间后,推动注射器活塞,使水全部进入试管 | 铜片表面产生气泡,溶液变蓝,试管内气体逐渐变为无色 | |
| iii. 试管内气体变为无色后,拉动注射器活塞,吸取少量无色气体;拔下注射器,再拉动活塞吸入少量空气 | 注射器中无色气体变为红棕色 |
(1)步骤i中,红棕色气体是
(2)步骤ii中,浓硝酸被稀释成稀硝酸,能说明稀硝酸具有氧化性的现象是
(3)步骤iii中,注射器中无色气体变为红棕色,发生反应的化学方程式为
(4)上述实验能否证明铜与稀硝酸反应生成NO,并说明理由
更新时间:2023-06-27 08:47:21
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学学习小组采用下列装置对浓硝酸与木炭的反应进行探究。请回答下列问题:
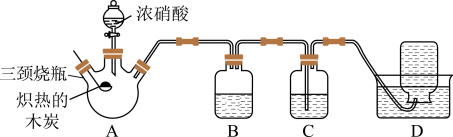
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,立即伸入三颈烧瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三颈烧瓶中气体的颜色为___________ ,产生该气体的反应的化学方程式是___________ 。
(2)装置C中盛有足量淀粉—KI溶液,反应一段时间后可观察到C中的现象为___________ 。
(3)装置B的作用是___________ 。
(4)装置D中收集到了无色气体,部分同学认为该气体是NO,还有部分同学认为是 。下列对该气体进行检验的方法合适的是
。下列对该气体进行检验的方法合适的是_______ (填字母)。
A.敞口观察集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
(5)用氢氧化钠溶液可以吸收氮氧化物,反应的化学方程式如下:
2NO2+2NO+4NaOH=4NaNO2+2H2O ①,
2NO2+2NaOH=NaNO2+NaNO3+H2O ②,
在反应①中,氧化剂是___________ ,还原剂是_______ 。在反应②中,氧化剂和还原剂的物质的量之比为___________ 。

(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,立即伸入三颈烧瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三颈烧瓶中气体的颜色为
(2)装置C中盛有足量淀粉—KI溶液,反应一段时间后可观察到C中的现象为
(3)装置B的作用是
(4)装置D中收集到了无色气体,部分同学认为该气体是NO,还有部分同学认为是
 。下列对该气体进行检验的方法合适的是
。下列对该气体进行检验的方法合适的是A.敞口观察集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
(5)用氢氧化钠溶液可以吸收氮氧化物,反应的化学方程式如下:
2NO2+2NO+4NaOH=4NaNO2+2H2O ①,
2NO2+2NaOH=NaNO2+NaNO3+H2O ②,
在反应①中,氧化剂是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】利用空气制取氨肥的流程如图所示。

回答下列问题:
(1)常压下,N2沸点-196℃,O2沸点-183℃。将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是_______ 。
(2)反应I中参加反应的单质甲的化学式为_______ 。
(3)反应II中反应的化学方程式为_______ 。
(4)用如图装置可模拟反应II实验。在锥形瓶中加入浓氨水,向其中鼓入氧气并迅速将烧红的铂丝伸入锥形瓶中并接近浓氨水的液面。铂丝锥形瓶内可观察到有红棕色气体生成,该气体的化学式是_______ 。锥形瓶内还有白烟( )产生,产生该现象的化学方程式为
)产生,产生该现象的化学方程式为_______ 。

(5)反应III的化学方程式为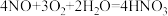 ,若有4.48LNO参与反应(标准状况),则反应中转移的电子数为
,若有4.48LNO参与反应(标准状况),则反应中转移的电子数为_______ 个。(用NA表示阿伏加德罗常数)
(6)判断下列说法是否正确,错误的请说明原因。
i.给农作物施铵态氮肥时,需将其埋在土中,因为铵盐受热易分解_______ 。
ii.给农作物施铵态氮肥时,与生石灰混用的效果更好_______ 。

回答下列问题:
(1)常压下,N2沸点-196℃,O2沸点-183℃。将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是
(2)反应I中参加反应的单质甲的化学式为
(3)反应II中反应的化学方程式为
(4)用如图装置可模拟反应II实验。在锥形瓶中加入浓氨水,向其中鼓入氧气并迅速将烧红的铂丝伸入锥形瓶中并接近浓氨水的液面。铂丝锥形瓶内可观察到有红棕色气体生成,该气体的化学式是
 )产生,产生该现象的化学方程式为
)产生,产生该现象的化学方程式为
(5)反应III的化学方程式为
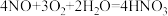 ,若有4.48LNO参与反应(标准状况),则反应中转移的电子数为
,若有4.48LNO参与反应(标准状况),则反应中转移的电子数为(6)判断下列说法是否正确,错误的请说明原因。
i.给农作物施铵态氮肥时,需将其埋在土中,因为铵盐受热易分解
ii.给农作物施铵态氮肥时,与生石灰混用的效果更好
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某研究性学习小组利用下图装置研究硝酸的性质。
Ⅰ实验一:甲同学用图1装置来证实稀硝酸与铜反应生成NO。

(1)请写出稀HNO3与Cu反应的离子方程式___ 。
(2)从A中向U形管中注满稀硝酸后,关闭A,待反应结束后,如何证明生成的无色气体气体是NO,操作是___ 。
(3)图2收集NO气体的各种装置中,合理的是___ (填序号,多选不给分)。
(4)在100mL混合溶液中,HNO3和H2SO4的物质的量浓度分别是0.4mol·L-1、0.2mol·L-1,向该混合液中加入2.56g铜粉,加热待充分反应后,所得溶液中Cu2+的物质的量浓度是___ 。
Ⅱ.实验二、乙组同学利用上述装置完成浓硝酸与铜的反应
(5)同学们发现实验室里有几瓶浓硝酸呈黄色,请用化学方程式和简单的文字说明解释这种现象___ 。
(6)同学们发现反应后的溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了NO2气体所致。同学们分别设计了以下4个实验来判断两种看法是否正确。
这些方案中可行的是___ (填序号,多选不给分)
①加热该绿色溶液,观察颜色变化
②加水稀释绿色溶液,观察颜色变化
③向该绿色溶液中通入氮气,观察颜色变化
④向饱和硝酸铜溶液中通入NO2气体,观察颜色变化
Ⅰ实验一:甲同学用图1装置来证实稀硝酸与铜反应生成NO。

(1)请写出稀HNO3与Cu反应的离子方程式
(2)从A中向U形管中注满稀硝酸后,关闭A,待反应结束后,如何证明生成的无色气体气体是NO,操作是
(3)图2收集NO气体的各种装置中,合理的是
(4)在100mL混合溶液中,HNO3和H2SO4的物质的量浓度分别是0.4mol·L-1、0.2mol·L-1,向该混合液中加入2.56g铜粉,加热待充分反应后,所得溶液中Cu2+的物质的量浓度是
Ⅱ.实验二、乙组同学利用上述装置完成浓硝酸与铜的反应
(5)同学们发现实验室里有几瓶浓硝酸呈黄色,请用化学方程式和简单的文字说明解释这种现象
(6)同学们发现反应后的溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了NO2气体所致。同学们分别设计了以下4个实验来判断两种看法是否正确。
这些方案中可行的是
①加热该绿色溶液,观察颜色变化
②加水稀释绿色溶液,观察颜色变化
③向该绿色溶液中通入氮气,观察颜色变化
④向饱和硝酸铜溶液中通入NO2气体,观察颜色变化
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素,A、B、C三种元素的原子序数之和为31,D元素与A、B、C三种元素既不同周期,也不同主族,请回答:
(1)C元素在元素周期表中的位置是_____________________________ ;
(2)A、B、D可组成一种离子化合物,是常见的化肥,其化学式为_________________ ;
(3)A2和D2两种物质可以构成一种新型的原电池,若原电池中电解质溶液为KOH溶液,则正极的电极反应式为_____________________________ ;
(4)若将一充满20 mlBA2和A2混合气体的大试管倒立于D2A中,充分反应后,在相同条件下,测得试管中余下5mL无色气体,则原混合气体中BA2和A2物质的量之比为________________ 。
(1)C元素在元素周期表中的位置是
(2)A、B、D可组成一种离子化合物,是常见的化肥,其化学式为
(3)A2和D2两种物质可以构成一种新型的原电池,若原电池中电解质溶液为KOH溶液,则正极的电极反应式为
(4)若将一充满20 mlBA2和A2混合气体的大试管倒立于D2A中,充分反应后,在相同条件下,测得试管中余下5mL无色气体,则原混合气体中BA2和A2物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】工业上通过氮气和氢气反应合成氨,氨经一系列反应可以得到硝酸。反应如下图所示:
(1)实验室制取氨气的化学方程式为___________ ;工业合成氨的化学方程式为___________ 。
(2) 与
与 制取
制取 的化学方程式为
的化学方程式为___________ 。
(3)下列说法正确的是(选填序号字母)___________。
(4)工业制硝酸时尾气中含有 、
、 ,可用以下方法吸收:
,可用以下方法吸收:
①水吸收法。结合化学用语说明用水吸收 的缺陷
的缺陷___________ 。
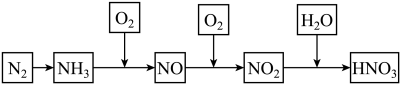
② 溶液吸收法。发生的反应有(均未配平):
溶液吸收法。发生的反应有(均未配平):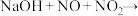
___________ (填化学式) 、
、
___________ (填化学式)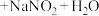 。
。
(1)实验室制取氨气的化学方程式为
(2)
 与
与 制取
制取 的化学方程式为
的化学方程式为(3)下列说法正确的是(选填序号字母)___________。
A. 排放到大气中会形成硝酸型酸雨, 排放到大气中会形成硝酸型酸雨, 的雨水称为酸雨 的雨水称为酸雨 |
| B.铵态氮肥一般不能与碱性化肥共同使用 |
| C.浓硝酸通常用无色试剂瓶保存 |
D.某浓硝酸中含有溶质2mol,标准状况下,该浓硝酸与足量的铜完全反应能生成1mol |
(4)工业制硝酸时尾气中含有
 、
、 ,可用以下方法吸收:
,可用以下方法吸收:①水吸收法。结合化学用语说明用水吸收
 的缺陷
的缺陷②
 溶液吸收法。发生的反应有(均未配平):
溶液吸收法。发生的反应有(均未配平):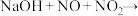
 、
、
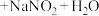 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】工业合成氨气的成功,解决了人类的重要的饥饿问题.我们在实验室中也常用NH4Cl和Ca(OH)2反应来制取一些氨气以便研究它的性质.请回答下列问题:
(1) 下图装置中能用于实验室制NH3的是____________ .
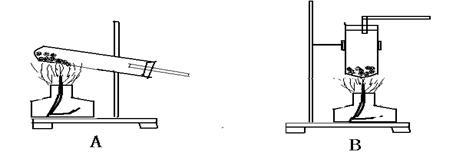
(2) 写出用NH4Cl和Ca(OH)2制取氨气的反应方程式:_______________ .
(3) 将湿润的红色石蕊试纸伸入充满氨气的试剂瓶中可以看到的现象是_______________ .
(4) NH3在工业上除作为制作化肥的原料外,也常用来制取硝酸,其主要步骤为:
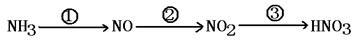
请写出下列反应的化学方程式:
NH3→ NO :_________________________ .
Cu和浓硝酸反应:__________________ .
(1) 下图装置中能用于实验室制NH3的是

(2) 写出用NH4Cl和Ca(OH)2制取氨气的反应方程式:
(3) 将湿润的红色石蕊试纸伸入充满氨气的试剂瓶中可以看到的现象是
(4) NH3在工业上除作为制作化肥的原料外,也常用来制取硝酸,其主要步骤为:
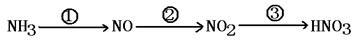
请写出下列反应的化学方程式:
NH3→ NO :
Cu和浓硝酸反应:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系。
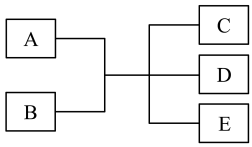
(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,则A为:______ B为:_____ (填化学式)
(2)若A是一种紫红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,反应的离子方程式是___________________ ,B在反应中表现出的性质是______ 、______ 。
(3)若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,则C为:________ D为:_________ (填化学式),实验室检验C的常用方法是___________________________ 。

(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,则A为:
(2)若A是一种紫红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,反应的离子方程式是
(3)若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,则C为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
Ⅰ.(1)实验室用金属铜和稀硝酸制取NO的离子方程式为
___________________________________________________ 。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________ (填选项编号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是____________________ (填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反就开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是___________________________________ 。
②让反应停止的操作方法及原因是________________________ 。

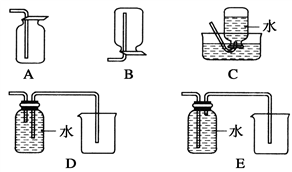
(4)以下收集NO气体的装置,合理的是________ (填选项代号)。
(5)假设实验中12.8 g Cu全部溶解,需要通入标况下________ mL O2才能使NO全部溶于水。
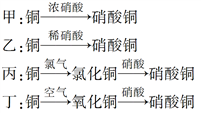
Ⅱ.用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________ (填“甲”、“乙”、“丙”或“丁”),理由是___________________________________________ 。
Ⅰ.(1)实验室用金属铜和稀硝酸制取NO的离子方程式为
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反就开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是
②让反应停止的操作方法及原因是

(4)以下收集NO气体的装置,合理的是
(5)假设实验中12.8 g Cu全部溶解,需要通入标况下
Ⅱ.用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下图中 、
、 、
、 为单质,其它为化合物,它们之间存在如下转化关系(部分产物已略去)。已知,
为单质,其它为化合物,它们之间存在如下转化关系(部分产物已略去)。已知, 溶液中滴加
溶液中滴加 溶液显血红色,
溶液显血红色, 单质是航空工业常用的金属材料。
单质是航空工业常用的金属材料。
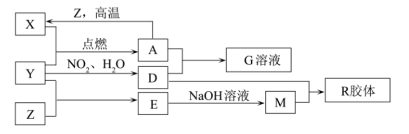
回答下列问题:
(1) 物质的化学式为
物质的化学式为_______ ,组成单质 的元素在周期表中的位置是
的元素在周期表中的位置是_______ 。
(2)一定条件下, 的氢化物与水反应的化学方程式为
的氢化物与水反应的化学方程式为_______ 。
(3) 和
和 的稀溶液反应的现象为
的稀溶液反应的现象为_______ 。
(4)标况下,将1L 和4L
和4L 混合充满于烧瓶中,再将烧瓶倒扣水槽中,最后水充满了烧瓶。则烧瓶中
混合充满于烧瓶中,再将烧瓶倒扣水槽中,最后水充满了烧瓶。则烧瓶中 的物质的量浓度为
的物质的量浓度为_______ 。
 、
、 、
、 为单质,其它为化合物,它们之间存在如下转化关系(部分产物已略去)。已知,
为单质,其它为化合物,它们之间存在如下转化关系(部分产物已略去)。已知, 溶液中滴加
溶液中滴加 溶液显血红色,
溶液显血红色, 单质是航空工业常用的金属材料。
单质是航空工业常用的金属材料。
回答下列问题:
(1)
 物质的化学式为
物质的化学式为 的元素在周期表中的位置是
的元素在周期表中的位置是(2)一定条件下,
 的氢化物与水反应的化学方程式为
的氢化物与水反应的化学方程式为(3)
 和
和 的稀溶液反应的现象为
的稀溶液反应的现象为(4)标况下,将1L
 和4L
和4L 混合充满于烧瓶中,再将烧瓶倒扣水槽中,最后水充满了烧瓶。则烧瓶中
混合充满于烧瓶中,再将烧瓶倒扣水槽中,最后水充满了烧瓶。则烧瓶中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学课外兴趣小组为探究铜与浓硫酸的反应,用如图所示的装置进行实验:

请回答下列问题:
(1)B是用于收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整_____ 。
(2)实验中他们取6.4g铜片和12mL18mol/L浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余。
①写出铜与浓硫酸反应的化学方程式:_____ ;
②实验中若有m g铜参加了反应,则有____ mol硫酸被还原,电子转移数目为______ 。
(3)为了测定消耗硫酸的物质的量,该兴趣小组设计了两个实验方案:
方案一:将装置A产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量,两次称量的质量差即是吸收二氧化硫的质量。
方案二:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化后生成硫酸钡沉淀的质量。
实际上,方案一、二均不可取。
方案一产生的气体中含有___ ,使干燥管增重偏大;也可能由于___ ,使干燥管增重偏小。
方案二:由于________ 与氯化钡溶液反应,使测定的结果偏大。

请回答下列问题:
(1)B是用于收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整
(2)实验中他们取6.4g铜片和12mL18mol/L浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余。
①写出铜与浓硫酸反应的化学方程式:
②实验中若有m g铜参加了反应,则有
(3)为了测定消耗硫酸的物质的量,该兴趣小组设计了两个实验方案:
方案一:将装置A产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量,两次称量的质量差即是吸收二氧化硫的质量。
方案二:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化后生成硫酸钡沉淀的质量。
实际上,方案一、二均不可取。
方案一产生的气体中含有
方案二:由于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某小组设计实验探究铜和浓硫酸的反应,装置如图所示。回答下列问题:
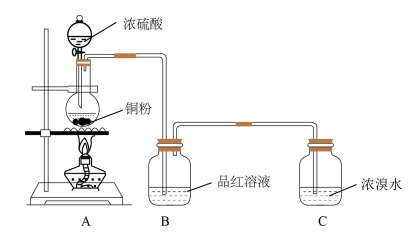
已知:CuS、 都是难溶于水、难溶于稀硫酸的黑色固体。实验中,铜粉完全反应后,观察到烧瓶底部有灰白带黑色固体。
都是难溶于水、难溶于稀硫酸的黑色固体。实验中,铜粉完全反应后,观察到烧瓶底部有灰白带黑色固体。
(1)B装置的作用是___________ ;Cu与浓硫酸反应时,体现了浓硫酸的___________ 性和___________ 性。
(2)C装置中浓溴水颜色变浅,则发生反应的离子方程式为___________ 。
(3)实验完毕后,分离A中烧瓶里的混合物并探究其成分:
将混合物倒入盛有水的烧杯中,搅拌,静置,过滤,得到蓝色溶液和黑色固体。
①黑色固体不可能是___________ (填标号),判断依据是___________ 。
A.CuS B. C.CuO
C.CuO
②探究该黑色固体成分。
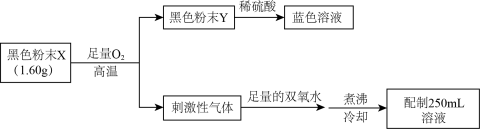
“配制250mL溶液时”需要使用的玻璃仪器有烧杯、量筒、玻璃棒和___________ ;取所配制的溶液25mL于锥形瓶中,加入20mL 的NaOH溶液恰好完全反应,则X是
的NaOH溶液恰好完全反应,则X是___________ (填化学式)。

已知:CuS、
 都是难溶于水、难溶于稀硫酸的黑色固体。实验中,铜粉完全反应后,观察到烧瓶底部有灰白带黑色固体。
都是难溶于水、难溶于稀硫酸的黑色固体。实验中,铜粉完全反应后,观察到烧瓶底部有灰白带黑色固体。(1)B装置的作用是
(2)C装置中浓溴水颜色变浅,则发生反应的离子方程式为
(3)实验完毕后,分离A中烧瓶里的混合物并探究其成分:
将混合物倒入盛有水的烧杯中,搅拌,静置,过滤,得到蓝色溶液和黑色固体。
①黑色固体不可能是
A.CuS B.
 C.CuO
C.CuO②探究该黑色固体成分。

“配制250mL溶液时”需要使用的玻璃仪器有烧杯、量筒、玻璃棒和
 的NaOH溶液恰好完全反应,则X是
的NaOH溶液恰好完全反应,则X是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某学习小组探究铜跟浓硫酸的反应时,利用如图实验装置进行相关实验。按要求填写下列空白:
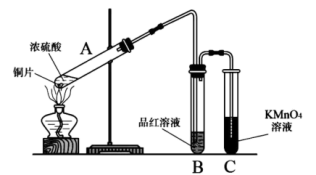
(1)装置A中发生的化学反应方程式为_______ 。
(2)实验过程中装置C中溶液褪色说明装置A中产生的气体具有_______ 性。
(3)实验结束拆开装置后,加热装置B的试管,观察到的现象是_______ 。
(4)实验结束后,发现试管A中底部出现了白色固体,设计实验方案检验该固体中含有CuSO4_______ 。
(5)将6.4 g铜片加入到盛有含0.2mol H2SO4的浓H2SO4试管中加热,充分反应后,铜片有剩余,原因是_______ 。

(1)装置A中发生的化学反应方程式为
(2)实验过程中装置C中溶液褪色说明装置A中产生的气体具有
(3)实验结束拆开装置后,加热装置B的试管,观察到的现象是
(4)实验结束后,发现试管A中底部出现了白色固体,设计实验方案检验该固体中含有CuSO4
(5)将6.4 g铜片加入到盛有含0.2mol H2SO4的浓H2SO4试管中加热,充分反应后,铜片有剩余,原因是
您最近一年使用:0次



