某学习小组研究影响锌与稀硫酸反应速率的外界因素,设计了如下对比实验:
反应速率最快的是
| 实验序号 | 锌的质量/g | 锌的状态 | 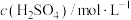 | 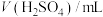 | 反应温度/℃ |
| ① | 3.25 | 粉末 | 0.8 | 50 | 20 |
| ② | 3.25 | 粉末 | 0.5 | 50 | 35 |
| ③ | 3.25 | 粉末 | 0.8 | 50 | 35 |
| ④ | 3.25 | 块状 | 0.8 | 50 | 35 |
| A.①组 | B.②组 | C.③组 | D.④组 |
20-21高一下·广东·期中 查看更多[3]
广东省普通高中2020-2021学年高一下学期教学质量联合测评化学试题(已下线)实验02 定性与定量研究影响化学反应速率的因素-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)6.2.1化学反应的速率-随堂练习
更新时间:2023-06-27 16:45:31
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列实验操作能达到相应实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 将铜片插入 溶液中 溶液中 | 比较 和 和 的活泼性 的活泼性 |
| B | 将相同的铁片分别加到等体积的稀硝酸和浓硝酸溶液中 | 探究浓度对化学反应速率的影响 |
| C | 将足量稀盐酸加到 溶液中 溶液中 | 比较 和 和 的非金属性强弱 的非金属性强弱 |
| D | 向盛有少量苯的试管中加入酸性 溶液 溶液 | 验证苯分子是否存在碳碳双键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用3g块状大理石与0.1mol/L盐酸反应制取CO2气体,下列措施不能提高反应速率的是
| A.将大理石研碎 | B.再加入少量块状大理石 |
| C.改用0.3mol/L盐酸 | D.适当升高温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究反应物浓度对化学反应速率的影响 | 分别取10mL 0.1mol·Lˉ1Na2S2O3溶液和5mL 0.1mol·Lˉ1Na2S2O3溶液、5mL蒸馏水于两支试管中,然后同时加入10mL 0.1mol·Lˉ1H2SO4溶液 | 前者出现浑浊的时间更短,说明增大Na2S2O3浓度,可以加快反应速率 |
| B | 探究压强对化学反应速率的影响 | 在容积不变的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),向其中通入氩气,反应速率不变 2NH3(g),向其中通入氩气,反应速率不变 | 化学反应速率不受压强影响 |
| C | 检验Fe(NO3)2晶体是否氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 | 若溶液变红,则Fe(NO3)2晶体已氧化变质 |
| D | 研究淀粉的水解程度 | 取0.5g淀粉于试管中,加入适量20%的硫酸溶液后沸水浴加热5min,再滴加过量氢氧化钠溶液,再加入适量碘水 | 若溶液没有变成蓝色,则淀粉已经水解完全 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】为了研究外界条件对H2O2分解反应速率的影响,某同学在相应条件下进行实验,实验记录如下表:
下列说法中错误的是
| 实验序号 | 反应物 | 温度/℃ | 催化剂 | 收集VmL气体所用时间/s |
① | 5mL5%H2O2溶液 | 25 | 2滴1mol/LFeCl3溶液 | t1 |
② | 5mL5%H2O2溶液 | 45 | 2滴1mol/LFeCl3溶液 | t2 |
③ | 5mL5%H2O2溶液 | b | 2滴1mol/LFeCl3溶液 | t3 |
④ | 5mL5%H2O2溶液 | 25 | 2滴蒸馏水 | t4 |
| A.表格中的数据:a=5,b= 25 |
| B.表格中的数据:t1>t4 |
| C.通过对比实验①②,可研究温度对反应速率的影响 |
| D.实验④加入2滴蒸馏水的目的是控制单一变量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】向两个锥形瓶中各加入0.05g镁条,塞紧橡胶塞,然后用注射器分别注入2mL2mol·L-1盐酸、2mL2mol·L-1醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法正确的是


| A.300s内平均反应速率v(HCl)=v(CH3COOH) |
| B.醋酸的平均反应速率呈现“慢—快”的趋势 |
| C.反应结束后锥形瓶中c(MgCl2)>c[(CH3COO)2Mg] |
| D.反应到100s时锥形瓶中c(HCl)=c(CH3COOH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】实验室以工业废渣(主要含CaSO4•2H2O,还含少量SiO2)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如图。下列说法正确的是
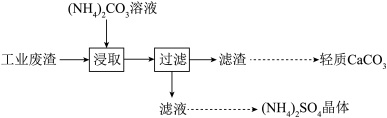

| A.为提高浸取效率,浸取时需在高温下进行 |
B.浸取时,需向(NH4)2CO3溶液中加入适量浓氨水,抑制 水解 水解 |
| C.滤渣经洗涤和干燥后得纯净的轻质CaCO3 |
| D.对滤液进行蒸发浓缩、冷却结晶可得到纯净的(NH4)2SO4晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】100 mL 6 mol·L-1的H2SO4跟过量锌粉反应,在一定温度下,要想加快反应进行的速率,但又不影响生成的氢气的总量,可向反应物中加入适量的
| A.适量浓H2SO4 | B.铜 | C.醋酸钠固体 | D.硝酸钾溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室利用废旧电池的铜帽(主要成分为Cu、Zn)制备CuSO4·5H2O的部分实验步骤如图:

下列说法不正确 的是

下列说法
| A.“溶解Ⅰ”中,为加快溶解速率,可将铜帽粉碎 |
| B.“滤液Ⅰ”中,溶质的主要成分为ZnSO4 |
| C.“溶解Ⅱ”过程中,有大量的气体产生 |
| D.“操作Ⅰ”是将溶液直接加热蒸干得到CuSO4·5H2O晶体 |
您最近一年使用:0次



