完成下列问题。
(1)Ba(OH)2溶液与NaHSO4溶液的反应:
①当反应后的溶液呈碱性时,反应的离子方程式为___________ 。
②当n[Ba(OH)2]∶n(NaHSO4)=1∶2时反应的离子方程式为___________ 。
(2)在富氧条件下,通过硝酸盐菌的作用,将氨氮(以 表示)氧化成硝酸盐的离子方程式为
表示)氧化成硝酸盐的离子方程式为________________ 。
(3)将过碳酸钠(2Na2CO3·3H2O2)溶于水配成溶液,加入适量稀硫酸,再加入足量KI,充分反应后加入少量淀粉试剂,溶液呈蓝色,该反应的离子方程式为___________ 。
(1)Ba(OH)2溶液与NaHSO4溶液的反应:
①当反应后的溶液呈碱性时,反应的离子方程式为
②当n[Ba(OH)2]∶n(NaHSO4)=1∶2时反应的离子方程式为
(2)在富氧条件下,通过硝酸盐菌的作用,将氨氮(以
 表示)氧化成硝酸盐的离子方程式为
表示)氧化成硝酸盐的离子方程式为(3)将过碳酸钠(2Na2CO3·3H2O2)溶于水配成溶液,加入适量稀硫酸,再加入足量KI,充分反应后加入少量淀粉试剂,溶液呈蓝色,该反应的离子方程式为
2023高三·全国·专题练习 查看更多[1]
(已下线)第2讲 离子反应 离子方程式
更新时间:2023-07-20 15:13:54
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】用化学方法除去下列物质中混有的少量杂质,其中括号内为杂质,写出除杂需加入的试剂(用化学式表示)以及发生反应的离子方程式。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式___ ;
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式____ ;
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式____ ;
(4)气体CO2(HCl)除杂发生反应的离子方程式___ 。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式
(4)气体CO2(HCl)除杂发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
(1)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是___________ 。
②上述物质中既不是电解质也不是非电解质的是___________ 。
③有下列三种物质: ;
; ;
; ;
;
a.写出上述物质中的盐在熔融状态下的电离方程式___________ ,
b.写出上述物质中的酸与氨水反应的离子方程式___________ 。
(2)在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来;
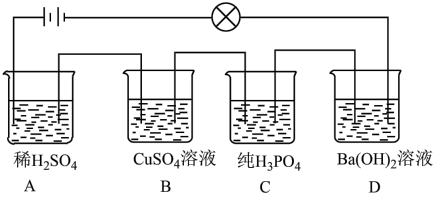
①加水的烧杯为___________ 。
②向烧杯A滴入 溶液,溶液导电性
溶液,溶液导电性___________ 。
A.变强 B.变弱 C.先变弱后变强 D.先变强后变弱
③ 是三元酸,能生成
是三元酸,能生成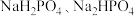 两种酸式盐和
两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸 (H3PO3)。已知:
一种正盐。磷还有一种含氧酸叫亚磷酸 (H3PO3)。已知: 与
与 反应只生成
反应只生成 和
和 两种盐。那么
两种盐。那么 为
为___________ (填“正盐”或“酸式盐”);写出 与少量
与少量 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(1)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是
②上述物质中既不是电解质也不是非电解质的是
③有下列三种物质:
 ;
; ;
; ;
;a.写出上述物质中的盐在熔融状态下的电离方程式
b.写出上述物质中的酸与氨水反应的离子方程式
(2)在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来;

①加水的烧杯为
②向烧杯A滴入
 溶液,溶液导电性
溶液,溶液导电性A.变强 B.变弱 C.先变弱后变强 D.先变强后变弱
③
 是三元酸,能生成
是三元酸,能生成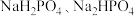 两种酸式盐和
两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸 (H3PO3)。已知:
一种正盐。磷还有一种含氧酸叫亚磷酸 (H3PO3)。已知: 与
与 反应只生成
反应只生成 和
和 两种盐。那么
两种盐。那么 为
为 与少量
与少量 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列物质:① 晶体;②
晶体;② ;③液态醋酸;④水银;⑤
;③液态醋酸;④水银;⑤ ;⑥蔗糖;⑦
;⑥蔗糖;⑦ 胶体;⑧氨水;⑨
胶体;⑧氨水;⑨ 溶液;⑩熔融的氯化钠。
溶液;⑩熔融的氯化钠。
(1)上述物质中,能导电的是_______ (填序号,下同);属于非电解质的是_______ ;属于强电解质的是_______ ;弱电解质在水溶液中的电离方程式:_______ ;
(2)若将①和⑨在溶液中按照溶质 混合,反应的离子方程式为
混合,反应的离子方程式为_______ ,此时溶液呈_______ (填“酸性”、“碱性”或“中性”)。若继续往所得溶液中加入①,则反应的离子方程式为_______ 。
(3)写出⑤在水溶液中的电离方程式_______ 。
(4)若将③逐渐加入⑧中,发生反应的离子方程式为_______ 。
 晶体;②
晶体;② ;③液态醋酸;④水银;⑤
;③液态醋酸;④水银;⑤ ;⑥蔗糖;⑦
;⑥蔗糖;⑦ 胶体;⑧氨水;⑨
胶体;⑧氨水;⑨ 溶液;⑩熔融的氯化钠。
溶液;⑩熔融的氯化钠。(1)上述物质中,能导电的是
(2)若将①和⑨在溶液中按照溶质
 混合,反应的离子方程式为
混合,反应的离子方程式为(3)写出⑤在水溶液中的电离方程式
(4)若将③逐渐加入⑧中,发生反应的离子方程式为
您最近一年使用:0次
【推荐1】2020年春“新冠病毒”疫情肆虐,在全国抗击“新冠肺炎”的战役中使用了大量的含氯消毒剂,原料氯气的制备有多种方法。回答下列问题:
(1)用离子方程式表示实验室制取氯气的化学反应原理为:_______
该反应中氧化剂是_______ (填化学式),被氧化的元素是_______ (元素符号)。该反应中氧化剂和还原剂的物质的量之比为_______
(2)配平下列化学方程式并用单线桥法表示电子转移的方向和数目:_______
_______KClO3+_______HC1(浓)→_______KCl+_______C12↑+_______H2O
(3)有一种“地康法”制取氯气,是在氯化铜的催化作用下,在450℃用空气中氧气跟氯化氢反应制氯气。反应原理如下所示。

①分步反应I属于_______ 反应(填四种基本反应类型之一)。
②“地康法”制取氯气的总反应方程式为:_______ 。
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种对环境无污染的气体,试写出该反应的化学方程式:_______ 。
(1)用离子方程式表示实验室制取氯气的化学反应原理为:
该反应中氧化剂是
(2)配平下列化学方程式并用单线桥法表示电子转移的方向和数目:
_______KClO3+_______HC1(浓)→_______KCl+_______C12↑+_______H2O
(3)有一种“地康法”制取氯气,是在氯化铜的催化作用下,在450℃用空气中氧气跟氯化氢反应制氯气。反应原理如下所示。

①分步反应I属于
②“地康法”制取氯气的总反应方程式为:
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种对环境无污染的气体,试写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题。
(1)按要求书写下列反应的离子方程式。
①向澄清石灰水中通入少量二氧化碳,请写出此反应的离子方程式:___________ 。
②锌粒投入稀硫酸中,溶液中氢离子的量减少,锌离子的量增加,___________ 离子的量没有变化,反应的离子方程式是___________ 。
③向 溶液中逐滴加入
溶液中逐滴加入 溶液至中性,请写出发生反应的离子方程式:
溶液至中性,请写出发生反应的离子方程式:___________ 。
④ 溶液与
溶液与 溶液混合,发生反应的离子方程式是
溶液混合,发生反应的离子方程式是___________ 。
(2)以下为中学化学中常见的几种物质:①二氧化碳;②熔融 ;③
;③ 固体;④铜;5稀硫酸;⑥澄清石灰水。其中属于电解质的有
固体;④铜;5稀硫酸;⑥澄清石灰水。其中属于电解质的有___________ (填序号,下同),属于非电解质的有___________ 。
(3)高铁酸钠( )(铁元素为
)(铁元素为 价)是一种新型的净水剂,可以通过下述反应制取:
价)是一种新型的净水剂,可以通过下述反应制取:
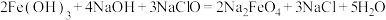
①该反应中氧化剂是___________ (用化学式表示),___________ 元素被氧化(填元素名称),还原产物为___________ (用化学式表示)。
②用单线桥表示反应中电子转移的情况:___________ 。
(1)按要求书写下列反应的离子方程式。
①向澄清石灰水中通入少量二氧化碳,请写出此反应的离子方程式:
②锌粒投入稀硫酸中,溶液中氢离子的量减少,锌离子的量增加,
③向
 溶液中逐滴加入
溶液中逐滴加入 溶液至中性,请写出发生反应的离子方程式:
溶液至中性,请写出发生反应的离子方程式:④
 溶液与
溶液与 溶液混合,发生反应的离子方程式是
溶液混合,发生反应的离子方程式是(2)以下为中学化学中常见的几种物质:①二氧化碳;②熔融
 ;③
;③ 固体;④铜;5稀硫酸;⑥澄清石灰水。其中属于电解质的有
固体;④铜;5稀硫酸;⑥澄清石灰水。其中属于电解质的有(3)高铁酸钠(
 )(铁元素为
)(铁元素为 价)是一种新型的净水剂,可以通过下述反应制取:
价)是一种新型的净水剂,可以通过下述反应制取: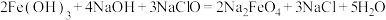
①该反应中氧化剂是
②用单线桥表示反应中电子转移的情况:
您最近一年使用:0次
【推荐3】阅读下面科普信息,回答问题:一个体重50kg的健康人含铁2g,这2g铁在入体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是_______ (填字母)。
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有_______ 性。下列不能实现上述转化的物质是_______ (填字母)。
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有_______ 性。
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,则56gFe参加反应时,被还原的HNO3为_______ g。
(5)请用双线桥法标出已知化学方程式电子转移的方向和数目:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑_______ 。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,则56gFe参加反应时,被还原的HNO3为
(5)请用双线桥法标出已知化学方程式电子转移的方向和数目:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑
您最近一年使用:0次



