某兴趣小组利用铁在氧气中燃烧的产物磁性氧化铁做如下实验:
(1)磁性氧化铁与铝在一定条件下发生反应时,氧化剂与还原剂的物质的量之比为___________ 。将磁性氧化铁完全溶于较浓的盐酸中,得到棕黄色的浓溶液,其反应的离子方程式为___________ 取少量所得溶液加入双氧水,其反应的离子方程式为___________ 。
(2)取适量(1)中所得的棕黄色溶液于试管中,向其中加入稍过量的铁粉,发生主要反应的离子方程式为___________ ;静置后向上层清液中加入NaOH溶液,并放置一段时间,观察到的实验现象为___________ 。
(3)另取(1)中所得的棕黄色溶液于试管中,向其中通入足量的氯气,所发生反应的化学方程式为___________ 。写出高炉炼铁中一氧化碳还原氧化铁的化学方程式:___________ 。
(1)磁性氧化铁与铝在一定条件下发生反应时,氧化剂与还原剂的物质的量之比为
(2)取适量(1)中所得的棕黄色溶液于试管中,向其中加入稍过量的铁粉,发生主要反应的离子方程式为
(3)另取(1)中所得的棕黄色溶液于试管中,向其中通入足量的氯气,所发生反应的化学方程式为
更新时间:2023-07-05 22:30:40
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有物质:①酒精②NaCl固体③SO3④Na2CO3溶液⑤熔融K2SO4⑥CaO⑦CH3COOH⑧银⑨新制氯水⑩CO2⑪)稀硫酸⑫NaOH溶液。
回答下列问题:
(1)上述物质属于盐的是________ (填序号,下同)。
(2)上述物质属于电解质的是________ 。
(3)上述物质属于酸性氧化物的是________ 。
(4)足量的⑩通入少量的⑫中发生反应的离子方程式为________ 。
(5)④和足量⑪发生反应的离子方程式为_________ 。
(6)将⑨滴到pH试纸上的现象是________ ,说明了该溶液具有________ 。
回答下列问题:
(1)上述物质属于盐的是
(2)上述物质属于电解质的是
(3)上述物质属于酸性氧化物的是
(4)足量的⑩通入少量的⑫中发生反应的离子方程式为
(5)④和足量⑪发生反应的离子方程式为
(6)将⑨滴到pH试纸上的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.现有以下物质:①铁;②液氨;③CO2;④NaHSO4固体;⑤Ba(OH)2溶液;⑥熔融态NaOH;⑦盐酸;⑧固态醋酸;⑨Fe(OH)3胶体;⑩液态硫酸。请回答下列问题:
(1)以上物质中属于非电解质的是___________ (填序号,下同),属于电解质的有___________ ,能导电的物质有___________ 。
(2)若向⑨中逐滴加入⑩的水溶液实验现象是___________
(3)写出向④的水溶液中加入⑤反应至恰好沉淀完全的离子方程式___________ 。
Ⅱ.双氧水H2O2和水都是极弱电解质,但H2O2显极弱的酸性。
(4)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:___________ 。
(5)鉴于 H2O2显弱酸性,它能同强碱作用形成“正盐”,在一定条件下也可形成“酸式盐”。请写出H2O2与Ba(OH)2作用形成的“正盐”的化学方程式:___________ 。
(1)以上物质中属于非电解质的是
(2)若向⑨中逐滴加入⑩的水溶液实验现象是
(3)写出向④的水溶液中加入⑤反应至恰好沉淀完全的离子方程式
Ⅱ.双氧水H2O2和水都是极弱电解质,但H2O2显极弱的酸性。
(4)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:
(5)鉴于 H2O2显弱酸性,它能同强碱作用形成“正盐”,在一定条件下也可形成“酸式盐”。请写出H2O2与Ba(OH)2作用形成的“正盐”的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】观察氧化物和酸碱盐的关系:
回答下列问题:
(1)横向从价态的视角,发现氧化物的中心元素价态越高,往往_______ 性越强;Pb元素有 、
、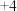 两种常见化合价,则对应氧化物碱性更强的是
两种常见化合价,则对应氧化物碱性更强的是_______ (填化学式)。
(2)纵向从对应酸碱盐的视角,发现氧化物与酸或碱反应成盐时,酸性氧化物提供盐中_______ ,碱性氧化物提供盐中_______ ;(选填编号)
A.金属阳离子 B.氢离子 C.含氧酸根离子 D.氯离子
(3)将 放入
放入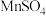 溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性:
溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性:
_______ 、MnO_______ 。
(4)Ti可以形成两种盐: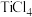 、
、 (微溶物),则
(微溶物),则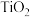 属于
属于_______ 氧化物(填性质)。写出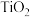 与浓NaOH溶液反应的离子方程式:
与浓NaOH溶液反应的离子方程式:_______ 。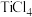 极易与水反应生成
极易与水反应生成 ,过滤后煅烧可制得
,过滤后煅烧可制得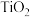 ,试写出生成
,试写出生成 时的化学反应方程式:
时的化学反应方程式:_______ 。
| 对应盐 | 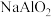 |  |  |  |  | ||
| 对应酸 |  |  | 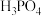 |  | 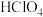 | ||
| 氧化物/性质 |  强碱性 | MgO 中强碱性 |  两性 |  弱酸性 |  中强酸性 |  强酸性 |  更强酸性 |
| 对应碱 | NaOH |  |  | ||||
| 对应盐 | NaCl | 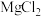 | 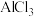 |
(1)横向从价态的视角,发现氧化物的中心元素价态越高,往往
 、
、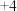 两种常见化合价,则对应氧化物碱性更强的是
两种常见化合价,则对应氧化物碱性更强的是(2)纵向从对应酸碱盐的视角,发现氧化物与酸或碱反应成盐时,酸性氧化物提供盐中
A.金属阳离子 B.氢离子 C.含氧酸根离子 D.氯离子
(3)将
 放入
放入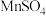 溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性:
溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性:
(4)Ti可以形成两种盐:
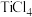 、
、 (微溶物),则
(微溶物),则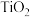 属于
属于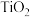 与浓NaOH溶液反应的离子方程式:
与浓NaOH溶液反应的离子方程式: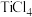 极易与水反应生成
极易与水反应生成 ,过滤后煅烧可制得
,过滤后煅烧可制得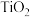 ,试写出生成
,试写出生成 时的化学反应方程式:
时的化学反应方程式:
您最近一年使用:0次
【推荐1】二氧化氯( )是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。回答下列问题:
)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。回答下列问题:
(1) 的制备:制备
的制备:制备 的常用方法有两种,分别为
的常用方法有两种,分别为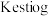 法、
法、 与
与 反应法。
反应法。
① 法制备
法制备 的原理为
的原理为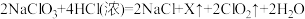 ,X的化学式为
,X的化学式为___________ ,将 通入
通入 溶液中,有红褐色沉淀生成,溶液中的主要阴离子为
溶液中,有红褐色沉淀生成,溶液中的主要阴离子为 、
、 ,若消耗
,若消耗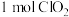 ,则被氧化的
,则被氧化的 为
为___________  。
。
② 与
与 反应法制备
反应法制备 ,生成物只有两种,参加反应的
,生成物只有两种,参加反应的 与
与 物质的量之比为
物质的量之比为___________ ,与 法相比,
法相比, 与
与 反应法的优点是
反应法的优点是___________ (填一条)。
(2) 的用途:除毒、除异味。
的用途:除毒、除异味。
① 可以将剧毒的氰化物氧化成
可以将剧毒的氰化物氧化成 和
和 ,离子方程式为
,离子方程式为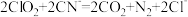 ,
, 属于
属于___________ (填“酸”“碱”或“两”)性氧化物,每转移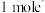 ,生成
,生成___________ L(标准状况下) 。
。
② 能把水溶液中有异味的
能把水溶液中有异味的 氧化成四价锰,使之形成不溶于水的
氧化成四价锰,使之形成不溶于水的 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
 )是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。回答下列问题:
)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。回答下列问题:(1)
 的制备:制备
的制备:制备 的常用方法有两种,分别为
的常用方法有两种,分别为 法、
法、 与
与 反应法。
反应法。①
 法制备
法制备 的原理为
的原理为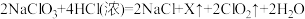 ,X的化学式为
,X的化学式为 通入
通入 溶液中,有红褐色沉淀生成,溶液中的主要阴离子为
溶液中,有红褐色沉淀生成,溶液中的主要阴离子为 、
、 ,若消耗
,若消耗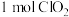 ,则被氧化的
,则被氧化的 为
为 。
。②
 与
与 反应法制备
反应法制备 ,生成物只有两种,参加反应的
,生成物只有两种,参加反应的 与
与 物质的量之比为
物质的量之比为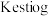 法相比,
法相比, 与
与 反应法的优点是
反应法的优点是(2)
 的用途:除毒、除异味。
的用途:除毒、除异味。①
 可以将剧毒的氰化物氧化成
可以将剧毒的氰化物氧化成 和
和 ,离子方程式为
,离子方程式为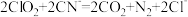 ,
, 属于
属于 ,生成
,生成 。
。②
 能把水溶液中有异味的
能把水溶液中有异味的 氧化成四价锰,使之形成不溶于水的
氧化成四价锰,使之形成不溶于水的 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据下列各组信息,完成有关问题:
(1)根据反应Cu+4HNO3 (浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原产物是_______ 。
②未被还原的硝酸与参加反应的总硝酸的质量之比为_______ 。
(2)氢能是一种极具发展潜力的清洁能源,以太阳能为热源,热化学硫碳循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
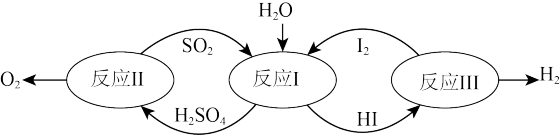
反应Ⅰ的化学方程式:_______
(3)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,配平该反应的化学方程式,并在方程式上用单线桥标出电子转移:_______
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2↑+_______Cl2↑+_______H2O
(4)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O
、Cl-、H2O
①写出并配平湿法制高铁酸钾反应的离子程式_______ 。
②每生成1个FeO 转移
转移_______ 个电子,若反应过程中转移了3个电子,则生产_______ 个还原产物。
(1)根据反应Cu+4HNO3 (浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原产物是
②未被还原的硝酸与参加反应的总硝酸的质量之比为
(2)氢能是一种极具发展潜力的清洁能源,以太阳能为热源,热化学硫碳循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

反应Ⅰ的化学方程式:
(3)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,配平该反应的化学方程式,并在方程式上用单线桥标出电子转移:
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2↑+_______Cl2↑+_______H2O
(4)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O
、Cl-、H2O①写出并配平湿法制高铁酸钾反应的离子程式
②每生成1个FeO
 转移
转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,此反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、Cr2(SO4)3、K2SO4、H2O七种物质。
(1)若将碳纳米颗粒分散到一定溶剂中,形成稳定的分散系,其所具有的性质是__________ 。
①丁达尔效应 ②加入饱和(NH4)2SO4溶液产生聚沉 ③可通过半透膜
(2)请用上述物质填空,并配平化学方程式:____C+____+____H2SO4→____K2SO4+________+____Cr2(SO4)3+____ H2O。
(3)H2SO4在上述反应中表现出来的性质是________ (填选项编号)。
A.氧化性 B.氧化性和酸性
C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为____________ 。
(1)若将碳纳米颗粒分散到一定溶剂中,形成稳定的分散系,其所具有的性质是
①丁达尔效应 ②加入饱和(NH4)2SO4溶液产生聚沉 ③可通过半透膜
(2)请用上述物质填空,并配平化学方程式:____C+____+____H2SO4→____K2SO4+________+____Cr2(SO4)3+
(3)H2SO4在上述反应中表现出来的性质是
A.氧化性 B.氧化性和酸性
C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.分别只用一种试剂除去下列各组中所含的少量杂质(括号内为杂质),在空格中填上需加入最适合的一种试剂:
(1)FeCl3溶液(FeCl2)________________ ,
(2)FeCl2溶液(FeCl3)________________ ,
(3)Fe 粉末(Al)_______________ ,
Ⅱ.为测定某镁铝合金样品中铝的含量,进行了下列实验:取一定量合金,加入100 mL 0.3 mol·L-1稀硝酸,合金完全溶解,产生的气体在标准状况下体积为560 mL;再加入0.2 mol·L-1 NaOH溶液至沉淀质量恰好不再变化,用去300 mL NaOH溶液。则所取样品中铝的物质的量为___________ ,反应中转移的电子数为______________ 。
(1)FeCl3溶液(FeCl2)
(2)FeCl2溶液(FeCl3)
(3)Fe 粉末(Al)
Ⅱ.为测定某镁铝合金样品中铝的含量,进行了下列实验:取一定量合金,加入100 mL 0.3 mol·L-1稀硝酸,合金完全溶解,产生的气体在标准状况下体积为560 mL;再加入0.2 mol·L-1 NaOH溶液至沉淀质量恰好不再变化,用去300 mL NaOH溶液。则所取样品中铝的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】填写下列空白:
(1)FeCl3溶液中加入铁粉,溶液由___ 色变为___ 色,该反应的离子方程式为______ ;
(2)除去FeCl3溶液中混有的FeCl2需向溶液中通入______ (填物质名称),该反应的离子方程式为______ ;
(3)在Fe3O4 +4CO 3Fe+4CO 2的反应中,
3Fe+4CO 2的反应中,_____ 是氧化剂,被氧化的元素为____ ,氧化产物是________ ,若有11.6g Fe3O4参加反应则转移电子的物质的量为__________ 。
(1)FeCl3溶液中加入铁粉,溶液由
(2)除去FeCl3溶液中混有的FeCl2需向溶液中通入
(3)在Fe3O4 +4CO
 3Fe+4CO 2的反应中,
3Fe+4CO 2的反应中,
您最近一年使用:0次



